ウイルス型ワクチンの製造
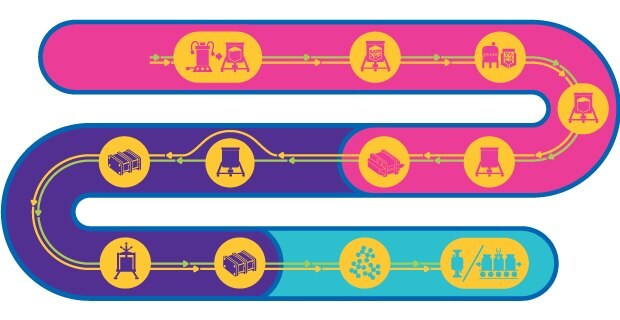
不活化ウイルス・弱毒化生ウイルスの一連のプロセス
関連技術資料
- アジュバントの選択は、ワクチン製剤と個別の用途によって異なります。アジュバントの選択において有効性と安全性は最も重要ですが、その他の多くの特性を考慮する必要があります
- すべて表示 (0)
技術資料・プロトコールの検索
的確なスケールアップによるアップストリームの生産性と清澄化を最適化する
ウイルス型のワクチン製造用に開発されたアップストリームの培養工程は、生産性を満たすように最適化する必要があります。この最適化の作業には、細胞および細胞デブリスの除去やウイルスの回収に不可欠な清澄化のステップなどが含まれます。 しかし、商用製造スケールへのスケールアップができない限り、アップストリームの工程がうまくいくことはありません。
不純物を確実に除去し、収率と効率の目標を達成する
細胞由来の核酸は、ウイルスベースワクチンのプロセスでよく見られる不純物です。規制では、キャリーオーバーされる宿主細胞の核酸の濃度は、ワクチン一容量当たり10 ng未満とすることが求められています。Benzonase®エンドヌクレアーゼ阻害薬の使用後に行うタンジェンシャルフローフィルトレーションは、残った核酸成分を分解・除去する確実で強力な組み合わせです。
ダウンストリームの回収率を最大化する
Benzonase®エンドヌクレアーゼ阻害薬は、濃縮およびダイアフィルトレーションの際に、大半のワクチンに求められるレベルの純度を十分達成できます。ただし、日本脳炎ウイルス(JEV)やデング熱ウイルス(DENV)といった、次世代のワクチンについての純度を達成するためには、クロマトグラフィーが必要です。製造の各工程は、ウイルスの特性に合わせて調整する必要があります。そのため、最適な回収率を保証しつつ目的とする純度を達成するためには、ダウンストリームにおける精製が不可欠です。
患者の安全を保証する
ウイルス型のワクチンは弱毒化ウイルスを用いて製造されていますが、患者の安全保証は依然として懸念されます。最終的なウイルスワクチンのバルクは、大量の水と同じようなものです。そのため、製剤および充填の最終ステップに進む前に、滅菌ろ過(0.22 µm)を使用して滅菌できます。

バイオプロセッシング液体細胞培養用培地・バッファー
メルクには業界最高の品質を誇るろ過滅菌液体製品の製造施設があり、お客様のバイオ医薬品製造を最適化するために世界中のGMP施設からすぐに使える細胞培養培地、液体バッファー、CIP製品、SIP製品をお届けしています。

ダウンストリーム - タンジェンシャルフローフィルトレーション

最終無菌ろ過と充填
最終充填要件を効率化し、現行の規制要件に準拠しながら、製品交叉汚染の懸念を取り除きます。
関連資料
- アプリケーションガイド:バイオ医薬品
製造に伴う課題を克服する役に立つ検索ツール。
- カタログ:ワクチン製造ハンドブック
このハンドブックでは、ワクチン製造プロセスならびにあらゆる種類のワクチン開発プラットフォームのプロセス改善について説明しています。
- ミニハンドブック:セルベースワクチン製造
弱毒化生ウイルスワクチンは、複数の工程で構成される複雑な細胞ベースの製造プロセスを用いて作られます。テンプレート化されたプロセスではありません。各ウイルスワクチンの製造プロセスは異なります。
- 電子書籍:ワクチン製造プラットフォームのための能力と解決方法
プロセス開発からフルスケールのGMP製造まで、世界中にあるメルクのワクチン製造施設は、ウイルス型ワクチン、サブユニットワクチン、VLPウイルスベクターワクチン、pDNA/mRNAワクチンなどお客様のあらゆるモダリティ/プラットフォームで目標を達成する役に立ちます。
- ホワイトペーパー:Filtration Strategies for Optimal Development and Purification of a Foot and Mouth Disease Virus
メルクは、スケーラブルでコスト効率の高いGMP準拠プロセスを確立するために、FMDワクチン製造のアップストリーム・ダウンストリームプロセスの最適化でMEVACとコラボレーションしました。このホワイトペーパーでは、アップストリームとダウンストリームのプロセスにおける新しいろ過戦略の統合に注目します。
- ホワイトペーパー:メンブレンクロマトグラフィーを用いたウイルス精製におけるダウンストリームプロセス強化
このホワイトペーパーでは、ウイルス製造の現行アプローチに伴う課題、ならびにさまざまなウイルスモダリティで使用可能でプロセス開発を加速させるプラットフォームアプローチを開発するチャンスについて概説します。
- アプリケーションノート:Effect of Benzonase® Endonuclease Addition to Purification of Sabin Polio Virus Type 3
このアプリケーションノートでは、ポリオウイルス3型生産プロセスでBenzonase® エンドヌクレアーゼを使用する利点をまとめています。
- 技術資料:Filter-Based Clarification of Viral Vaccines and Vectors
この技術資料では、さまざまなろ過技術とウイルスワクチン清澄化におけるそれらの応用を包括的に概説し、課題や現行ベストプラクティスを紹介しています。
続きを確認するには、ログインするか、新規登録が必要です。
アカウントをお持ちではありませんか?


