AP112P
Anticorpo anti-IgG humano de cabra, conjugado com HRP
Chemicon®, from goat
Sinônimo(s):
Conjugado HRP de IgG anti-humana
About This Item
Produtos recomendados
fonte biológica
goat
Nível de qualidade
conjugado
peroxidase conjugate
forma do anticorpo
affinity isolated antibody
tipo de produto de anticorpo
secondary antibodies
clone
polyclonal
forma
lyophilized
reatividade de espécies
human
fabricante/nome comercial
Chemicon®
técnica(s)
ELISA: suitable
western blot: suitable
Isotipo
IgG
Condições de expedição
wet ice
temperatura de armazenamento
2-8°C
modificação pós-traducional do alvo
unmodified
Descrição geral
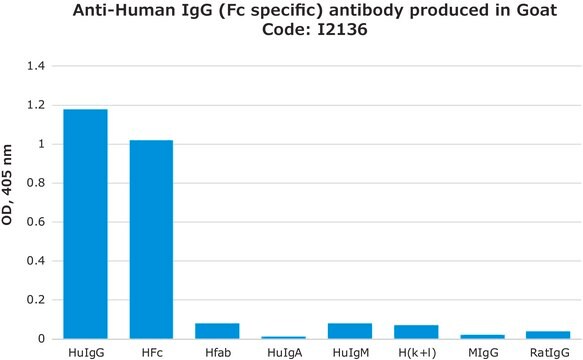
Especificidade
Imunogênio
Aplicação
- para detectar a imunoglobulina G (IgG) ligada no ensaio de imunoabsorção enzimática (ELISA)
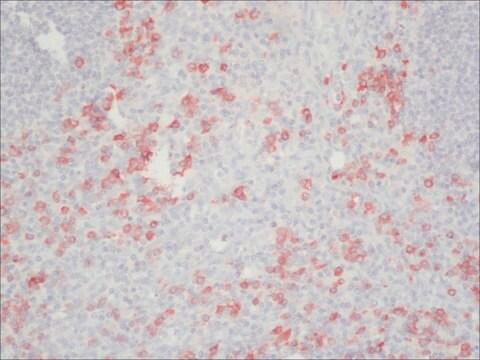
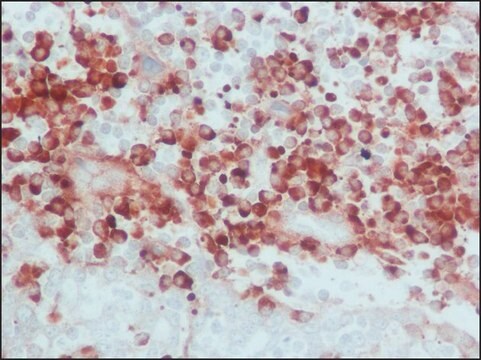
- em imuno-histoquímica ou citoquímica na diluição de 1:500 - 1:5.000
- para análises Western Blot com substratos cromogênicos na diluição de 1:5.000 - 1:100.000 e com substratos ECL na diluição de 1:10.000 - 1:200.000.
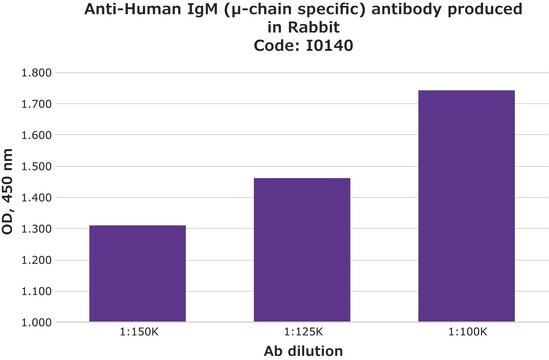
- para EIA na diluição de 1:5.000-1:100.000
Ações bioquímicas/fisiológicas
forma física
Armazenamento e estabilidade
AVISO:
O uso de azida sódica como conservante inibirá significativamente a atividade enzimática da peroxidase de rábano (HRP).
Outras notas
Anticorpos secundários de imunoglobulinas inteiras
Informações legais
Exoneração de responsabilidade
Não está encontrando o produto certo?
Experimente o nosso Ferramenta de seleção de produtos.
Código de classe de armazenamento
13 - Non Combustible Solids
Classe de risco de água (WGK)
WGK 3
Ponto de fulgor (°F)
Not applicable
Ponto de fulgor (°C)
Not applicable
Certificados de análise (COA)
Busque Certificados de análise (COA) digitando o Número do Lote do produto. Os números de lote e remessa podem ser encontrados no rótulo de um produto após a palavra “Lot” ou “Batch”.
Já possui este produto?
Encontre a documentação dos produtos que você adquiriu recentemente na biblioteca de documentos.
Os clientes também visualizaram
Nossa equipe de cientistas tem experiência em todas as áreas de pesquisa, incluindo Life Sciences, ciência de materiais, síntese química, cromatografia, química analítica e muitas outras.
Entre em contato com a assistência técnica