おすすめの製品
アプリケーション
BChE活性の選択的阻害は、有機リン酸エステルの検出に使用されます。有機リン中毒の治療における使用が検討されています。ヒトの血中 BChE濃度は、有毒である可能性のある神経ガスに対する防御の程度と相関することが報告されています。コリンエステラーゼは、アルツハイマー病における役割についても研究されています。
生物化学的/生理学的作用
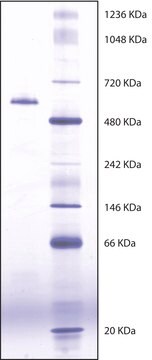
ブチルコリンエステラーゼ(BChE)はセリン加水分解酵素であり、アセチルコリンエステラーゼ(AChE)と構造的には似ていますが、基質特異性と阻害剤感受性が異なります。BChEは、AChEと異なり、ブチルコリンやベンゾイルコリンなどの比較的大きなコリンエステルを効率的に加水分解することができます。この酵素は、4つの等しいサブユニット(各110 kDa)をもつ四量体糖タンパク質です。この酵素は、Ca2+とMg2+によって活性化されます。pH域6.0~8.0で活性は一定です。ベタイン、ニコチン、有機リン酸エステル、カルバマートによって阻害されます。
単位の定義
1ユニットは、pH 8.0、37°C、1分間に、1.0 μmolのブチリルコリンをコリンと酪酸に加水分解する酵素量です。ブチリルコリンを基質とした場合の活性は、アセチルコリンを基質とした場合の約2.5倍となります。
物理的形状
バッファ-塩を含有する高純度物質
アナリシスノート
タンパク量はビウレット法で測定
シグナルワード
Danger
危険有害性情報
危険有害性の分類
Resp. Sens. 1
保管分類コード
11 - Combustible Solids
WGK
WGK 3
引火点(°F)
Not applicable
引火点(℃)
Not applicable
個人用保護具 (PPE)
Eyeshields, Gloves, type N95 (US)
適用法令
試験研究用途を考慮した関連法令を主に挙げております。化学物質以外については、一部の情報のみ提供しています。 製品を安全かつ合法的に使用することは、使用者の義務です。最新情報により修正される場合があります。WEBの反映には時間を要することがあるため、適宜SDSをご参照ください。
Jan Code
C1057-BULK:
C1057-100UN:
C1057PROC:
C1057-5KU:
C1057-500UN:
C1057-VAR:
C1057-1KU:
C1057-CP:
この製品を見ている人はこちらもチェック
Tarek Mohamed et al.
Bioorganic & medicinal chemistry letters, 20(12), 3606-3609 (2010-05-18)
A group of 2,4-disubstituted pyrimidine derivatives (7a-e, 8a-e and 9a-d) that possess a variety of C-2 aliphatic five- and six-membered heterocycloalkyl ring in conjunction with a C-4 arylalkylamino substituent were designed, synthesized and evaluated as cholinesterase (ChE) inhibitors. The steric
Keriman Ozadali-Sari et al.
Bioorganic chemistry, 72, 208-214 (2017-05-10)
The present study describes the synthesis, pharmacological evaluation (BChE/AChE inhibition, Aβ antiaggregation, and neuroprotective effects), and molecular modeling studies of novel 2-[4-(4-substitutedpiperazin-1-yl)phenyl]benzimidazole derivatives. The alkyl-substituted derivatives exhibited selective inhibition on BChE with varying efficiency. Compounds 3b and 3d were found
Jianhua Liu et al.
The Journal of clinical endocrinology and metabolism, 93(5), 1980-1987 (2008-03-20)
Ghrelin, an acylated peptide hormone secreted from the gut, regulates appetite and metabolism. Elucidating its pattern of secretion in the fed and fasted states is important in the face of the obesity epidemic. Our objective was to examine changes in
R M Blong et al.
The Biochemical journal, 327 ( Pt 3), 747-757 (1998-05-15)
Butyrylcholinesterase (BChE) in human serum consists predominantly of tetramers. Recombinant BChE, however, expressed in Chinese hamster ovary (CHO) cells, consists of approx. 55% dimers, 10-30% tetramers and 15-40% monomers. To determine the origin of the monomer species we added the
Determination of butyrylcholinesterase inhibition using ion transfer across the interface between two immiscible liquids
Beattie PD, et al.
Analytical Chemistry, 66(1), 52-57 (1994)
ライフサイエンス、有機合成、材料科学、クロマトグラフィー、分析など、あらゆる分野の研究に経験のあるメンバーがおります。.
製品に関するお問い合わせはこちら(テクニカルサービス)