ADC Manufacturing
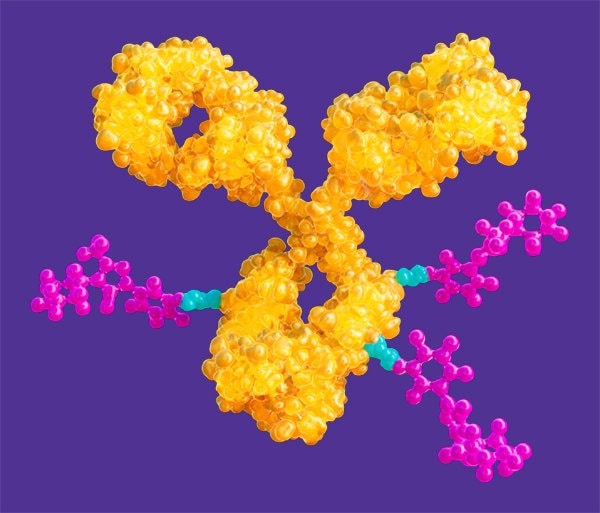
Technologia koniugacji przeciwciał z lekami (ADC) wykorzystuje przeciwciała monoklonalne (mAbs) do dostarczania silnych, wysoce aktywnych składników farmaceutycznych (HPAPI) do komórek docelowych. W postaci skoniugowanej, HPAPI wykazują selektywną cytotoksyczność, która może uchronić komórki niedocelowe przed toksycznymi skutkami. Realizacja ogromnego potencjału technologii ADC jest jednak trudna i złożona. Zaawansowane zestawy produkcyjne i dedykowany sprzęt są niezbędne do scharakteryzowania cząsteczki i wykazania jej czystości, jednorodności i stabilności. Skuteczne połączenie unikalnego, ukierunkowanego na nowotwór mAb z silnym, zabijającym komórki cytotoksycznym lekiem małocząsteczkowym to dopiero początek - zaspokojenie potrzeb produkcyjnych ADC wymaga kompleksowego portfolio produktów i szerokiej wiedzy specjalistycznej w zakresie rozwoju, produkcji i testowania małych i dużych cząsteczek. |
Powiązane artykuły techniczne
- ADC to szybko rozwijająca się metoda leczenia nowotworów. Dowiedz się więcej o częściach ADC, działaniu biokoniugatów i procesie produkcji ADC.
- Meta opis: Półprodukty ładunku ADC, takie jak DOLCore ™, MAYCore ™ i PBDCore ™, upraszczają syntezę ładunku dla najczęściej używanych ładunków: maytansyny, dolastatyny i dimerów PBD.
- Zobacz dane na temat tego, jak chito-oligosacharyd ChetoSensar™ pokonuje wyzwania związane z rozpuszczalnością ADC.
- Zapoznaj się z najlepszymi praktykami dotyczącymi stosowania kapsułek Pellicon® w przetwarzaniu ADC, a także z danymi z dwóch badań wykorzystujących kapsułki Pellicon® i kasety Pellicon® w procesie produkcji ADC.
Powiązane zasoby dotyczące produktów
- Brochure: Biopharmaceutical and ADC Processing Portfolio
The document outlines the complexities of Antibody Drug Conjugate (ADC) development and emphasizes the expertise and integrated services offered to advance ADCs to market efficiently.
- White Paper: Know your ADC’s Critical Quality Attributes
The increased focus on cancer has led to the rapid development of antibody drug conjugates (ADCs), a highly effective class of oncology therapeutics with a projected global market value of $7.5 billion by 2025.
- White Paper: Commercializing Antibody-drug Conjugates: a CMO’s Journey
In this white paper, we outline how our organization used over 12 years of experience to establish commercial-scale ADC manufacturing capabilities.
- Poster: Efficacy Screening of Antibody-Drug-Conjugates by Surface Plasmon Resonance
The intro details the complexity and challenges in characterizing antibody-drug conjugates (ADCs) and the factors influencing their effectiveness, especially in tumor targeting. It also mentions a study that expands the investigation into linker and toxin variation and binding activities using Surface Plasmon Resonance (SPR).
- Poster: Novel Format Conjugates – Process and Analytical
Bioconjugation technology have greatly improved the efficacy of treatments for diseases previously difficult to address with traditional ADC therapies, leading to a demand for clinical supplies.
- PDF: ADC Express™ Services for Best Candidate Selection
As a leading CTDMO in the ADC space, we offer a rapid approach for developing ADC constructs and provide efficient bioconjugation capabilities for developers needing ADC library generation. Our ADC Express™ Service facilitates the transition to development and GMP manufacturing for candidates entering the clinic.
- White Paper: Benefits of Monodisperse and Activated PEGs in ADC Development
The whitepaper highlights the use of PEGs to enhance solubility in ADC development, emphasizing the importance of ADCs in delivering drugs directly to tumors while minimizing damage to healthy tissue.
- White Paper: Use of Payload Core Compounds to Accelerate ADC Clinical Development Timelines
ADCs treat diseases like cancer by targeting specific cells to minimize off-target toxicity. Eleven are approved, with hundreds in development.
- Technical Flyer: ADCore Payload Intermediates: Simplify Your Payload Synthesis
ADCore products are cGMP quality advanced intermediates that help accelerate drug development efforts by reducing the number of development and manufacturing steps needed to produce Maytansinoid, Dolastatin, or Pyrrolobenzodiazepine (PBD)payloads.
- Technical Flyer: ChetoSensar™
Our ChetoSensar™ Technology can help to improve the solubility of ADCs and provides access to highly hydrophobic novel payloads that might not be considered.
- Technical Flyer: Maytansinoid GMP Quality Payloads for Your Drug Conjugate Programs
Our maytansinoid products aim to expedite your journey to the clinic. Offerings include GMP quality DM1-Mertansine for drug conjugate programs and MAYCore™ intermediate for simplified payload synthesis. These products feature high purity, free samples, and regulatory filing support, suitable for phase I clinical studies with valid processes.
- Brochure: Biopharmaceutical and ADC Process Application Guide
Developing an Antibody Drug Conjugate (ADC) demands expertise in small and large molecule development, manufacturing, formulation, and testing.
- Data Sheet: Eshmuno® CMX mix-mode chromatography resin
- Case Study: Complete Single-use ADC technology, from development to scale-up
The global antibody-drug conjugate (ADC) market is rapidly expanding, with an estimated 22% compound annual growth rate (CAGR) from 2017 to 2022.
- Application Note: Compatibility of a Mobius® Single-use Solution for ADC Processing
ADCs, a fast-growing biomolecule class in oncology therapeutics, include a monoclonal antibody (mAb), linker, and cytotoxic payload, all contributing to therapeutic efficacy
- Poster: Mobius® Single-use ADC Technology Supporting ADC Processing
Our Mobius® line provides a comprehensive single-use bioprocessing portfolio, featuring mixers, chromatography, and tangential flow filtration systems ideal for antibody drug conjugate production.
- Application Note: Pellicon® Capsules for Ultrafiltration/Diafiltration of ADCs
Tangential flow filtration (TFF) is crucial in antibody drug conjugate (ADC) manufacturing. Ultrafiltration (UF) concentrates the protein product, while diafiltration (DF) exchanges buffer and removes impurities.
- White Paper: ChetoSensar™- Overcoming the Solubility Challenges of Antibody-drug Conjugates
The St. Louis (USA) manufacturing site offers over 35 years of experience in bioconjugation, APIs, excipients, and adjuvants manufacturing. With extensive analytical capabilities, dedicated compliance resources, and innovative manufacturing capabilities, the site assists customers worldwide in accelerating their drug development programs.
- Brochure: Process Development and Drug Manufacturing
We provide comprehensive services for drug development and manufacturing, including technical and regulatory expertise and process development support.
Klucze do silnego partnerstwa ADCPłynny łańcuch dostaw od sekwencji genów do testów stabilności końcowego produktu leczniczego może skrócić czas wprowadzenia na rynek poprzez zminimalizowanie złożoności rozwoju i produkcji.
|
Przepływ pracy
Znalezienie brakującego ogniwa w dostawie ładunku
Wysoce aktywny ładunek użyteczny i środek wiążący lek są dopasowywane do mAb w celu ostatecznej koniugacji w przeciwciało.
Monodyspersyjne i aktywowane PEG lub technologia Chetosensar™ mogą rozwiązać wyzwania związane z rozpuszczalnością podczas odkrywania i opracowywania leków. Zaawansowane półprodukty ładunku użytecznego dla najpopularniejszych klas ładunków użytecznych mogą pomóc w skróceniu czasu rozwoju.

Łączenie punktów z usługami koniugacji
Opracowane składniki linii komórkowej, przeciwciała, ładunku i łącznika łączą się ze sobą podczas koniugacji i/lub biokoniugacji.
Usługi testowania masowych substancji leczniczych (BDS) ADC
BDS, a także końcowy produkt leczniczy przechodzą szeroko zakrojone testy analityczne, w tym testy stabilności i uwalniania.
Koniugacja z cząsteczką cytotoksyczną
Połączenie między przeciwciałem a wysoce aktywnym ładunkiem jest krytycznym elementem ADC, wymagającym szerokiej gamy produktów i chemikaliów.
Chromatografia (opcjonalnie)
Opcjonalny etap chromatograficzny może być wykorzystany do usuwania gatunków o wysokiej masie cząsteczkowej, takich jak agregaty przeciwciał i pozostałości wolnego leku, jednocześnie wspierając optymalizację stosunku lek-przeciwciało (DAR) i kontrolę polidyspersyjności.
Żywica Eshmuno® CMX została zaprojektowana do wysoce selektywnej chromatografii w trybie mieszanym.
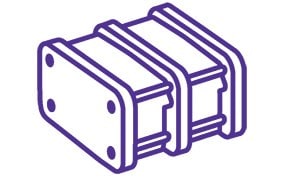
Ultrafiltracja/diafiltracja
Usunięcie pozostałości rozpuszczalnika i wolnego leku po koniugacji jest konieczne przed przygotowaniem końcowej formulacji o pożądanym stężeniu i buforze.
Kapsułka Pellicon® jest pierwszym tego rodzaju - prawdziwym jednorazowym urządzeniem TFF, które jest gotowe do przetwarzania ADC w ciągu kilku minut.
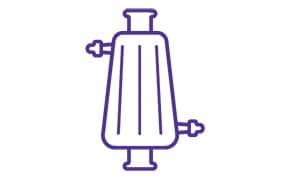
Filtracja sterylna
Filtracja na poziomie sterylizacji podlega coraz intensywniejszej kontroli organów regulacyjnych, które wymagają wysokiego stopnia zapewnienia sterylności.
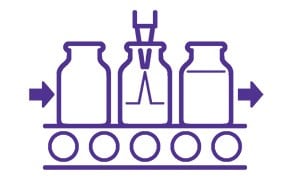
ADC BDS Final Fill and Formulation
BDS jest przygotowywany do ostatecznej i unikalnej formulacji. Preferowana jest liofilizowana postać dawkowania, która zwykle zawiera bufor, stabilizator (np. trehalozę lub sacharozę) i środek powierzchniowo czynny.
Zaloguj się lub utwórz konto, aby kontynuować.
Nie masz konta użytkownika?