Usługi opracowywania i wytwarzania mAb

Akcelerate the Biologic Drug Development Journey
Dzięki Millipore® CTDMO Services zapewniamy dogłębną wiedzę i elastyczne rozwiązania na wszystkich etapach rozwoju i produkcji przeciwciał monoklonalnych, przeciwciał dwuswoistych, białek fuzyjnych lub fragmentów przeciwciał. Współpracujemy z naszymi klientami, aby zrównoważyć ryzyko, zoptymalizować szybkość i wspierać wszystkie aspekty zgodności z przepisami na drodze do wprowadzenia produktu na rynek.
Nasze usługi obejmują rozwój linii komórkowych ssaków i procesów, badania przesiewowe mediów i paszy, bankowanie komórek macierzystych, zwiększanie skali oraz wytwarzanie klinicznych i komercyjnych substancji leczniczych GMP. Ponadto opracowujemy, walidujemy i testujemy metody analityczne we własnym zakresie.
.Nasze osiągnięcia
35+
Lata doświadczenia w rozwoju procesów
25+
Lata doświadczenia w produkcji GMP
10+
Doświadczenie w produkcji elastycznych produktów jednorazowego użytku
85+
Serie GMP zwolnione w ciągu ostatnich 10 lat
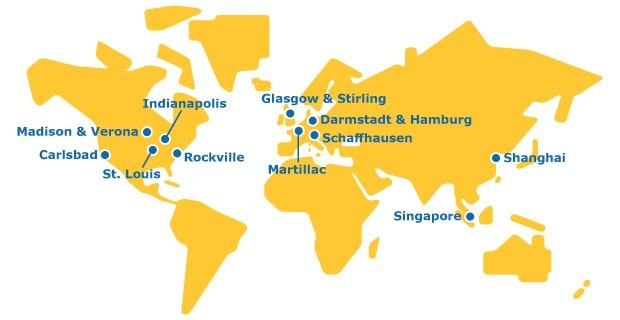
Ślad globalny
Jesteśmy pojedynczą organizacją z globalną siecią dostarczającą usługi CDMO na wszystkich etapach łańcucha wartości cząsteczek.
Silnie połączona sieć CDMO zapewnia szybkość, skalowalność, jakość i elastyczność w zakresie opracowywania i produkcji przeciwciał monoklonalnych, przeciwciał dwuswoistych, białek fuzyjnych i fragmentów przeciwciał.

Nasz zakład w Szanghaju jest domem dla naszego Chińskiego Centrum Testów Biologicznych, w którym mieszczą się zestawy do weryfikacji wirusologicznej. Umożliwia to klientom lokalne przeprowadzanie badań czystości wirusowej od rozwoju przedklinicznego do komercjalizacji w Chinach i na eksport globalny.

Nasz zakład w Martillac został założony w 1987 roku i rozrósł się do w pełni zintegrowanego ośrodka, który oferuje rozwój procesów i produkcję pilotażową do 200 l oraz produkcję kliniczną i komercyjną GMP do 2000 l.
.

Usługi w zakresie testowania bezpieczeństwa biologicznego i produkcji obejmują cykl produktu od wczesnego rozwoju przedklinicznego do licencjonowanej produkcji. Usługi obejmują rozwój analityczny, bankowanie komórek, charakterystykę linii komórkowych, usuwanie wirusów, testowanie uwalniania substancji leczniczych i produktów leczniczych, a także szybkie metody.
Powiązane zasoby dotyczące produktów
- Why Choosing a Client-centric CTDMO is Critical when Outsourcing
This infographic discoveres 5 considerations, that are most critical as indicators of success.
- Trends in Outsourcing the Development and Manufacturing of Biologics
In this whitepaper, we share highlights from a global market research survey of small, midsized and large biopharmaceutical companies on trends related to outsourcing.
- A Molecule’s Journey Break Down Roadblocks to Clinical Success
A guidebook for today’s biopharma executives seeking to navigate through the important considerations necessary to successfully bring a molecule to the clinic.
- Optimize the Formulation for a Monoclonal Antibody
This case study shows, how our innovative, custom solutions and decades of expertise allow to effectively balance cost, speed and risk when optimizing drug substance formulations in an accelerated timeframe.
- Reduce the Level of Host Cell Proteins in the Bioreactor Harvest
Learn how conceptualized and effective approaches help to address process development challenges such as HCP removal, in an accelerated timeframe.
- Scale your Process Directly from 3L to 2000L
In this case study we showcase how to advance a drug candidate into the clinic and ultimately onto the market faster.
- A Molecule’s Journey: Break Down Roadblocks to Commercial Manufacturing Success
A guidebook for today’s biopharma executives outlining key considerations to help ensure commercial manufacturing success.
Zaloguj się lub utwórz konto, aby kontynuować.
Nie masz konta użytkownika?