5.05602
Inhibitor BDK II,(S)-CPP
Synonim(y):
Inhibitor kinazy BCKD II, inhibitor kinazy dehydrogenazy α-ketokwasów rozgałęzionych II, kwas(S)-α-chloro-fenylopropionowy, Kwas(S)-α-chloro-fenylopropionowy, inhibitor kinazy BCKD II, inhibitor kinazy dehydrogenazy α-ketokwasów o rozgałęzionym łańcuchu II
About This Item
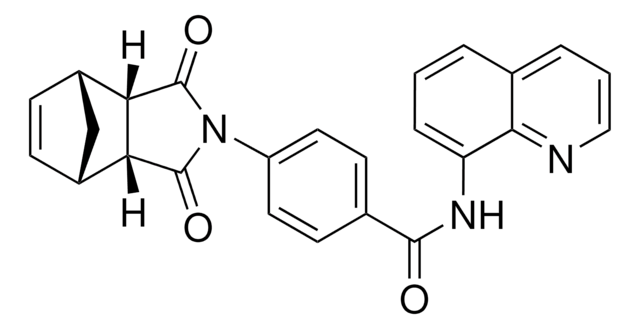
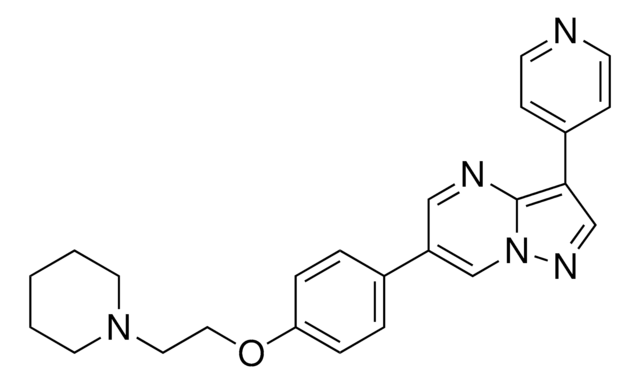
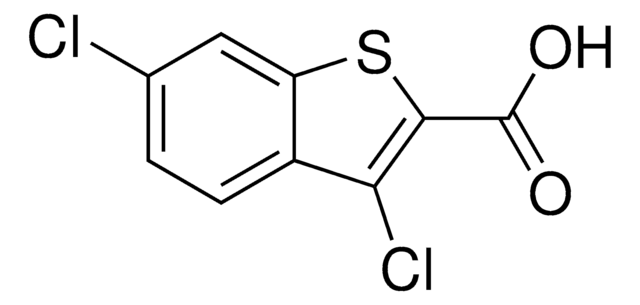
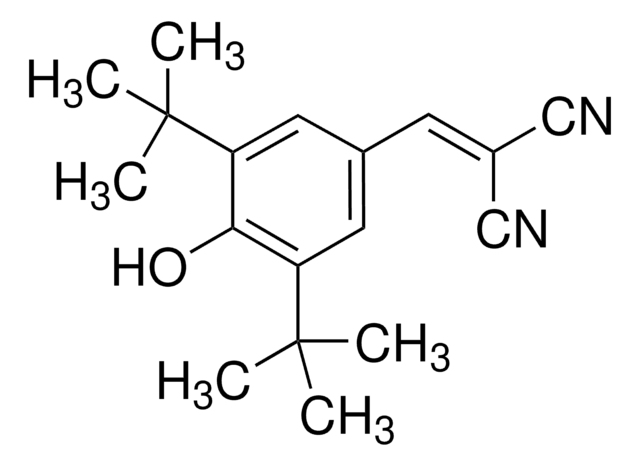
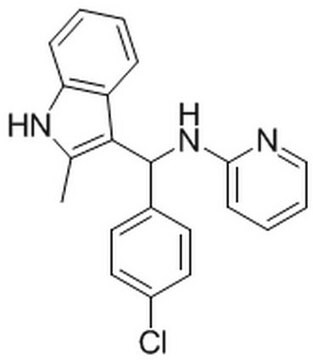
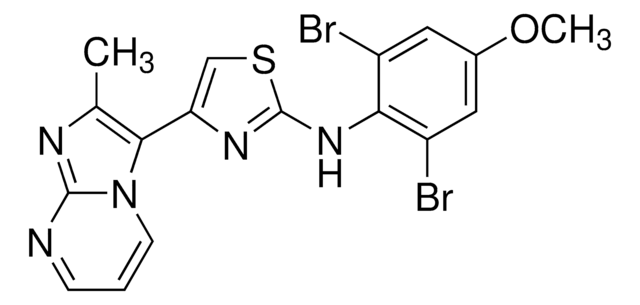
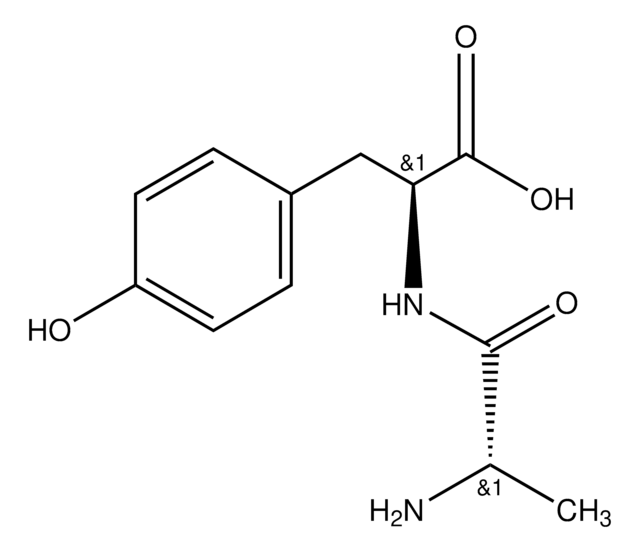
Polecane produkty
Próba
≥98% (HPLC)
Poziom jakości
Formularz
oil
producent / nazwa handlowa
Calbiochem®
warunki przechowywania
OK to freeze
desiccated
protect from light
kolor
clear colorless
rozpuszczalność
DMSO: 100 mg/mL
temp. przechowywania
−20°C
ciąg SMILES
Cl[C@@H](Cc1ccccc1)C(=O)O
InChI
1S/C9H9ClO2/c10-8(9(11)12)6-7-4-2-1-3-5-7/h1-5,8H,6H2,(H,11,12)/t8-/m0/s1
Klucz InChI
LIDRHDRWTSPELB-QMMMGPOBSA-N
Opis ogólny
Działania biochem./fizjol.
BDK
Opakowanie
Ostrzeżenie
Rekonstytucja
Inne uwagi
Informacje prawne
Kod klasy składowania
11 - Combustible Solids
Klasa zagrożenia wodnego (WGK)
WGK 3
Temperatura zapłonu (°F)
Not applicable
Temperatura zapłonu (°C)
Not applicable
Certyfikaty analizy (CoA)
Poszukaj Certyfikaty analizy (CoA), wpisując numer partii/serii produktów. Numery serii i partii można znaleźć na etykiecie produktu po słowach „seria” lub „partia”.
Masz już ten produkt?
Dokumenty związane z niedawno zakupionymi produktami zostały zamieszczone w Bibliotece dokumentów.
Nasz zespół naukowców ma doświadczenie we wszystkich obszarach badań, w tym w naukach przyrodniczych, materiałoznawstwie, syntezie chemicznej, chromatografii, analityce i wielu innych dziedzinach.
Skontaktuj się z zespołem ds. pomocy technicznej