108975
Leupeptyna, Hemisiarczan, Drobnoustroje
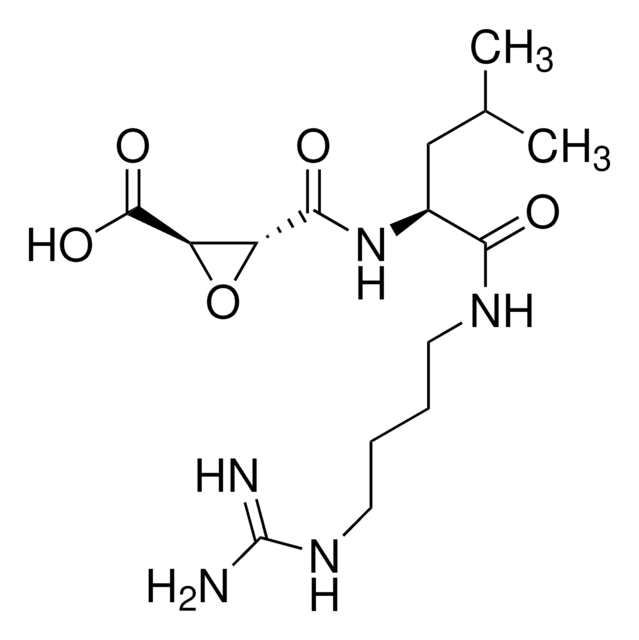
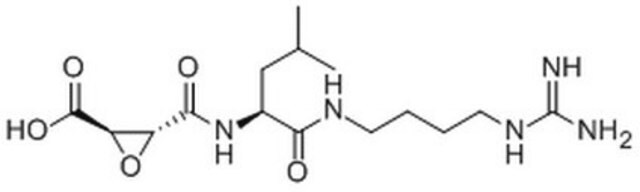
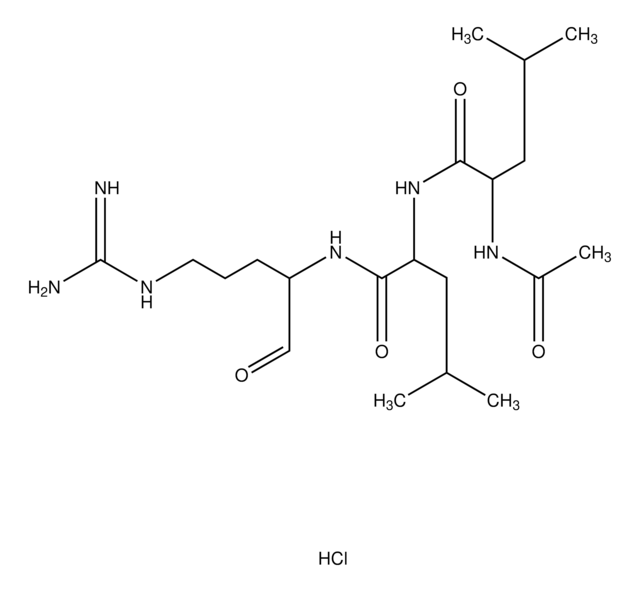
Leupeptin hemisulfate, CAS 103476-89-7, is a reversible inhibitor of trypsin-like proteases and cysteine proteases
Synonim(y):
Ac-LLR-CHO, ½H₂SO₄
About This Item
Polecane produkty
Poziom jakości
opis
Merck USA index - 14, 5456
Próba
≥90% (HPLC)
Formularz
lyophilized solid
producent / nazwa handlowa
Calbiochem®
warunki przechowywania
OK to freeze
desiccated (hygroscopic)
kolor
white
rozpuszczalność
water: 50 mg/mL
Warunki transportu
ambient
temp. przechowywania
−20°C
ciąg SMILES
[N+H](=C(N)N)CCC[C@H](NC(=O)[C@@H](NC(=O)[C@@H](NC(=O)C)CC(C)C)CC(C)C)C=O
InChI
1S/C20H38N6O4/c1-12(2)9-16(24-14(5)28)19(30)26-17(10-13(3)4)18(29)25-15(11-27)7-6-8-23-20(21)22/h11-13,15-17H,6-10H2,1-5H3,(H,24,28)(H,25,29)(H,26,30)(H4,21,22,23)/p+1/t15-,16-,17-/m0/s1
Klucz InChI
GDBQQVLCIARPGH-ULQDDVLXSA-O
Opis ogólny
Działania biochem./fizjol.
trypsin- and cysteine-like proteases
Ostrzeżenie
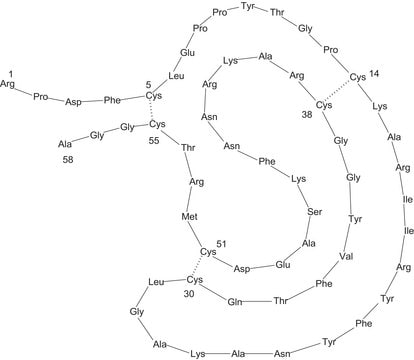
Sekwencja
Rekonstytucja
Inne uwagi
Sarin, A., et al. 1994. J. Immunol.153, 862.
Informacje prawne
Kod klasy składowania
11 - Combustible Solids
Klasa zagrożenia wodnego (WGK)
WGK 3
Temperatura zapłonu (°F)
Not applicable
Temperatura zapłonu (°C)
Not applicable
Certyfikaty analizy (CoA)
Poszukaj Certyfikaty analizy (CoA), wpisując numer partii/serii produktów. Numery serii i partii można znaleźć na etykiecie produktu po słowach „seria” lub „partia”.
Masz już ten produkt?
Dokumenty związane z niedawno zakupionymi produktami zostały zamieszczone w Bibliotece dokumentów.
Klienci oglądali również te produkty
Nasz zespół naukowców ma doświadczenie we wszystkich obszarach badań, w tym w naukach przyrodniczych, materiałoznawstwie, syntezie chemicznej, chromatografii, analityce i wielu innych dziedzinach.
Skontaktuj się z zespołem ds. pomocy technicznej