Wszystkie zdjęcia(1)
Kluczowe dokumenty
927821
EBX2-alkyne
≥95%
Synonim(y):
5-Methyl-1-((trimethylsilyl)ethynyl)-1l3-benzo[d][1,2]iodaoxol-3(1H)-one
Zaloguj sięWyświetlanie cen organizacyjnych i kontraktowych
About This Item
Wzór empiryczny (zapis Hilla):
C13H15IO2Si
Numer CAS:
Masa cząsteczkowa:
358.25
Numer MDL:
Kod UNSPSC:
12352101
NACRES:
NA.22
Polecane produkty
Poziom jakości
Próba
≥95%
Formularz
powder
temp. przechowywania
−20°C
ciąg SMILES
CC1=CC(C(OI2C#C[Si](C)(C)C)=O)=C2C=C1
InChI
1S/C13H15IO2Si/c1-10-5-6-12-11(9-10)13(15)16-14(12)7-8-17(2,3)4/h5-6,9H,1-4H3
Zastosowanie
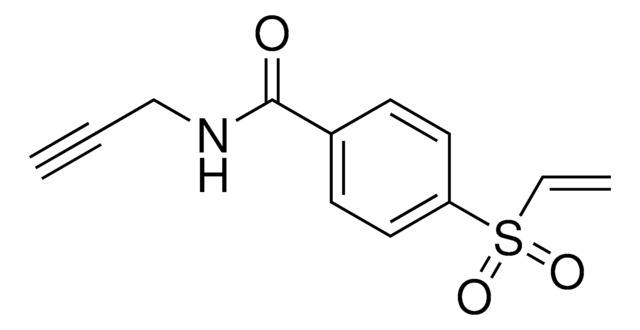
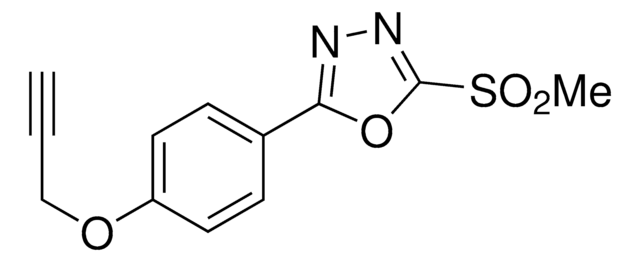
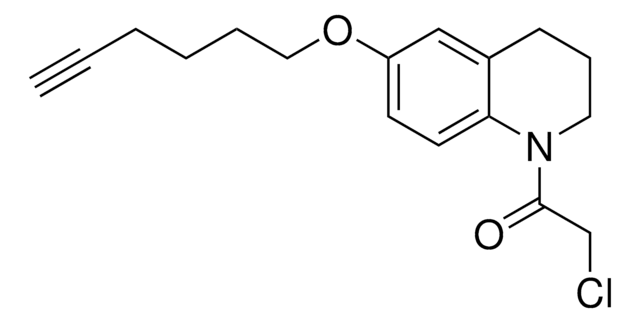
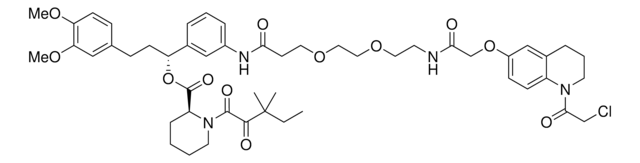
EBX2-alkyne is a hypervalent iodine reagent used for labeling cysteines. A method was developed using cysteine-reactive compounds including this one to allow for unbiased analysis of proteomic data in quantitative applications . The method uses light or heavy labeling with the isotopically labelled desthiobiotin azide (isoDTB) tag for mass spectrometry analysis . Analysis then uses the isotopic tandem orthogonal proteolysis activity-based protein profiling (isoTOP-ABPP) workflow .
Ta strona może zawierać tekst przetłumaczony maszynowo.
Kod klasy składowania
11 - Combustible Solids
Klasa zagrożenia wodnego (WGK)
WGK 3
Temperatura zapłonu (°F)
Not applicable
Temperatura zapłonu (°C)
Not applicable
Wybierz jedną z najnowszych wersji:
Certyfikaty analizy (CoA)
Lot/Batch Number
Przepraszamy, ale COA dla tego produktu nie jest aktualnie dostępny online.
Proszę o kontakt, jeśli potrzebna jest pomoc Obsługa Klienta
Masz już ten produkt?
Dokumenty związane z niedawno zakupionymi produktami zostały zamieszczone w Bibliotece dokumentów.
Profiling the proteome-wide selectivity of diverse electrophiles.
Zanon P R A, et al.
ChemRxiv : the preprint server for chemistry (2021)
Eranthie Weerapana et al.
Nature, 468(7325), 790-795 (2010-11-19)
Cysteine is the most intrinsically nucleophilic amino acid in proteins, where its reactivity is tuned to perform diverse biochemical functions. The absence of a consensus sequence that defines functional cysteines in proteins has hindered their discovery and characterization. Here we
Patrick R A Zanon et al.
Angewandte Chemie (International ed. in English), 59(7), 2829-2836 (2019-11-30)
Rapid development of bacterial resistance has led to an urgent need to find new druggable targets for antibiotics. In this context, residue-specific chemoproteomic approaches enable proteome-wide identification of binding sites for covalent inhibitors. Described here are easily synthesized isotopically labeled
Eranthie Weerapana et al.
Nature, 468(7325), 790-795 (2010-11-19)
Cysteine is the most intrinsically nucleophilic amino acid in proteins, where its reactivity is tuned to perform diverse biochemical functions. The absence of a consensus sequence that defines functional cysteines in proteins has hindered their discovery and characterization. Here we
Nasz zespół naukowców ma doświadczenie we wszystkich obszarach badań, w tym w naukach przyrodniczych, materiałoznawstwie, syntezie chemicznej, chromatografii, analityce i wielu innych dziedzinach.
Skontaktuj się z zespołem ds. pomocy technicznej