おすすめの製品
product name
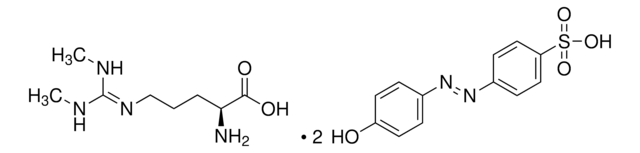
L-ホモアルギニン 塩酸塩, unnatural arginine analog
アッセイ
≥98% (TLC)
形状
powder
色
white to off-white
mp
213-215 °C (lit.)
溶解性
H2O: soluble
アプリケーション
peptide synthesis
SMILES記法
Cl[H].N[C@@H](CCCCNC(N)=N)C(O)=O
InChI
1S/C7H16N4O2.ClH/c8-5(6(12)13)3-1-2-4-11-7(9)10;/h5H,1-4,8H2,(H,12,13)(H4,9,10,11);1H/t5-;/m0./s1
InChI Key
YMKBVNVCKUYUDM-JEDNCBNOSA-N
類似した製品をお探しですか? 訪問 製品比較ガイド
アプリケーション
L-Homoarginine may be used to create non-natural proteins for studies of post-translational protein modifications. Arginine residues are often located at the active centers of proteins and enzymes. Replacing these arginines with homoarginine can elucidate protein function and structural requirements. L-Homoarginine is used to study the mechanisms of nitric oxide production by cells via nitric oxide synthase(s). L-Homoarginine is used as a selective mammalian alkaline phosphatase isoenzyme inhibitor. The substitution of homoarginine for arginine or lysine renders proteins resistant to proteolysis by trypsin.
アルギニンまたはリジンをホモアルギニンに置換することで、タンパク質はトリプシンのタンパク質分解に対して耐性を持ちます。アルギニン残基は、タンパク質および酵素の活性中心によく見られます。これらのアルギニンをホモアルギニンと置換することで、タンパク質機能および構造条件の解明が可能になります。
生物化学的/生理学的作用
ホモアルギニンは、組織非特異的アルカリホスファタ-ゼ(TNALP)の阻害剤です。また、ナトリウム非依存性の高親和性y+トランスポ-タ-によるアルギニンの細胞内輸送の阻害剤でもあります。
保管分類コード
11 - Combustible Solids
WGK
WGK 3
引火点(°F)
Not applicable
引火点(℃)
Not applicable
個人用保護具 (PPE)
Eyeshields, Gloves, type N95 (US)
適用法令
試験研究用途を考慮した関連法令を主に挙げております。化学物質以外については、一部の情報のみ提供しています。 製品を安全かつ合法的に使用することは、使用者の義務です。最新情報により修正される場合があります。WEBの反映には時間を要することがあるため、適宜SDSをご参照ください。
Jan Code
H1007-BULK:
H1007-250MG:
H1007-VAR:
H1007-5G:
H1007-1G:
試験成績書(COA)
製品のロット番号・バッチ番号を入力して、試験成績書(COA) を検索できます。ロット番号・バッチ番号は、製品ラベルに「Lot」または「Batch」に続いて記載されています。
この製品を見ている人はこちらもチェック
Roman N Rodionov et al.
Journal of the American Heart Association, 8(14), e012486-e012486 (2019-07-16)
Background Homoarginine ( hA rg) has been shown to be cardioprotective in a model of ischemic heart failure; however, the mechanism remains unknown. hA rg can inhibit tissue-nonspecific alkaline phosphatase ( TNAP ), an enzyme that promotes vascular calcification. We
J Fernandes et al.
Brazilian journal of medical and biological research = Revista brasileira de pesquisas medicas e biologicas, 41(1), 41-46 (2007-12-22)
Our objective was to characterize the modulation of the activity of Saccharomyces cerevisiae alkaline phosphatases (ALPs) by classic inhibitors of ALP activity, cholesterol and steroid hormones, in order to identify catalytic similarities between yeast and mammalian ALPs. S. cerevisiae expresses
Gabor Tajti et al.
Allergy, asthma, and clinical immunology : official journal of the Canadian Society of Allergy and Clinical Immunology, 14, 2-2 (2018-01-09)
Contribution of nitric-oxide (NO) pathway to the pathogenesis of bronchial asthma (asthma) is ambiguous as NO may confer both protective and detrimental effects depending on the NO synthase (NOS) isoforms, tissue compartments and underlying pathological conditions (e.g. systemic inflammation). Asymmetric
Robert N. Atkinson et al.
The Journal of organic chemistry, 64(10), 3467-3475 (2001-10-25)
Using the catalytic asymmetric Sharpless carbamate aminohydroxylation, conformationally restricted L-arginine and L-homoarginine derivatives (5-8) were prepared in good enantiomeric excess to investigate the binding requirements of L-arginine-based compounds with nitric oxide synthase. The L-arginine derivatives (5 and 6) inhibited both
Akiya Akahoshi et al.
Biochemical and biophysical research communications, 414(3), 625-630 (2011-10-18)
Arginine analogs were incorporated site-specifically into proteins using an in vitro translation system. In this system, mRNAs containing a CGGG codon were translated by an aminoacyl-tRNA(CCCG), which was charged with arginine analogs using yeast arginyl-tRNA synthetase. N(G)-monomethyl-L-arginine, L-citrulline and L-homoarginine
ライフサイエンス、有機合成、材料科学、クロマトグラフィー、分析など、あらゆる分野の研究に経験のあるメンバーがおります。.
製品に関するお問い合わせはこちら(テクニカルサービス)