G1549
PNGase F Elizabethkingia meningoseptica由来
ready-to-use solution, recombinant, expressed in E. coli
別名:
N-グリコシダーゼF, PNGase F Chryseobacterium meningosepticum由来, PNGase F Flavobacterium meningosepticum由来, ペプチドN-グリコシダーゼ
ログイン組織・契約価格を表示する
すべての画像(1)
About This Item
CAS番号:
MDL番号:
UNSPSCコード:
12352204
NACRES:
NA.54
おすすめの製品
リコンビナント
expressed in E. coli
品質水準
結合体
(N-linked)
グレード
Proteomics Grade
フォーム
ready-to-use solution
比活性
≥1000 U/mg
シェルフライフ
≥1 yr at -20 °C
分子量
~36 kDa
輸送温度
wet ice
保管温度
−20°C
類似した製品をお探しですか? 訪問 製品比較ガイド
関連するカテゴリー
アプリケーション
Recombinant PNGase F has been purified by affinity chromatography and dialyzed into a 50% glycerol solution with 10 mM potassium phoosphate pH 7.5 to produce a stable product. The product contains low levels of buffer salts. This highly purified material can be used for preparative deglycosylation or for analytical applications in gel, in solution, or on blot membranes. The enzyme can be removed from preparative operations by utilizing its C-terminal 6x histidine fusion tag. PNGase F from Elizabethkingia meningoseptica has been used in deglycosylation assay in human plasma samples and in deglycosylation of chondroitin sulfate proteoglycan.
タンパク質の脱グリコシル化に使用できます。
生物化学的/生理学的作用
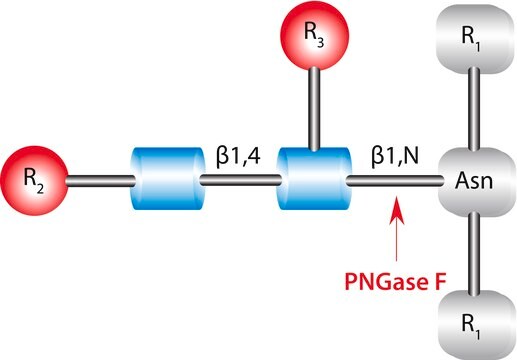
PNGase F from Elizabethkingia meningoseptica has glycan-binding catalytic domain and a bowl-like domain at the N-terminus. It cleaves an entire glycan from a glycoprotein provided the glycosylated asparagine moiety is substituted on its amino and carboxyl terminus with a polypeptide chain. It is cost-effectively produced on a large scale in prokaryotic hosts and requires divalent zinc ions for its enzymatic activity.
グリコシル化されたアスパラギン残基のN末端とC末端がポリペプチド鎖で置換されているとき、糖タンパク質からグリカン全体を切断します。
単位の定義
One unit will catalyze the release of N-linked oligosaccharides from 1 nanomole of denatured ribonuclease B in one minute at 37°C at pH 7.5 monitored by SDS-PAGE. One Sigma unit of PNGase F activity is equal to 1 IUB milliunit.
物理的形状
Supplied as 300 Units/mL enzyme in 50% (v/v) glycerol and 50% (v/v) 20 mM Potassium Phosphate, pH 7.5.
保管分類コード
10 - Combustible liquids
WGK
WGK 1
引火点(°F)
Not applicable
引火点(℃)
Not applicable
適用法令
試験研究用途を考慮した関連法令を主に挙げております。化学物質以外については、一部の情報のみ提供しています。 製品を安全かつ合法的に使用することは、使用者の義務です。最新情報により修正される場合があります。WEBの反映には時間を要することがあるため、適宜SDSをご参照ください。
Jan Code
G1549-300UN-PW:
G1549PROC:
G1549-PH:
G1549-50UN:
G1549-50UN-PW:
G1549-BULK:
G1549-VAR:
G1549-300UN:
この製品を見ている人はこちらもチェック
N-glycosylation of apolipoprotein A1 in cardiovascular diseases
Majek P, et al.
Translational Research, 165(2), 360-362 (2015)
Characterization and analysis of extracellular matrix in malignant brain tumors and their cellular derivatives
Extracellular Matrix, 113-138 (2015)
Discovery and characterization of a novel extremely acidic bacterial N-glycanase with combined advantages of PNGase F and A
Wang T, et al.
Bioscience Reports, 34(6), e00149-e00149 (2014)
Identification and characterization of a novel prokaryotic peptide: N-glycosidase from Elizabethkingia meningoseptica
Sun G, et al.
The Journal of Biological Chemistry, jbc-M114 (2015)
T H Plummer et al.
The Journal of biological chemistry, 259(17), 10700-10704 (1984-09-10)
Endo-beta-N-acetylglucosaminidase F preparations from Flavobacterium meningosepticum have been found to contain peptide:N-glycosidase activity. Only the second activity, designated as peptide:N-glycosidase F, readily cleaves the beta-aspartylglycosylamine linkage of a fetuin triantennary complex glycopeptide, as shown by the isolation of the corresponding
ライフサイエンス、有機合成、材料科学、クロマトグラフィー、分析など、あらゆる分野の研究に経験のあるメンバーがおります。.
製品に関するお問い合わせはこちら(テクニカルサービス)