C1057
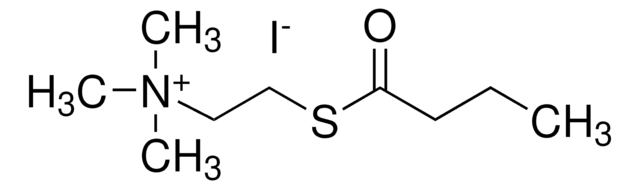
Butirrilcolinesterasi
lyophilized powder, ≥900 units/mg protein
Sinonimo/i:
Acilcolina acil-idrolasi, Colin esterasi, butirril, Pseudocolinesterasi
Autenticatiper visualizzare i prezzi riservati alla tua organizzazione & contrattuali
About This Item
Prodotti consigliati
Stato
lyophilized powder
Livello qualitativo
Attività specifica
≥900 units/mg protein
PM
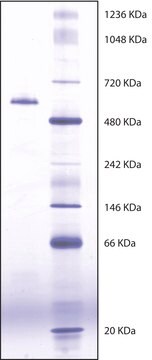
tetramer 440 kDa
Composizione
Protein, ≥10%
Solubilità
H2O: soluble 10 mg/mL
applicazioni
diagnostic assay manufacturing
Temperatura di conservazione
−20°C
Cerchi prodotti simili? Visita Guida al confronto tra prodotti
Applicazioni
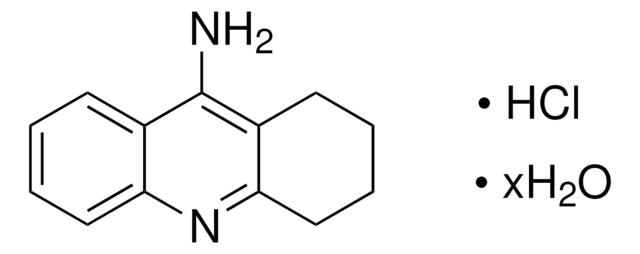
L′inibizione selettiva dell′attività della BChE può essere utilizzata nel rilevamento degli organofosfati. È stato esplorato il suo impiego nel trattamento della tossicità degli organofosfati. È stato riferito che il livello di BChE nel sangue umano è correlato al grado di protezione contro gli agenti nervini potenzialmente tossici. Le colinesterasi sono state studiate anche in relazione al loro ruolo nella malattia di Alzheimer.
Azioni biochim/fisiol
La butirilcolinesterasi (BChE) è una serina idrolasi strutturalmente simile all′acetilcolinesterasi (AChE), ma differisce per specificità del substrato e sensibilità dell′inibitore. A differenza dell′AChE, la BChE riesce a idrolizzare efficientemente grandi esteri di colina, come la butirilcolina e la benzoilcolina. L′enzima è una glicoproteina tetramerica con quattro subunità uguali (110 kDa ciascuna). L′enzima è attivato da Ca2+ e Mg2+. L′attività è costante entro il range pH di 6,0-8,0. È inibito da betaina, nicotina, organofosfati e carbammato.
Definizione di unità
Un′unità idrolizza 1,0 μmole di butirilcolina a colina e butirrato in un minuto a pH 8,0 e a 37 °C. L′attività ottenuta utilizzando la butirilcolina come substrato è superiore di circa 2,5 volte quella ottenuta con l′acetilcolina.
Stato fisico
Altamente purificata; contiene sali tampone
Risultati analitici
Proteina determinata da biureto
Inibitore
N° Catalogo
Descrizione
Determinazione del prezzo
Avvertenze
Danger
Indicazioni di pericolo
Consigli di prudenza
Classi di pericolo
Resp. Sens. 1
Codice della classe di stoccaggio
11 - Combustible Solids
Classe di pericolosità dell'acqua (WGK)
WGK 3
Punto d’infiammabilità (°F)
Not applicable
Punto d’infiammabilità (°C)
Not applicable
Dispositivi di protezione individuale
Eyeshields, Gloves, type N95 (US)
Scegli una delle versioni più recenti:
Possiedi già questo prodotto?
I documenti relativi ai prodotti acquistati recentemente sono disponibili nell’Archivio dei documenti.
I clienti hanno visto anche
Tarek Mohamed et al.
Bioorganic & medicinal chemistry letters, 20(12), 3606-3609 (2010-05-18)
A group of 2,4-disubstituted pyrimidine derivatives (7a-e, 8a-e and 9a-d) that possess a variety of C-2 aliphatic five- and six-membered heterocycloalkyl ring in conjunction with a C-4 arylalkylamino substituent were designed, synthesized and evaluated as cholinesterase (ChE) inhibitors. The steric
Keriman Ozadali-Sari et al.
Bioorganic chemistry, 72, 208-214 (2017-05-10)
The present study describes the synthesis, pharmacological evaluation (BChE/AChE inhibition, Aβ antiaggregation, and neuroprotective effects), and molecular modeling studies of novel 2-[4-(4-substitutedpiperazin-1-yl)phenyl]benzimidazole derivatives. The alkyl-substituted derivatives exhibited selective inhibition on BChE with varying efficiency. Compounds 3b and 3d were found
Jianhua Liu et al.
The Journal of clinical endocrinology and metabolism, 93(5), 1980-1987 (2008-03-20)
Ghrelin, an acylated peptide hormone secreted from the gut, regulates appetite and metabolism. Elucidating its pattern of secretion in the fed and fasted states is important in the face of the obesity epidemic. Our objective was to examine changes in
R M Blong et al.
The Biochemical journal, 327 ( Pt 3), 747-757 (1998-05-15)
Butyrylcholinesterase (BChE) in human serum consists predominantly of tetramers. Recombinant BChE, however, expressed in Chinese hamster ovary (CHO) cells, consists of approx. 55% dimers, 10-30% tetramers and 15-40% monomers. To determine the origin of the monomer species we added the
Determination of butyrylcholinesterase inhibition using ion transfer across the interface between two immiscible liquids
Beattie PD, et al.
Analytical Chemistry, 66(1), 52-57 (1994)
Il team dei nostri ricercatori vanta grande esperienza in tutte le aree della ricerca quali Life Science, scienza dei materiali, sintesi chimica, cromatografia, discipline analitiche, ecc..
Contatta l'Assistenza Tecnica.