T3754
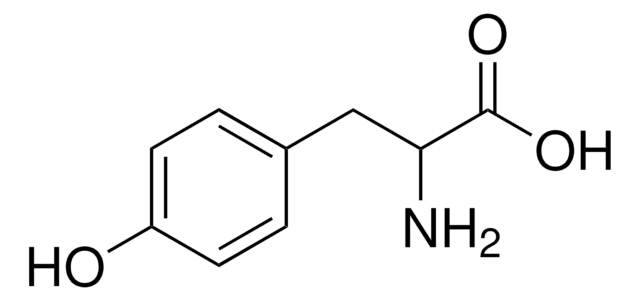
L-Tyrosine
≥98% (HPLC)
Sinônimo(s):
(S)-2-Amino-3-(4-hydroxyphenyl)propionic acid, 3-(4-Hydroxyphenyl)-L-alanine
About This Item
Produtos recomendados
product name
L-Tyrosine, reagent grade, ≥98% (HPLC)
grau
reagent grade
Nível de qualidade
Ensaio
≥98% (HPLC)
forma
powder
cor
white to off-white
pf
>300 °C (dec.) (lit.)
solubilidade
1 M HCl: soluble 50 mg/mL
aplicação(ões)
detection
cadeia de caracteres SMILES
N[C@@H](Cc1ccc(O)cc1)C(O)=O
InChI
1S/C9H11NO3/c10-8(9(12)13)5-6-1-3-7(11)4-2-6/h1-4,8,11H,5,10H2,(H,12,13)/t8-/m0/s1
chave InChI
OUYCCCASQSFEME-QMMMGPOBSA-N
Procurando produtos similares? Visita Guia de comparação de produtos
Aplicação
Ações bioquímicas/fisiológicas
Outras notas
Código de classe de armazenamento
11 - Combustible Solids
Classe de risco de água (WGK)
WGK 1
Ponto de fulgor (°F)
Not applicable
Ponto de fulgor (°C)
Not applicable
Equipamento de proteção individual
dust mask type N95 (US), Eyeshields, Gloves
Escolha uma das versões mais recentes:
Certificados de análise (COA)
Não está vendo a versão correta?
Se precisar de uma versão específica, você pode procurar um certificado específico pelo número do lote ou da remessa.
Já possui este produto?
Encontre a documentação dos produtos que você adquiriu recentemente na biblioteca de documentos.
Os clientes também visualizaram
Artigos
Proteinase K (EC 3.4.21.64) activity can be measured spectrophotometrically using hemoglobin as the substrate. Proteinase K hydrolyzes hemoglobin denatured with urea, and liberates Folin-postive amino acids and peptides. One unit will hydrolyze hemoglobin to produce color equivalent to 1.0 μmol of tyrosine per minute at pH 7.5 at 37 °C (color by Folin & Ciocalteu's Phenol Reagent).
Protocolos
Proteinase K (EC 3.4.21.64) activity can be measured spectrophotometrically using hemoglobin as the substrate. Proteinase K hydrolyzes hemoglobin denatured with urea, and liberates Folin-postive amino acids and peptides. One unit will hydrolyze hemoglobin to produce color equivalent to 1.0 μmol of tyrosine per minute at pH 7.5 at 37 °C (color by Folin & Ciocalteu's Phenol Reagent).
To standardize a procedure for the enzymatic assay of Protease using Casein as a substrate at Sigma-Aldrich St. Louis.
Nossa equipe de cientistas tem experiência em todas as áreas de pesquisa, incluindo Life Sciences, ciência de materiais, síntese química, cromatografia, química analítica e muitas outras.
Entre em contato com a assistência técnica