Boroniany MIDA
Wprowadzenie
Reakcja sprzęgania krzyżowego Suzuki-Miyaura kwasów boronowych jest jedną z najważniejszych i najczęściej wykorzystywanych reakcji w zestawie narzędzi chemii organicznej, z zastosowaniami w nauce o polimerach, a także w przemyśle chemicznym i farmaceutycznym. Jednak wiele kwasów boronowych jest wyjątkowo niestabilnych i podatnych na rozkład, co czyni je nieefektywnymi w reakcjach sprzęgania lub utrudnia ich długotrwałe przechowywanie. Ponadto, nie opracowano metody iteracyjnego sprzęgania krzyżowego Suzuki Miyaura w łagodnych warunkach. Niedawno profesor Martin Burke z Uniwersytetu Illinois w Urbana-Champaign opracował metodę osłabiania transmetalacji między kwasami boronowymi a gatunkami palladu poprzez rehybrydyzację centrum boronowego ze sp2 do sp3 poprzez kompleksowanie z trójwartościowym ligandem kwasu N-metyloiminodioctowego (MIDA). Pozwoliło to na przeprowadzenie sekwencyjnych reakcji Suzuki-Miyaura w łagodnych warunkach.

MIDA M51008
Ochronione przez MIDA estry boronianowe są łatwe w obsłudze, bezterminowo stabilne w powietrzu, kompatybilne z chromatografią i niereaktywne w standardowych warunkach bezwodnego sprzęgania krzyżowego, nawet w temperaturach do 80 °C. Jednakże, deprotekcję można łatwo osiągnąć w temperaturze pokojowej w łagodnych wodnych warunkach zasadowych przy użyciu 1M NaOH lub nawet NaHCO3.
Odniesienia: Gillis, E. P.; Burke, M. D. J. Am. Chem. Soc. 2007, 129, 6716.
Wyświetl pełną listę boronianów MIDA z Sigma-Aldrich®.
Reprezentatywne aplikacje
MIDA jako grupa ochronna i iteracyjne sprzęganie krzyżowe
Aby zademonstrować skuteczność MIDA jako grupy ochronnej, grupa Burke'a przereagowała mieszaninę 1:1 mieszaniny boronianu MIDA (698229) i kwasu 4-butylofenyloboronowego z 4-bromobenzaldehydem w bezwodnych warunkach Suzuki-Miyaura Buchwalda (Schemat 1). Otrzymana mieszanina produktów wykazywała preferencję 24:1 dla reakcji z niezabezpieczonym kwasem boronowym. I odwrotnie, gdy przeprowadzono reakcję kontrolną z mieszaniną kwasu 4-n-butylofenyloboronowego i albo niezabezpieczonego kwasu boronowego (393622) lub adduktu N-metylodietanoloaminy, nie zaobserwowano selektywności.

Scheme 1
Potencjał iteracyjnych sprzężeń krzyżowych z wykorzystaniem metodologii Burke'a został zademonstrowany w ich całkowitej syntezie ratanhiny (Schemat 2).Kwas trans-1-propen-1-yloboronowy został sprzężony z boronianem benzofuranylu MIDA 1.który deprotekcjonowano i sprzęgano krzyżowo z nieporęcznym bromkiem arylowym boronianu MIDA 2 w podwyższonej temperaturze. Kolejny związek pośredni został usunięty, sprzężony z bromkiem winylu 3, aby otrzymać eter diMOM, a rozszczepienie dwóch grup MOM dało w rezultacie ratanhinę. Ułatwiające cechy tego typu syntezy obejmują wykorzystanie tylko jednej, łagodnej reakcji do złożenia zbioru łatwo syntetyzowanych, łatwo oczyszczanych i wysoce wytrzymałych bloków budulcowych. Co więcej, krótki i modułowy charakter tej ścieżki umożliwia łatwe przygotowanie analogów po prostu poprzez zastąpienie zmodyfikowanych bloków budulcowych w tej samej iteracyjnej sekwencji sprzęgania krzyżowego.

Scheme 2.
Boroniany MIDA polienów
Zwykle kwasy polieniloboronowe są bardzo niestabilne i dlatego nie są stosowane w syntezie. W innej przykładowej demonstracji stabilności i wydajności boronianów MIDA w iteracyjnym sprzęganiu krzyżowym, Burke i współpracownicy wykorzystali powszechny alkenylowy boronian MIDA (703478) do stworzenia serii polienowych bloków budulcowych. Końcówka boronianu MIDA jest obojętna na sprzężenia Hecka, Stille'a i Suzuki, dając boroniany MIDA butadienylu (Schemat 3).

Scheme 3
Boronian alkenylowy MIDA 703478 został również zastosowany do syntezy karotenoidu all-trans-retinalu. Demonstrując wykonalność polienylowych boronianów MIDA w syntezie, B-deprotekcja intermediatu 4 przebiegła gładko, generując kwas boronowy, który następnie został sprzężony z β-bromo enalem w celu dostarczenia all-trans-retinalu (Schemat 4).

Scheme 4
Jeszcze bardziej imponujące są borylacje Miyaura, sprzężenia Sonogashira i Negishi, które dają bis-metalizowane odczynniki typu lynchpin (Schemat 5). Odczynniki 5 i 6 były dalej rozwijane w syntezach polienowych produktów naturalnych kwasu β-parinarynowego (Schemat 6) i łańcucha polienowego amfoterycyny B poprzez stabilny polienowy blok budulcowy 7 (Schemat 7).

Scheme 5

Scheme 6

Scheme 7
Tworzenie złożonych kwasów boronowych z boronianów MIDA
Kolejną niezwykle użyteczną cechą boronianów MIDA jest ich kompatybilność z szeroką gamą popularnych odczynników syntetycznych, co pozwala na opracowanie sfunkcjonalizowanych boronianów MIDA w celu stworzenia strukturalnie złożonych surogatów kwasu boronowego. Zostało to niedawno zademonstrowane przez Burke'a i współpracowników poprzez transformację boronianu 4-(hydroksymetylo)fenylu MIDA (698105) przez różne powszechne utleniacze i odczynniki w celu utworzenia szeregu syntetycznie użytecznych boronianów MIDA (Schemat 8). Nawet ostre odczynniki, takie jak kwas triflicowy i utlenianie Jonesa, były dobrze tolerowane, utrzymując boronian MIDA w stanie nienaruszonym. W kilku przypadkach transformacje można łatwo odwrócić, uzyskując oryginalny boronian 4-(hydroksymetylo)fenylu MIDA.

Scheme 8
Boronian 4-formylofenylu MIDA 697494 został dalej opracowany w różnych reakcjach tworzenia wiązań C-C. Wyniki pokazują, że boroniany MIDA są również kompatybilne z protokołami aminowania redukcyjnego, aldolowania Evansa, olefinowania Hornera-Wadswortha-Emmonsa i olefinowania Takai (Schemat 9).

Scheme 9
Wpływ wyjątkowej kompatybilności boronianu MIDA wykazano w całkowitej syntezie (+)-rokacyny C z akroleinowego boronianu MIDA (Schemat 10). Boronian MIDA tolerował aldol Patersona i diastereoselektywny protokół redukcji, dając diolowy boronian MIDA, który oczyszczono za pomocą chromatografii żelu krzemionkowego. Oczyszczony boronian MIDA był permetylowany solą Meerweina, deprotekcjonowany CAN, utleniany periodynanem Dess-Martina i poddawany olefinacji Takai z otrzymaniem stabilnego, krystalicznego, kompleksowego boronianu MIDA 8. Sprzęganie Stille'a 8 ze znanym blokiem budulcowym 9, a następnie uwalnianie kwasu boronowego in situ i krzyżowe sprzęganie z bromobenzenem dostarcza (+)-rokacyny C.

Scheme 10
Otrzymywanie boronianu trans-(2-bromowinylu) MIDA i boronianu winylu MIDA z odpowiednich silanów
Z powodu niestabilności niektórych kwasów boronowych, grupa Burke'a opracowała bardzo praktyczne syntezy bardziej wrażliwych bloków budulcowych. Na przykład, podczas gdy trans-(2-bromowinylo) boronian MIDA (703478) można było przygotować poprzez bromoborowanie acetylenu i reakcję z MIDA w obecności zasady, opracowano później wygodniejszą procedurę. Syntezę trans-(2-bromowinylo) boronianu MIDA uzyskuje się poprzez transmetalizację 1-bromo-2-trimetylosililoetylenu za pomocą BBr3.a następnie pułapkowanie za pomocą MIDA2-Na+2 tworząc boronian MIDA (Schemat 11-(1)). Podobnie, tworzenie boronianu MIDA winylu zostało osiągnięte zgodnie z tą procedurą, dając początek bardzo użytecznemu blokowi budulcowemu boronianu MIDA winylu (Schemat 11-(2)). Warto zauważyć, że odpowiedni kwas boronowy jest bardzo niestabilny.

Scheme 11
Użyteczność syntetyczna boronianu MIDA winylu
Użyteczność boronianu MIDA winylu została zademonstrowana poprzez cyklopropanowanie i epoksydowanie do odpowiedniego cyklopropanu i oksiranu MIDA. Procedury te (Schemat 12) zapewniły w obu przypadkach stabilne w powietrzu i chromatografii ciała stałe, przy czym oksiran jest pierwszą znaną syntezą niepodstawionego oksiranyloboranu (potwierdzoną analizą rentgenowską oksiranyloboranu).
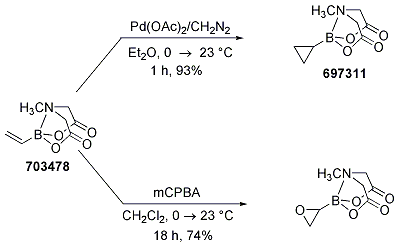
Scheme 12
Boronian winylu MIDA został również z powodzeniem poddany reakcjom Hecka i utleniającym reakcjom Hecka, a także metatezie olefin (Schemat 13) w celu uzyskania produktu sprzężonego krzyżowo. Metateza krzyżowa boronianu MIDA winylu z różnymi olefinami stanowi silną strategię dla wysoce stereoselektywnej konstrukcji podstawionych boranów winylowych. Metoda ta okazała się skuteczna w przygotowaniu różnych niepodstawionych olefin (Tabela 1) z doskonałą wydajnością (81-98%) i diastereoselektywnością (>20:1) i stanowi znaczący postęp, ponieważ metoda ta była często ograniczona stabilnością alkenylowych estrów boronowych, diastereoselektywnością transformacji lub łatwością oczyszczania produktu niepodstawionego alkenyloboranu.

Scheme 13

Table 1.Cross-Metathesis with Vinylboronic acid MIDA ester
Powolne uwalnianie niestabilnych kwasów boronowych z boronianów MIDA
Oprócz osłabionej reaktywności w kierunku bezwodnego sprzęgania krzyżowego, boroniany MIDA posiadają wysoce sprzyjającą zdolność do in situ powolnego uwalniania kwasów boronowych w wodnych warunkach zasadowych. Wykorzystując to zjawisko, kwasy boronowe, które są notorycznie niestabilne, mogą być skutecznie wykorzystywane w sprzęganiu krzyżowym, gdy są stosowane jako boroniany MIDA. wolne uwalnianie bardziej wrażliwych kwasów boronowych można osiągnąć stosując K3PO4. Podczas gdy wodne roztwory NaOH sprzyjają szybkiej hydrolizie do odpowiedniego kwasu boronowego, zastosowanie wodnego K3PO4 pozwala na powolne uwalnianie stosunkowo niestabilnego kwasu boronowego, co zapobiega rozkładowi prekursora metaloorganicznego i poprawia ogólną wydajność reakcji Suzuki.

Figure 1. Slow-Release of Unstable Boronic Acids
- Stabilność w powietrzu
- Stabilność w warunkach bezwodnego sprzęgania krzyżowego
- Kompatybilność z typowymi i trudnymi odczynnikami syntetycznymi<
- Rozpuszczalność w różnych rozpuszczalnikach organicznych
- Skład monomeryczny
- Kompatybilność z żelem krzemionkowym<
Burke i współpracownicy zbadali koncepcję powolnego uwalniania poprzez porównanie różnych świeżo przygotowanych kwasów boronowych z odpowiadającymi im boronianami MIDA, biorąc pod uwagę zarówno stabilność laboratoryjną, jak i wydajność w sprzęganiu krzyżowym. Badanie wykazało, że wiele kwasów boronowych ulega znacznemu rozkładowi za pomocą różnych metod, w tym protodeboronacji, utleniania i polimeryzacji (po zaledwie 15 dniach przechowywania na stole laboratoryjnym w powietrzu -Tabela 2). Z drugiej strony, odpowiadające im boroniany MIDA były wyjątkowo stabilne, a 95% każdego MIDA pozostało po ≥60 dniach przechowywania w powietrzu. Oprócz komplikacji związanych z przechowywaniem różnych klas kwasów boronowych, na wydajność reakcji Suzuki wpływa również charakter jednostki boronowej, ponieważ kwasy boronowe rozkładają się in situ szybciej niż może wystąpić sprzężenie krzyżowe. Scenariusz ten dodatkowo komplikuje fakt, że rozkład jest przyspieszany w obecności odczynników i warunków wspólnych dla wielu reakcji Suzuki. Zgodnie z tą analizą, wydajności obserwowane, gdy nawet świeżo przygotowane kwasy boronowe są stosowane w reakcjach sprzęgania krzyżowego, są na ogół niskie lub umiarkowane. W przeciwieństwie do tego, gdy boroniany MIDA zostały poddane tym samym warunkom reakcji, konwersja do produktu sprzęgania krzyżowego została osiągnięta z doskonałą wydajnością (Tabela 2).

Table 2.Comparison of Benchtop Stability and Coupling Efficiency of Boronic Acids and MIDA Boronates
Zakres tego nowego zjawiska był dalej badany przy użyciu różnych boronianów MIDA, z których odpowiednie kwasy boronowe historycznie wykazywały wyzwania w odniesieniu do przechowywania lub użytkowania. Tabela 3 pokazuje szereg boronianów MIDA, które są wysoce skuteczne w reakcjach sprzęgania krzyżowego Suzuki-Miyaura z nieaktywowanymi (i w wielu przypadkach elektronicznie lub sterycznie dezaktywowanymi) chlorkami arylowymi i heteroarylowymi. Oprócz 2-podstawionych heteroarylowych boronianów MIDA, boronian winylowy MIDA, jak również boronian cyklopropylowy MIDA zostały wykorzystane w warunkach powolnego uwalniania w celu uzyskania trudnych sprzężeń z dezaktywowanymi chlorkami heteroarylowymi. Niezabezpieczone kwasy boronowe są ogólnie znane jako słabe substraty do sprzęgania krzyżowego, ale gdy są generowane z odpowiednich boronianów MIDA w warunkach powolnego uwalniania, stają się realnymi kandydatami syntetycznymi, zapewniając produkt sprzężony krzyżowo z doskonałą wydajnością.

Table 3.Slow Release Cross-Coupling of MIDA boronates
Opracowanie stabilnego w powietrzu i skutecznego surogatu dla notorycznie niestabilnego kwasu 2-pirydyloboronowego jest od dawna wyzwaniem w dziedzinie sprzęgania krzyżowego. Motyw ten jest wszechobecny w małych cząsteczkach podobnych do leków, co czyni ten problem szczególnie ważnym. Chociaż istnieją surogaty kwasu 2-pirydylo-boronowego, ich użycie jest skomplikowane ze względu na ich wrażliwość na powietrze i wilgoć, a także ich nieco zmienny i nieczysty skład. W przeciwieństwie do tego, Burke i współpracownicy odkryli, że boronian 2-pirydylu MIDA jest izolowalny, stabilny w warunkach laboratoryjnych i stabilny w chromatografii. Podczas gdy warunki sprzyjające powolnemu sprzęganiu krzyżowemu, o którym mowa powyżej, nie były generalnie skuteczne w przypadku boronianu 2-pirydylu MIDA, wykorzystanie izopropanolu zamiast wody jako współrozpuszczalnika i substechiometrycznej ilości Cu(OAc)2 jako współkatalizatora (wcześniej wykazano, że sole miedzi sprzyjają trudnym sprzęganiom Suzuki-Miyaura) okazało się skuteczne. Oprócz bezprecedensowej stabilności laboratoryjnej boronianu 2-pirydylu MIDA (uzyskano strukturę rentgenowską), powolne uwalnianie aktywnych form boru pozwala na udane sprzęganie z różnymi chlorkami arylowymi i heteroarylowymi (Tabela 4).

Table 4.Slow Release Cross-Coupling of 2-pyridyl MIDA boronate
Discover MIDA Boronates (1 Mb PDF)
Zobacz naszą pełną listę MIDA Boronates.
Aby uzyskać więcej informacji, zapoznaj się z następującymi publikacjami:
Zaloguj się lub utwórz konto, aby kontynuować.
Nie masz konta użytkownika?
