Kluczowe dokumenty
SMB01385
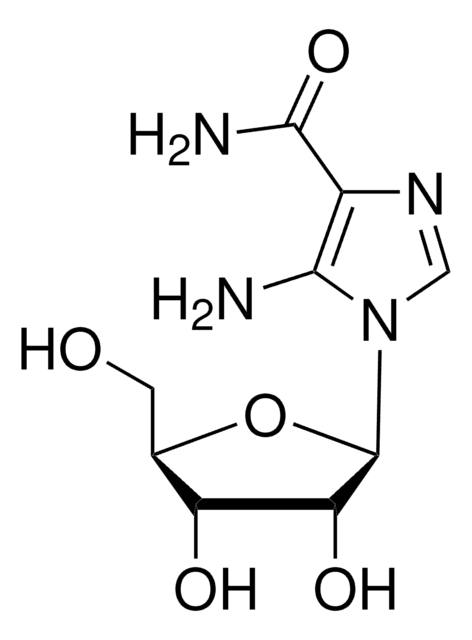
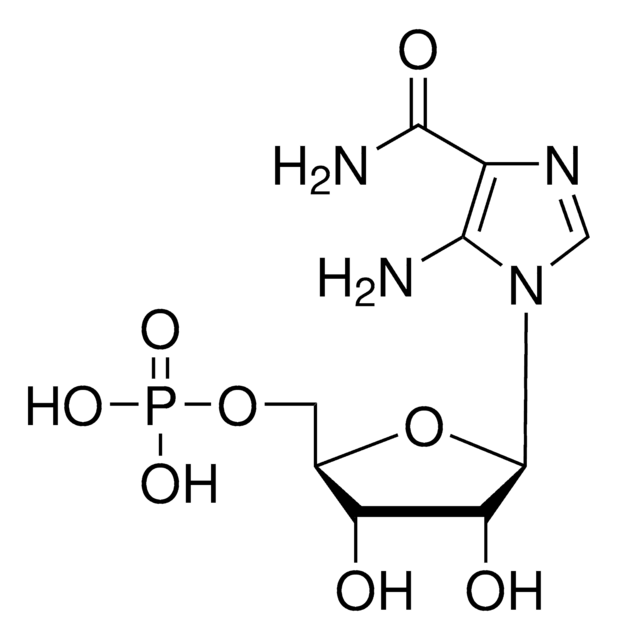
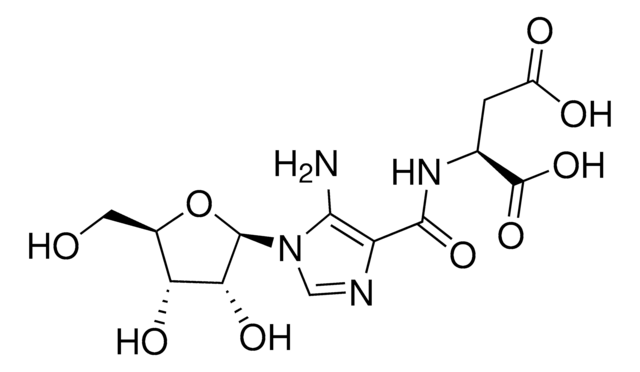
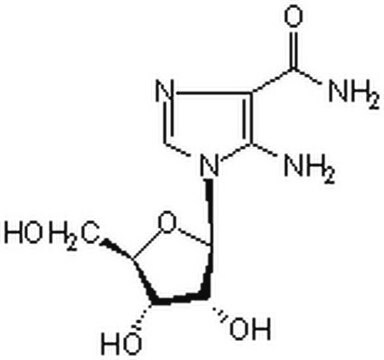
SAICAR
≥95% (HPLC)
Synonim(y):
Kwas N-[[5-amino-1-(5-O-fosfono-β-D-ribofuranozylo)-1H-imidazolo-4-ylo]karbonylo]-L-asparaginowy, Succino-AICAR, Sukcynylo-AICAR
About This Item
Polecane produkty
pochodzenie biologiczne
synthetic
Poziom jakości
Próba
≥95% (HPLC)
Formularz
solid
Zastosowanie
metabolomics
Warunki transportu
2-8°C
temp. przechowywania
2-8°C
ciąg SMILES
NC1=C(N=CN1[C@H]2[C@H](O)[C@H](O)[C@@H](COP(O)(O)=O)O2)C(N[C@@H](CC(O)=O)C(O)=O)=O
InChI
1S/C13H19N4O12P/c14-10-7(11(22)16-4(13(23)24)1-6(18)19)15-3-17(10)12-9(21)8(20)5(29-12)2-28-30(25,26)27/h3-5,8-9,12,20-21H,1-2,14H2,(H,16,22)(H,18,19)(H,23,24)(H2,25,26,27)/t4-,5+,8+,9+,12+/m0/s1
Klucz InChI
NAQGHJTUZRHGAC-ZZZDFHIKSA-N
Opis ogólny
Kod klasy składowania
11 - Combustible Solids
Klasa zagrożenia wodnego (WGK)
WGK 3
Temperatura zapłonu (°F)
Not applicable
Temperatura zapłonu (°C)
Not applicable
Wybierz jedną z najnowszych wersji:
Certyfikaty analizy (CoA)
It looks like we've run into a problem, but you can still download Certificates of Analysis from our Dokumenty section.
Proszę o kontakt, jeśli potrzebna jest pomoc Obsługa Klienta
Masz już ten produkt?
Dokumenty związane z niedawno zakupionymi produktami zostały zamieszczone w Bibliotece dokumentów.
Nasz zespół naukowców ma doświadczenie we wszystkich obszarach badań, w tym w naukach przyrodniczych, materiałoznawstwie, syntezie chemicznej, chromatografii, analityce i wielu innych dziedzinach.
Skontaktuj się z zespołem ds. pomocy technicznej