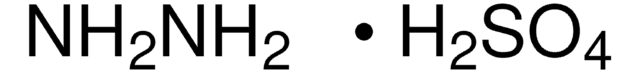8.04608
Hydrazinium hydroxide
(about 100% N₂H₅OH) for synthesis
Synonim(y):
Hydrazinium hydroxide, Hydrazine hydrate
About This Item
Polecane produkty
ciśnienie pary
20 hPa ( 20 °C)
Poziom jakości
Postać
liquid
temp. samozapłonu
280 °C
siła działania
169 mg/kg LD50, oral (Rat)
granice wybuchowości
3.4-99 % (v/v)
pH
10-11 (20 °C, 10 g/L in H2O)
tw
120.5 °C/1013 hPa
mp
-51.7 °C
gęstość
1.03 g/cm3 at 20 °C
temp. przechowywania
15-25°C
InChI
1S/H4N2.H2O/c1-2;/h1-2H2;1H2
Klucz InChI
IKDUDTNKRLTJSI-UHFFFAOYSA-N
Zastosowanie
- Magnetic nickel nanoparticles by polyol process using nickel acetate as a precursor.
- Cu@Cu2O core-shell nanoparticles via a chemical reduction method using CuSO4.5H2O as a precursor.
It can also be used as a reactant to prepare:
2H-indazolo[2,1-b]phthalazine-1,6,11(13H)-trione derivatives by Ce(SO4)2·4H2O catalyzed condensation reaction with phthalic anhydride, aromatic aldehydes, and dimedone.
Hasło ostrzegawcze
Danger
Zwroty wskazujące rodzaj zagrożenia
Zwroty wskazujące środki ostrożności
Klasyfikacja zagrożeń
Acute Tox. 2 Inhalation - Acute Tox. 3 Dermal - Acute Tox. 3 Oral - Aquatic Acute 1 - Aquatic Chronic 1 - Carc. 1B - Eye Dam. 1 - Flam. Liq. 3 - Skin Corr. 1B - Skin Sens. 1
Kod klasy składowania
3 - Flammable liquids
Klasa zagrożenia wodnego (WGK)
WGK 3
Temperatura zapłonu (°F)
100.4 °F - closed cup - (anhydrous substance)
Temperatura zapłonu (°C)
38 °C - closed cup - (anhydrous substance)
Certyfikaty analizy (CoA)
Poszukaj Certyfikaty analizy (CoA), wpisując numer partii/serii produktów. Numery serii i partii można znaleźć na etykiecie produktu po słowach „seria” lub „partia”.
Masz już ten produkt?
Dokumenty związane z niedawno zakupionymi produktami zostały zamieszczone w Bibliotece dokumentów.
Klienci oglądali również te produkty
Protokoły
Rozszczepienie i deprotekcja żywicy Fmoc są kluczowymi etapami syntezy peptydów, dając pożądany peptyd po odłączeniu żywicy.
Powiązane treści
Fmoc resin cleavage and deprotection follows the difficult task of detaching the peptide from the resin support and removing all the side-chain protecting groups of the amino acid residues to yield the desired peptide.
Nasz zespół naukowców ma doświadczenie we wszystkich obszarach badań, w tym w naukach przyrodniczych, materiałoznawstwie, syntezie chemicznej, chromatografii, analityce i wielu innych dziedzinach.
Skontaktuj się z zespołem ds. pomocy technicznej