すべての画像(1)
About This Item
化学式:
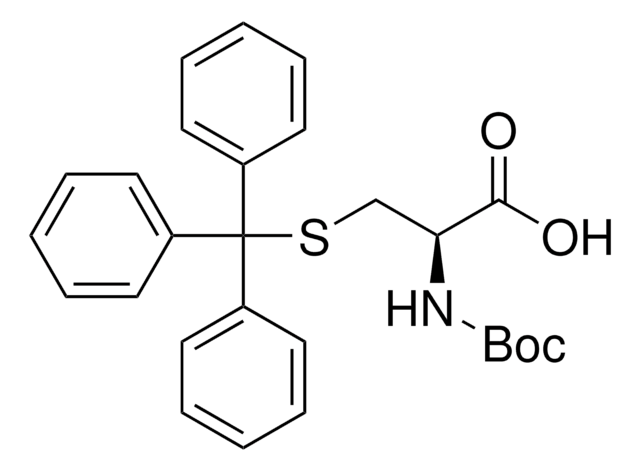
(C6H5)3CSCH2CH(NH2)CO2H
CAS番号:
分子量:
363.47
Beilstein:
2339626
MDL番号:
UNSPSCコード:
12352209
eCl@ss:
32160406
PubChem Substance ID:
NACRES:
NA.22
おすすめの製品
製品名
(+)-S-トリチル-L-システイン, 97%
品質水準
アッセイ
97%
光学活性
[α]25/D +115°, c = 0.8 in 0.04 M ethanolic HCl
反応適合性
reaction type: solution phase peptide synthesis
mp
182-183 °C (dec.) (lit.)
アプリケーション
peptide synthesis
SMILES記法
N[C@@H](CSC(c1ccccc1)(c2ccccc2)c3ccccc3)C(O)=O
InChI
1S/C22H21NO2S/c23-20(21(24)25)16-26-22(17-10-4-1-5-11-17,18-12-6-2-7-13-18)19-14-8-3-9-15-19/h1-15,20H,16,23H2,(H,24,25)/t20-/m0/s1
InChI Key
DLMYFMLKORXJPO-FQEVSTJZSA-N
類似した製品をお探しですか? 訪問 製品比較ガイド
アプリケーション
(+)-S-トリチル-L-システインは、非天然含硫アミノ酸であり、液相ペプチド合成(SPPS)の試薬として一般的に使用されています。ペプチド金属相互作用を介したカチオンセンシングアプリケーションソリューションのための、HBTUペプチドカップリング試薬を用いた置換フェロセノイルペプチド複合体を合成する金属結合剤としても使用されます。
適用法令
試験研究用途を考慮した関連法令を主に挙げております。化学物質以外については、一部の情報のみ提供しています。 製品を安全かつ合法的に使用することは、使用者の義務です。最新情報により修正される場合があります。WEBの反映には時間を要することがあるため、適宜SDSをご参照ください。
Jan Code
164739-VAR:
164739-5G:
164739-BULK:
164739-1G:
164739-25G:
この製品を見ている人はこちらもチェック
Sébastien Brier et al.
Journal of molecular biology, 360(2), 360-376 (2006-06-20)
The mitotic kinesin Eg5 plays an essential role in establishing the bipolar spindle. Recently, several antimitotic inhibitors have been shown to share a common binding region on Eg5. Considering the importance of Eg5 as a potential drug target for cancer
James A D Good et al.
Journal of medicinal chemistry, 56(5), 1878-1893 (2013-02-12)
The mitotic kinesin Eg5 is critical for the assembly of the mitotic spindle and is a promising chemotherapy target. Previously, we identified S-trityl-L-cysteine as a selective inhibitor of Eg5 and developed triphenylbutanamine analogues with improved potency, favorable drug-like properties, but
Frank Kozielski et al.
Proteomics, 8(2), 289-300 (2008-01-11)
Mitotic kinesins represent potential drug targets for anticancer chemotherapy. Inhibitors of different chemical classes have been identified that target human Eg5, a kinesin responsible for the establishment of the bipolar spindle. One potent Eg5 inhibitor is S-trityl-L-cysteine (STLC), which arrests
Total synthesis of didmolamides A and B
You Shu-Li and Kelly JW
Tetrahedron Letters, 46(15), 2567-2570 (2005)
Daniel B Nichols et al.
European journal of medicinal chemistry, 49, 191-199 (2012-01-28)
Structure-based studies led to the identification of a constrained derivative of S-trityl-l-cysteine (STLC) scaffold as a candidate inhibitor of hepatitis C virus (HCV) NS5B polymerase. A panel of STLC derivatives were synthesized and investigated for their activity against HCV NS5B.
ライフサイエンス、有機合成、材料科学、クロマトグラフィー、分析など、あらゆる分野の研究に経験のあるメンバーがおります。.
製品に関するお問い合わせはこちら(テクニカルサービス)