D1411
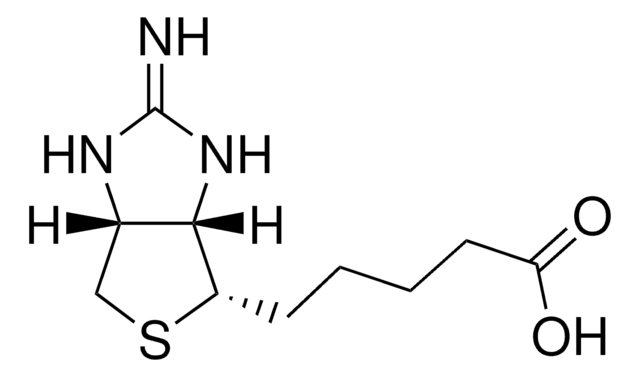
d-destiobiotina
≥98% (TLC)
Sinonimo/i:
Acido 5-metil-2-osso-4-imidazolidinesanoico
About This Item
Prodotti consigliati
Livello qualitativo
Saggio
≥98% (TLC)
Forma fisica
powder
Temperatura di conservazione
2-8°C
Stringa SMILE
C[C@@H]1NC(=O)N[C@@H]1CCCCCC(O)=O
InChI
1S/C10H18N2O3/c1-7-8(12-10(15)11-7)5-3-2-4-6-9(13)14/h7-8H,2-6H2,1H3,(H,13,14)(H2,11,12,15)/t7-,8+/m0/s1
AUTOLBMXDDTRRT-JGVFFNPUSA-N
Applicazioni
- le proteine precipitate dalla resina durante la coimmunoprecipitazione;
- l'elicasi CMG (Cdc45–MCM–GINS) umana durante la purificazione cromatografica delle proteine;
- il membro eterodimerico 3A/B (KIF3A/B) della famiglia delle chinesine e il dominio APCARM (APC armadillo) che lega KAP3 (proteina 3 associata alle chinesine) durante la purificazione cromatografica
Azioni biochim/fisiol
Codice della classe di stoccaggio
11 - Combustible Solids
Classe di pericolosità dell'acqua (WGK)
WGK 3
Punto d’infiammabilità (°F)
Not applicable
Punto d’infiammabilità (°C)
Not applicable
Dispositivi di protezione individuale
Eyeshields, Gloves, type N95 (US)
Certificati d'analisi (COA)
Cerca il Certificati d'analisi (COA) digitando il numero di lotto/batch corrispondente. I numeri di lotto o di batch sono stampati sull'etichetta dei prodotti dopo la parola ‘Lotto’ o ‘Batch’.
Possiedi già questo prodotto?
I documenti relativi ai prodotti acquistati recentemente sono disponibili nell’Archivio dei documenti.
Il team dei nostri ricercatori vanta grande esperienza in tutte le aree della ricerca quali Life Science, scienza dei materiali, sintesi chimica, cromatografia, discipline analitiche, ecc..
Contatta l'Assistenza Tecnica.