Wichtige Dokumente
A2181
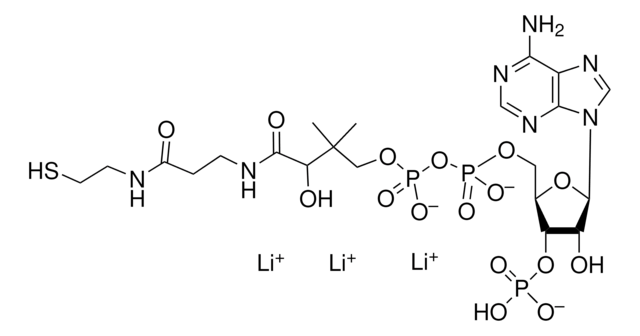
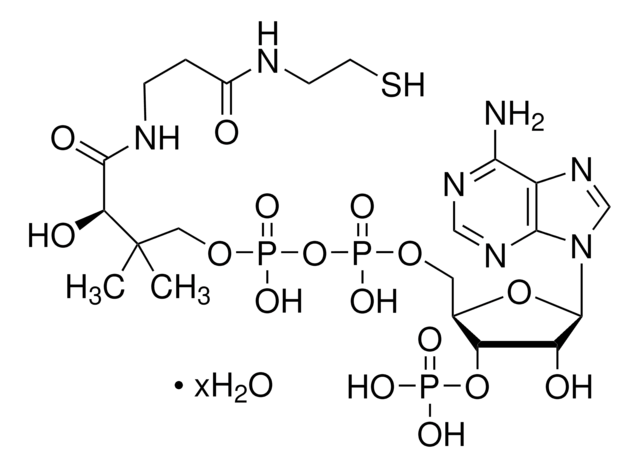
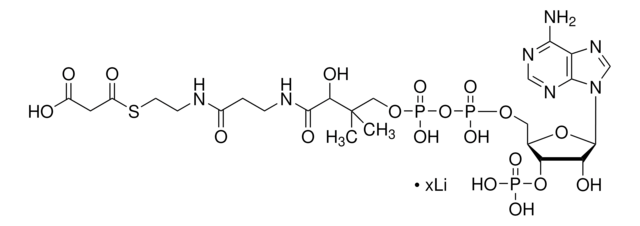
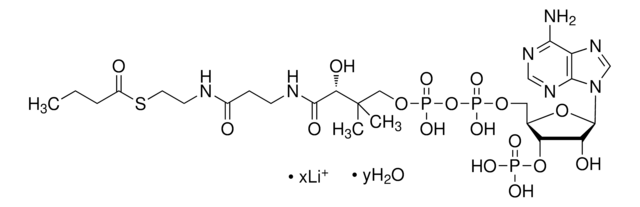
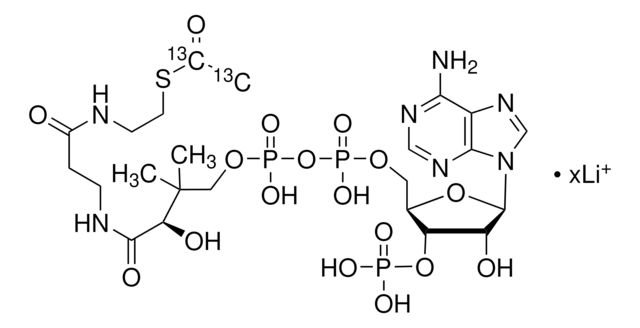
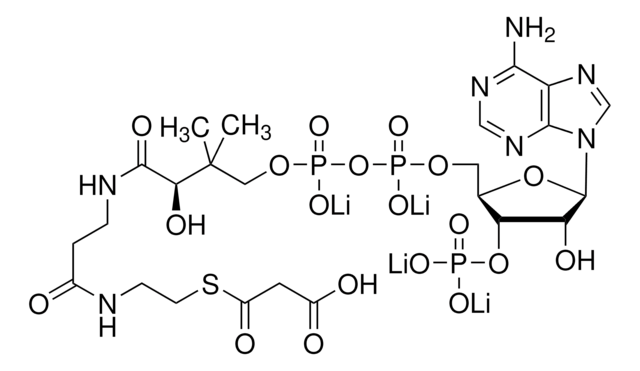
Acetyl-Coenzym A Trilithiumsalz
≥93% (HPLC)
Synonym(e):
Acetyl-CoA, Acetyl-S-CoA Li3
About This Item
Empfohlene Produkte
Qualitätsniveau
Assay
≥93% (HPLC)
Form
powder
Löslichkeit
H2O: soluble 100 mg/mL, clear, colorless
Lagertemp.
−20°C
SMILES String
[Li+].[Li+].[Li+].CC(=O)SCCNC(=O)CCNC(=O)[C@H](O)C(C)(C)COP([O-])(=O)OP([O-])(=O)OC[C@H]1O[C@H]([C@H](O)[C@@H]1OP(O)([O-])=O)n2cnc3c(N)ncnc23
InChI
1S/C23H38N7O17P3S.3Li/c1-12(31)51-7-6-25-14(32)4-5-26-21(35)18(34)23(2,3)9-44-50(41,42)47-49(39,40)43-8-13-17(46-48(36,37)38)16(33)22(45-13)30-11-29-15-19(24)27-10-28-20(15)30;;;/h10-11,13,16-18,22,33-34H,4-9H2,1-3H3,(H,25,32)(H,26,35)(H,39,40)(H,41,42)(H2,24,27,28)(H2,36,37,38);;;/q;3*+1/p-3/t13-,16-,17-,18+,22-;;;/m1.../s1
InChIKey
FTRFBNATWBKIQU-JHJDYNLLSA-K
Angaben zum Gen
human ... CHAT(1103) , HAT1(8520) , KAT2A(2648) , KAT2B(8850) , KAT5(10524)
mouse ... HAT1(107435) , KAT2A(14534) , KAT2B(18519) , KAT5(81601)
rat ... HAT1(296501) , KAT2A(303539) , KAT2B(301164) , KAT5(192218)
Suchen Sie nach ähnlichen Produkten? Aufrufen Leitfaden zum Produktvergleich
Anwendung
Biochem./physiol. Wirkung
Physikalische Eigenschaften
Angaben zur Herstellung
Rekonstituierung
Sonstige Hinweise
Signalwort
Warning
H-Sätze
Gefahreneinstufungen
Eye Irrit. 2 - Skin Irrit. 2 - STOT SE 3
Zielorgane
Respiratory system
Lagerklassenschlüssel
11 - Combustible Solids
WGK
WGK 3
Flammpunkt (°F)
Not applicable
Flammpunkt (°C)
Not applicable
Persönliche Schutzausrüstung
dust mask type N95 (US), Eyeshields, Gloves
Hier finden Sie alle aktuellen Versionen:
Besitzen Sie dieses Produkt bereits?
In der Dokumentenbibliothek finden Sie die Dokumentation zu den Produkten, die Sie kürzlich erworben haben.
Kunden haben sich ebenfalls angesehen
Artikel
Get to know the Tricarboxylic acid (TCA) cycle to better inform your research in biochemistry, metabolomics, or related fields concerned with this metabolic pathway and its enzymes, by-products, or intermediates.
Unser Team von Wissenschaftlern verfügt über Erfahrung in allen Forschungsbereichen einschließlich Life Science, Materialwissenschaften, chemischer Synthese, Chromatographie, Analytik und vielen mehr..
Setzen Sie sich mit dem technischen Dienst in Verbindung.