P4234
Pyranose-Oxidase aus Coriolus sp.
recombinant, expressed in E. coli, ≥2.7 units/mg solid
Synonym(e):
Pyranose: Sauerstoff 2-Oxidoreduktase
Anmeldenzur Ansicht organisationsspezifischer und vertraglich vereinbarter Preise
Alle Fotos(2)
About This Item
CAS-Nummer:
MDL-Nummer:
UNSPSC-Code:
12352204
NACRES:
NA.54
Empfohlene Produkte
Rekombinant
expressed in E. coli
Qualitätsniveau
Form
powder
Spezifische Aktivität
≥2.7 units/mg solid
Versandbedingung
wet ice
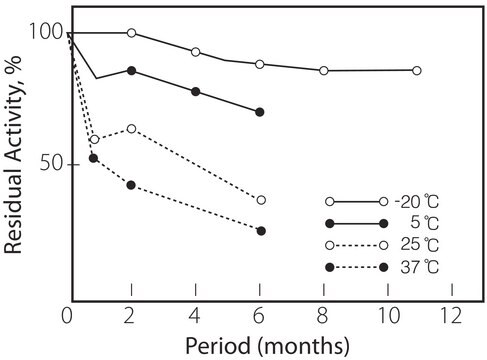
Lagertemp.
−20°C
Allgemeine Beschreibung
Pyranose-Oxidase (P2O) ist ein homotetramerisches Protein, das aus einem kovalent gebundenen Flavin-Adenin-Dinukleotid (FAD) besteht. P2O kommt vorwiegend in holzabbauenden Basidiomyceten vor.
Anwendung
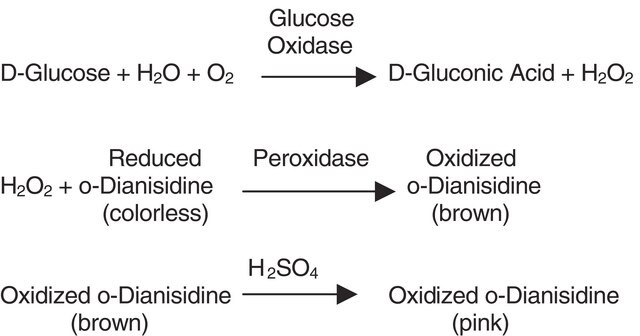
Pyranose-Oxidase von Coriolus sp. wird zur enzymatischen Oxidation von D-Glucose (DG) eingesetzt. Sie wird ebenfalls als Bestandteil in Sauerstoffabsorbern eingesetzt, um die Lebenszeit der Fluorophore zu erhöhen.
Biochem./physiol. Wirkung
In der klinischen Chemie kann Pyranose-Oxidase (P2O) zur Erkennung des 1,5-Anhydroglucitolmarkers eingesetzt werden, der zur glykämischen Kontrolle von Patienten mit Diabetes verwendet wird.
Pyranose-Oxidase (P2O) katalysiert die Oxidation von Aldopyranosen am C-2-Kohlenstoffatom, was zu den entsprechenden 2-Ketoaldosen führt. Es wird angenommen, dass die In-vivo-Substrate von P2O D-Glucose, D-Galactose und D-Xylose sind. Sie oxidieren zu 2-Keto-D-Glucose (D-arabino-Hexos-2-ulose, 2-Dehydro-D-Glucose), 2-Keto-D-Galactose (D-lyxo-Hexos-2-ulose, 2-Dehydro-D-Galactose) bzw. 2-Keto-D-Xylose (D-Threopentos-2-ulose, 2-Dehydro-D-Xylose). Pyranose-Oxidase weist eine bedeutende Aktivität mit Kohlenhydraten wie L-Sorbose, D-Glucono-1,5-lacton und D-Allose auf. Wenn Pyranose-Oxidase die Oxidation der Aldopyranosen katalysiert, werden Elektronen zu molekularem Sauerstoff übertragen und es kommt zur Bildung von Wasserstoffperoxid.
Einheitendefinition
Eine Einheit produziert 1,0 μmol Wasserstoffperoxid pro Minute bei 37 °C und einem pH-Wert von 7,0.
Sonstige Hinweise
Enthält Glutamat
Signalwort
Danger
H-Sätze
P-Sätze
Gefahreneinstufungen
Resp. Sens. 1
Lagerklassenschlüssel
11 - Combustible Solids
WGK
WGK 1
Flammpunkt (°F)
Not applicable
Flammpunkt (°C)
Not applicable
Analysenzertifikate (COA)
Suchen Sie nach Analysenzertifikate (COA), indem Sie die Lot-/Chargennummer des Produkts eingeben. Lot- und Chargennummern sind auf dem Produktetikett hinter den Wörtern ‘Lot’ oder ‘Batch’ (Lot oder Charge) zu finden.
Besitzen Sie dieses Produkt bereits?
In der Dokumentenbibliothek finden Sie die Dokumentation zu den Produkten, die Sie kürzlich erworben haben.
Kunden haben sich ebenfalls angesehen
The influence of temperature on bioconversion of D-glucose into 2-keto-D-glucose by Pyranose oxidase
Ene MD, et al.
UPB Scientific Bulletin, Series B: Chemistry and Materials Science, 2 (2014)
Oliver Spadiut et al.
Microbial cell factories, 9, 14-14 (2010-03-11)
The heterologous production of the industrially relevant fungal enzyme pyranose 2-oxidase in the prokaryotic host E. coli was investigated using 3 different expression systems, i.e. the well-studied T7 RNA polymerase based pET21d+, the L-arabinose inducible pBAD and the pCOLD system.
Antti Lignell et al.
Nature communications, 8(1), 1830-1830 (2017-12-01)
The neural crest is an embryonic population of multipotent stem cells that form numerous defining features of vertebrates. Due to lack of reliable techniques to perform transcriptional profiling in intact tissues, it remains controversial whether the neural crest is a
Warintra Pitsawong et al.
The Journal of biological chemistry, 285(13), 9697-9705 (2010-01-22)
Pyranose 2-oxidase (P2O) catalyzes the oxidation by O(2) of d-glucose and several aldopyranoses to yield the 2-ketoaldoses and H(2)O(2). Based on crystal structures, in one rotamer conformation, the threonine hydroxyl of Thr(169) forms H-bonds to the flavin-N5/O4 locus, whereas, in
Tien-Chye Tan et al.
Journal of molecular biology, 402(3), 578-594 (2010-08-17)
Flavoenzymes perform a wide range of redox reactions in nature, and a subclass of flavoenzymes carry covalently bound cofactor. The enzyme-flavin bond helps to increase the flavin's redox potential to facilitate substrate oxidation in several oxidases. The formation of the
Unser Team von Wissenschaftlern verfügt über Erfahrung in allen Forschungsbereichen einschließlich Life Science, Materialwissenschaften, chemischer Synthese, Chromatographie, Analytik und vielen mehr..
Setzen Sie sich mit dem technischen Dienst in Verbindung.