914339
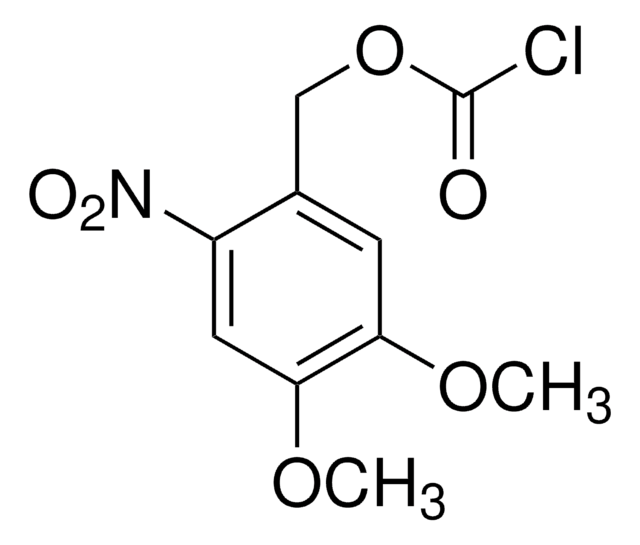
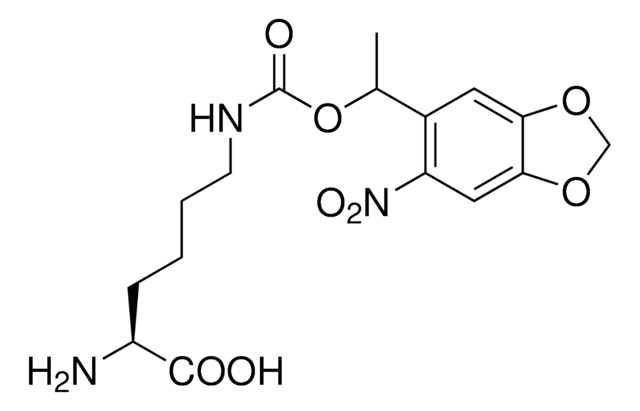
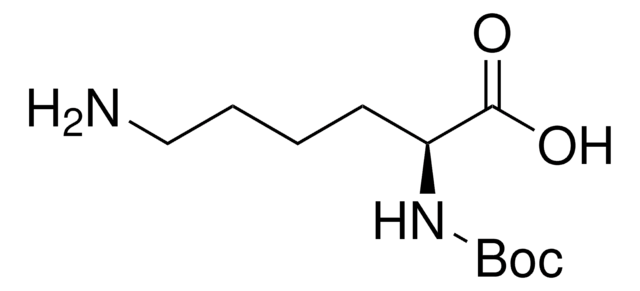
Fmoc-L-Lys(Nvoc)-OH
≥98%
Synonym(e):
(S)-2-(((9H-Fluoren-9-yl)methoxy)carbonylamino)-6-((4,5-dimethoxy-2-nitrobenzyloxy)carbonylamino)hexanoic acid, N2-(((9H-Fluoren-9-yl)methoxy)carbonyl)-N6-(((4,5-dimethoxy-2-nitrobenzyl)oxy)carbonyl)-L-lysine, Lysine with photoremovable NVOC, Photocaged amino acid, Photocleavable lysine derivative
About This Item
Empfohlene Produkte
Anwendung
Product can be used with our line of photoreactors: Including Penn PhD (Z744035) & SynLED 2.0 (Z744080)
Ähnliches Produkt
Lagerklassenschlüssel
11 - Combustible Solids
WGK
WGK 3
Flammpunkt (°F)
Not applicable
Flammpunkt (°C)
Not applicable
Hier finden Sie alle aktuellen Versionen:
Analysenzertifikate (COA)
Leider sind derzeit keine COAs für dieses Produkt online verfügbar.
Wenn Sie Hilfe benötigen, wenden Sie sich bitte an Kundensupport
Besitzen Sie dieses Produkt bereits?
In der Dokumentenbibliothek finden Sie die Dokumentation zu den Produkten, die Sie kürzlich erworben haben.
Unser Team von Wissenschaftlern verfügt über Erfahrung in allen Forschungsbereichen einschließlich Life Science, Materialwissenschaften, chemischer Synthese, Chromatographie, Analytik und vielen mehr..
Setzen Sie sich mit dem technischen Dienst in Verbindung.