Przewodnik wyboru glikolu polietylenowego (PEG)
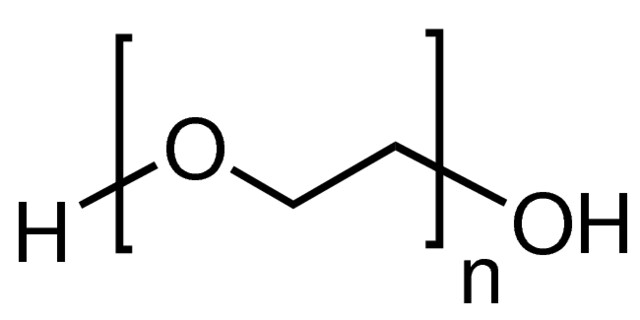
Struktura poli(glikolu etylenowego) (PEG)
Co to jest glikol polietylenowy?
Poli(glikol etylenowy) (PEG) to syntetyczny, hydrofilowy, biokompatybilny polimer o szerokim zastosowaniu w biomedycynie i innych aplikacjach. PEG są syntetyzowane przy użyciu polimeryzacji tlenku etylenu z otwarciem pierścienia w celu uzyskania szerokiego zakresu mas cząsteczkowych i rozkładów masy cząsteczkowej (polidyspersyjność); jednakże, dyskretne PEG (dPEG® odczynniki) są syntetyzowane z pojedynczą, określoną masą cząsteczkową. PEG mogą być syntetyzowane w geometrii liniowej, rozgałęzionej, w kształcie litery Y lub wieloramiennej. PEG mogą być aktywowane poprzez zastąpienie końcowej hydroksylowej grupy końcowej różnymi reaktywnymi funkcjonalnymi grupami końcowymi umożliwiającymi chemię sieciowania i koniugacji.
Jak wykorzystywany jest glikol polietylenowy?
PEG są nietoksyczne, zatwierdzone przez FDA, generalnie nieimmunogenne i są często wykorzystywane w wielu zastosowaniach biomedycznych, w tym w biokoniugacji,1 dostarczanie leków,2,3 funkcjonalizacja powierzchni,4 i inżynieria tkankowa.5 Biokoniugacja z PEG (znana również jako PEGylacja) to kowalencyjne sprzęganie celów leków, takich jak peptydy, białka lub oligonukleotydy z PEG w celu optymalizacji właściwości farmakokinetycznych.6 W dostarczaniu leków, PEG mogą być stosowane jako łączniki dla koniugatów przeciwciało-lek (ADC)7 lub jako powłoka powierzchniowa na nanocząstkach w celu poprawy ogólnoustrojowego dostarczania leków.6 PEG hydrożele to napęczniałe wodą, trójwymiarowe sieci polimerowe odporne na adhezję białek i biodegradację.8 Hydrożele PEG są wytwarzane przez sieciowanie reaktywnych grup końcowych PEG i są powszechnie stosowane w inżynierii tkankowej i dostarczaniu leków.
Wspólne grupy funkcyjne i odpowiadające im grupy reaktywne są wymienione w poniższej tabeli.
Referencje
Zaloguj się lub utwórz konto, aby kontynuować.
Nie masz konta użytkownika?