Spektrometria masowa
Co to jest spektrometria mas i do czego służy?
Spektrometria mas (MS) to narzędzie analityczne wykorzystywane do określania mas różnych związków w próbce. Technika ta jest przydatna do identyfikacji i ilościowego oznaczania związków w mieszaninie, co może obejmować wykrywanie zanieczyszczeń w próbce lub określanie mieszaniny białek w próbce komórkowej. Działa poprzez pomiar stosunku m/z (masy do ładunku) jonów.
Jak działa spektrometria mas?
Istnieje wiele wariacji na temat spektrometrii mas, ale podstawy są takie same i są w przybliżeniu trzy (może to zależeć od tego, jak wolisz "pogrupować" swoje kroki) i są one następujące:
- Jonizacja (źródło jonów)
- Rozdzielenie/izolacja jonów (analizator mas)
- Detekcja (detektor jonów)
Uwaga: Cały proces powinien odbywać się w próżni.
1. Jonizacja: Próbka jest odparowywana i jonizowana. (Uwaga: Jeśli próbka nie może zostać odparowana bez rozkładu, nie może być analizowana za pomocą spektrometrii masowej). Wczesna spektrometria związków organicznych opierała się na wiązce elektronów, która rozbijała białka. Jonizacja elektrorozpryskowa (ESI) i jonizacja desorpcji laserowej wspomagana matrycą (MALDI) mogą jonizować biomolekuły bez ich niszczenia. Każda technika jonizacji (ESI lub MALDI) ma swoje wady i zalety.
Jony analitu są określane jako "jony molekularne" (chyba że ulegną fragmentacji). Spektrometria masowa mierzy tylko masę naładowanych cząstek (tj. jonów). Związki neutralne są niewidoczne, ale kationy (naładowane dodatnio) i aniony (naładowane ujemnie) są "widoczne" (chociaż niektóre rodzaje spektrometrii masowej obejmują usuwanie anionów). W zależności od rodzaju spektrometrii mas, jony będą miały różne ilości ładunku. Na przykład MALDI skutkuje pojedynczymi ładunkami, ale ESI dużych cząsteczek będzie miało większe ładunki.
2. Separacja/izolacja jonów: Na tym etapie jony są rozdzielane według ich wartości m/z przy użyciu pól elektrycznych i/lub magnetycznych. Można stosować różne typy analizatorów masy, ale istota jest taka sama: interakcja między cząsteczkami o różnym ładunku i wielkości a polem (polami) powoduje rozdzielenie jonów na podstawie m/z. W przypadku separacji w polu elektrycznym ważny jest czas przelotu (TOF). Rozmiar i ładunek jonu określa, jak szybko jon dociera do detektora. (Na przykład, w polu elektrycznym, silniej naładowany, mały jon będzie poruszał się szybciej niż mniej naładowany, większy jon (Rysunek 1). W przypadku separacji w polu magnetycznym, różne jony będą w różny sposób kierować się na detektor i lądować w różnych miejscach w zależności od rozmiaru i ładunku. Innymi słowy, w przypadku pól elektrycznych liczy się to, kiedy jon zostanie wykryty, ale w przypadku pól magnetycznych liczy się to, gdzie jon zostanie wykryty.
3. Wykrywanie: Jony oddzielone przez analizator masy trafiają do detektora jonów, który rejestruje na komputerze, ile jonów trafiło dla każdego określonego stosunku m/z. Ogólnie rzecz biorąc, dane wyjściowe to pionowy wykres słupkowy, którego oś x reprezentuje rosnące m/z i którego oś y reprezentuje względną obfitość.

Rysunek 1.Schemat MALDI-TOF MS (spektrometria mas wspomagana laserem desorpcyjnym/jonizacyjnym w czasie przelotu).

Rysunek 2.Schemat ESI-MS (spektrometria mas z jonizacją elektrorozpryskową).
Jak odczytać widmo spektrometrii mas
Oś y wykresu przedstawia względną intensywność lub obfitość. Pik bazowy to pik/słupek o największej względnej liczebności. Pik bazowy może, ale nie musi być jonem molekularnym. (Dzisiejsze spektrometry masowe mogą z łatwością rozróżniać jony różniące się o jeden amu, takie jak te wykorzystujące atom deuteru zamiast atomu wodoru). Każdy pik na wykresie będzie odpowiadał innej wartości m/z i intensywności. Gdy jony mają pojedynczy ładunek, wartość m/z będzie równoważna masie cząsteczkowej. Zazwyczaj pik o najwyższym m/z odpowiada jonowi cząsteczkowemu, co daje względną masę cząsteczkową związku. (Mogą występować fragmenty, ale zwykle nie uzyskuje się większych związków.) Wzór widma - fragmenty i jon molekularny - razem wzięte mogą zidentyfikować, czym jest próbka. Baza danych wykresów widm masowych jest pomocna w porównywaniu widm i identyfikacji próbki. NIST posiada jedną taką bazę danych.
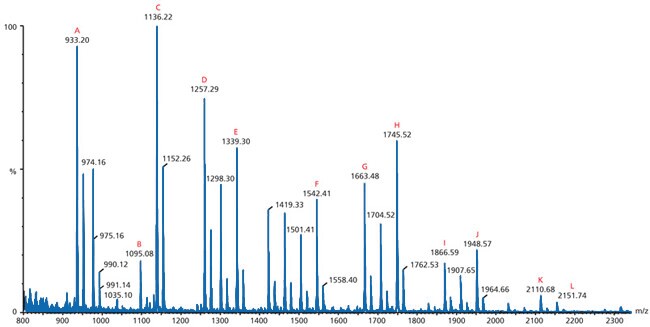
Rysunek 3.Laserowa desorpcja/jonizacja wspomagana matrycą
To konkretne widmo jest przykładem spektrometrii mas wspomaganej matrycą desorpcji/jonizacji laserowej (MALDI). Jest to dodatni jon MALDI MS neutralnych N-łańcuchowych glikanów z albuminy jaja kurzego uwolnionych przez traktowanie PNGazą F i zarejestrowanych przy użyciu 2,5-DHB jako matrycy. Litery (A-L) wskazują zidentyfikowane struktury pików.
Zaloguj się lub utwórz konto, aby kontynuować.
Nie masz konta użytkownika?