Opis ogólny
Dokładamy wszelkich starań, aby dostarczać bardziej ekologiczne produkty alternatywne, które są zgodne z co najmniej jedną z 12 zasad zielonej chemii. To przeciwciało nie zawiera konserwantów, zostało wyprodukowane bez szkody dla zwierząt i jest wyjątkowo stabilne, aby umożliwić wysyłkę i przechowywanie w razie potrzeby, a tym samym jest zgodne z "Zapobieganiem powstawaniu odpadów", "Projektowaniem bezpieczniejszych chemikaliów" i "Projektowaniem pod kątem efektywności energetycznej".
Kliknij tutaj, aby uzyskać więcej informacji.
Przeciwciała 10889 stanowią całkowicie nową generację rekombinowanych przeciwciał monoklonalnych. Każde przeciwciało 10889 jest wytwarzane przy użyciu naszego zastrzeżonego systemu ekspresji rekombinowanej, oczyszczane do jednorodności i precyzyjnie dozowane w celu uzyskania solidnej i wysoce powtarzalnej konsystencji między partiami. Do użytku badaczy udostępniane są wyłącznie klony o najwyższej wydajności. Każde przeciwciało jest walidowane pod kątem wysokiej swoistości i powinowactwa w wielu zastosowaniach, w tym w najczęściej używanym zastosowaniu. Przeciwciała 10889 są niezawodnie dostępne i gotowe do wysyłki, gdy są potrzebne.
Specyficzność
Klon 1B15 to rekombinowane królicze przeciwciało monoklonalne 10889, które specyficznie wykrywa białko oddziałujące z TRAF z białkiem B zawierającym domenę FHA (TIFAB). Jego celem jest epitop w obrębie 16 aminokwasów od regionu C-końcowego.
Immunogen
Liniowy peptyd sprzężony z KLH odpowiadający 16 aminokwasom z C-końcowego regionu ludzkiego białka TRAF oddziałującego z białkiem B zawierającym domenę FHA (TIFAB).
Zastosowanie
Testy kontroli jakości
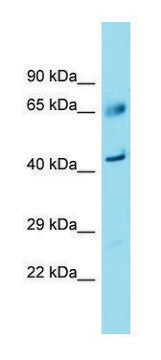
Oceniane metodą Western Blotting w lizacie komórek THP-1.
Analiza Western Blotting: Rozcieńczenie 1:10 000 tego przeciwciała wykryło TIFAB w lizacie komórek THP-1.
Testowane aplikacje
Analiza immunocytochemiczna: Rozcieńczenie 1:100 z reprezentatywnej partii wykryło TIFAB w komórkach THP-1.
Test wiązania powinowactwa: Reprezentatywna partia tego przeciwciała związała peptyd TIFAB z KD wynoszącym 1,4 x 10-6 w teście wiązania powinowactwa.
Uwaga: Rzeczywiste optymalne rozcieńczenia robocze muszą być określone przez użytkownika końcowego jako próbki, a warunki eksperymentalne mogą się różnić w zależności od użytkownika końcowego.
Opis wartości docelowych
Białko oddziałujące z TRAF z białkiem B zawierającym domenę FHA (UniProt: Q6ZNK6; znane również jako białko podobne do TIFA) jest kodowane przez gen TIFAB (Gene ID: 497189) u człowieka. Białko oddziałujące z TRAF z domeną widełkową (FHA) (TIFA) i białko oddziałujące z TRAF z białkiem B zawierającym domenę FHA (TIFAB) są ważnymi modyfikatorami wrodzonej sygnalizacji immunologicznej poprzez regulację białek TRAF. Zawierają one wysoce konserwatywną domenę FHA, która rozpoznaje reszty p-treoninowe na oddziałujących białkach. Domena FHA TIFAB jest zlokalizowana w aminokwasach 36-91, które są otoczone krótkimi sekwencjami N- i C-końcowymi. TIFA służy jako pozytywny regulator wrodzonych szlaków odpornościowych i zapalnych, podczas gdy TIFAB jest negatywnym regulatorem wrodzonych szlaków odpornościowych i zapalnych. Ekspresję TIFAB obserwuje się w śledzionie, płucach, grasicy i jelicie cienkim. Jest również wzbogacony w progenitory szpikowe i monocyty. Wykazano, że ulega wysokiej ekspresji w bardziej niedojrzałej frakcji normalnych ludzkich komórek macierzystych/progenitorowych CD34+ szpiku kostnego (BM) w porównaniu z dojrzałą frakcją komórek CD34- BM. Wykazano, że TIFAB wiąże się z TIFA i blokuje aktywację NF-κB za pośrednictwem TIFA, bez wpływu na poziomy TIFA. Ludzkie białko TIFAB wykazuje około 80% homologii do mysiego TIFAB, ale zawiera 14 dodatkowych aminokwasów na C-końcu. Delecja TIFAB w hematopoetycznych komórkach macierzystych i progenitorowych została powiązana z niewydolnością szpiku kostnego w modelach mysich. Jego delecja zwiększa sygnalizację p53 i zmniejsza funkcję komórek białaczkowych oraz rozwój białaczki. I odwrotnie, podwyższony poziom TIFAB hamuje p53 i zwiększa funkcję białaczkowych komórek progenitorowych. To rekombinowane przeciwciało monoklonalne 10889, generowane przez naszą zastrzeżoną technologię, oferuje znacznie zwiększoną swoistość, powinowactwo, powtarzalność i stabilność w porównaniu z konwencjonalnymi przeciwciałami monoklonalnymi. (Ref.: Niederkorn, M., et al. (2020). Exp. Hematol. 90; 18-29; Niederkorn, M., et al. (2020). Cell Rep. 30(8); 2776-2790; Matsumura, T., et al. (2004). Biochem. Biophys. Res. Commun. 317(1); 230-234).
Postać fizyczna
Oczyszczone rekombinowane królicze przeciwciało monoklonalne IgG, liofilizowane w PBS z 5% trehalozą, o normalnym wyglądzie gruboziarnistej lub półprzezroczystej żywicy. Składniki PBS/trehaloza w preparacie ZooMAb mogą mieć wygląd półstały (żel przypominający kulki) po liofilizacji. Jest to zjawisko normalne. Należy postępować zgodnie z zalecaną procedurą rekonstytucji zawartą w arkuszu danych, aby rozpuścić półstały, przypominający kulki materiał o wyglądzie żelu. Otrzymany roztwór przeciwciała jest całkowicie stabilny i funkcjonalny, co potwierdzają pełne testy funkcjonalne. Nie zawiera biocydów ani konserwantów, takich jak azydek, ani żadnych produktów ubocznych pochodzenia zwierzęcego. Większe opakowania są dostarczane jako wielokrotności 25 µL.
Przechowywanie i stabilność
Zaleca się przechowywanie liofilizowanego produktu w temperaturze 2-8°C. Przed rekonstytucją fiolki należy krótko mikrowirować, aby odwirować materiał na dno fiolki. Każdą fiolkę należy odtworzyć, dodając 25 µl przefiltrowanej wody laboratoryjnej lub PBS. Odtworzone przeciwciała można przechowywać w temperaturze 2-8°C lub -20°C w celu długotrwałego przechowywania. Unikać wielokrotnego zamrażania.
Inne uwagi
Stężenie: Stężenie specyficzne dla danej partii można znaleźć w certyfikacie analizy.
Informacje prawne
ZooMAb is a registered trademark of Merck KGaA, Darmstadt, Germany
Oświadczenie o zrzeczeniu się odpowiedzialności
O ile nie określono inaczej w naszym katalogu lub innej dokumentacji firmy dołączonej do produktu(-ów), nasze produkty są przeznaczone wyłącznie do użytku badawczego i nie mogą być wykorzystywane do żadnych innych celów, w tym między innymi do nieautoryzowanych zastosowań komercyjnych, zastosowań diagnostycznych in vitro, zastosowań terapeutycznych ex vivo lub in vivo lub jakiegokolwiek rodzaju konsumpcji lub zastosowania u ludzi lub zwierząt.
Ta strona może zawierać tekst przetłumaczony maszynowo.