Opis ogólny
Jesteśmy zaangażowani w dostarczanie bardziej ekologicznych produktów alternatywnych, które są zgodne z co najmniej jedną z 12 zasad zielonej chemii. To przeciwciało nie zawiera konserwantów, jest produkowane bez szkody dla zwierząt i wyjątkowo stabilne, aby umożliwić wysyłkę i przechowywanie w razie potrzeby, a tym samym jest zgodne z "Zapobieganiem powstawaniu odpadów", "Projektowaniem bezpieczniejszych chemikaliów" i "Projektowaniem pod kątem efektywności energetycznej".
Kliknij tutaj, aby uzyskać więcej informacji.
Przeciwciała 10889 reprezentują całkowicie nową generację rekombinowanych przeciwciał monoklonalnych. Każde przeciwciało 10889 jest wytwarzane przy użyciu naszego zastrzeżonego rekombinowanego systemu ekspresji, oczyszczane do jednorodności i precyzyjnie dozowane w celu uzyskania solidnej i wysoce powtarzalnej spójności między partiami. Do użytku badaczy udostępniane są wyłącznie klony o najwyższej wydajności. Każde przeciwciało jest walidowane pod kątem wysokiej swoistości i powinowactwa w wielu zastosowaniach, w tym w najczęściej używanym zastosowaniu. Przeciwciała 10889 są niezawodnie dostępne i gotowe do wysyłki, gdy są potrzebne.
Specyficzność
Klon 133-1H to rekombinowane mysie przeciwciało monoklonalne 10889, które specyficznie wykrywa glikoproteinę fuzyjną F0 w ludzkim syncytialnym wirusie oddechowym.
Immunogen
Ludzki syncytialny wirus oddechowy typu A (szczep A2).
Zastosowanie
Testy kontroli jakości
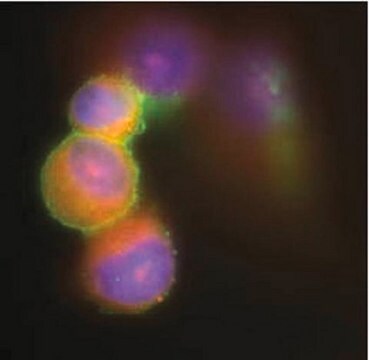
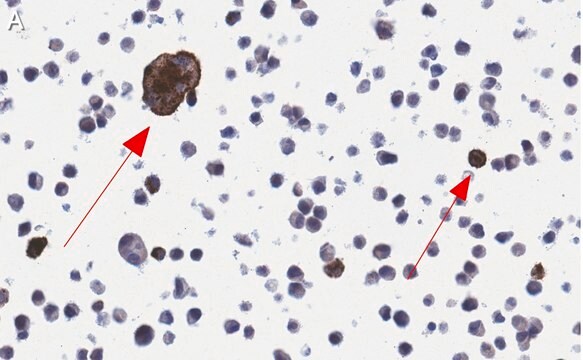
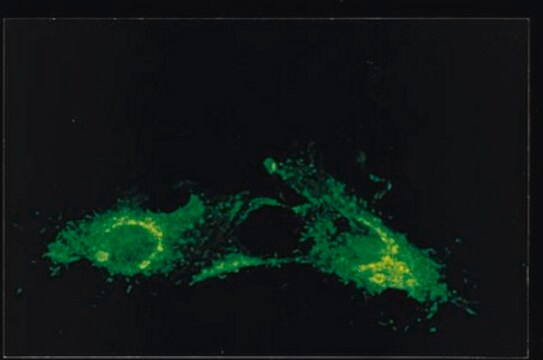
Ocena immunocytochemiczna w komórkach HEp-2 zakażonych RSV.
Analiza immunocytochemiczna: Rozcieńczenie 1:100 tego przeciwciała wykryło RSV w komórkach HEp-2 zakażonych ludzkim syncytialnym wirusem oddechowym (RSV).
Testowane aplikacje
Analiza immunoenzymatyczna (ELISA): Seryjne rozcieńczenia tego przeciwciała wykryły RSV oczyszczony z komórek VERO zakażonych ludzkim syncytialnym wirusem oddechowym.
Test wiązania powinowactwa: Reprezentatywna partia tego przeciwciała wiązała RSV z KD wynoszącym 1,2 x 10-6 w teście wiązania powinowactwa.
Uwaga: Rzeczywiste optymalne rozcieńczenia robocze muszą być określone przez użytkownika końcowego jako próbki, a warunki eksperymentalne mogą się różnić w zależności od użytkownika końcowego
Oceniane metodą immunocytochemii w komórkach HEp-2 zakażonych RSV.
Analiza immunocytochemiczna: Rozcieńczenie 1:100 tego przeciwciała wykryło RSV w komórkach HEp-2 zakażonych ludzkim syncytialnym wirusem oddechowym (RSV).
Opis wartości docelowych
Glikoproteina fuzyjna F0 (UniProt: P03420) jest kodowana przez gen F (Gene ID: 1494475) w ludzkim syncytialnym wirusie oddechowym A (szczep A2). Ludzki syncytialny wirus oddechowy (hRSV) jest pneumowirusem, który powoduje poważne choroby układu oddechowego u wcześniaków i noworodków urodzonych o czasie. Glikoproteina fuzyjna F0 wirusa RSV jest syntetyzowana z peptydem sygnałowym (aa 1-15), który jest następnie odcinany. Nieaktywny prekursor F0 jest następnie rozszczepiany w dwóch miejscach (aa 109-110 i 136-137) przez proteazę podobną do furyny, dając początek dojrzałym glikoproteinom fuzyjnym F1 i F2. Glikoproteina fuzyjna F1 jest jednoprzebiegowym białkiem błonowym typu I, które może istnieć jako homotrimer lub może tworzyć heterodimer połączony disiarczkiem z glikoproteiną fuzyjną F2. Jego N-koniec ma hydrofobowy peptyd fuzyjny, który wstawia się do docelowej błony gospodarza. Jest on zakopany w środku wnęki trimeru przed rozszczepieniem przez furynę gospodarza. Fuzja glikoproteiny F2 jest głównym czynnikiem determinującym swoistość gatunkową zakażenia RSV. Białko fuzyjne może istnieć w co najmniej 3 stanach konformacyjnych: stan natywny przed fuzją, stan pośredni przed spinką do włosów i stan spinki do włosów po fuzji. Podczas fuzji wirusa z błoną komórki plazmatycznej, zwinięte regiony cewki przyjmują strukturę trimeru spinki do włosów, pozycjonując peptyd fuzyjny w pobliżu C-końcowego regionu ektodomeny. Fuzja ta jest niezależna od pH i zachodzi w błonie plazmatycznej lub endosomalnej. Białko fuzyjne jest zaangażowane w wejście do komórki gospodarza poprzez interakcję z IGF-R1 gospodarza. Interakcja ta aktywuje kinazę białkową Z, która rekrutuje NCL/nukleolinę gospodarza na wierzchołkową powierzchnię komórki, gdzie może wiązać glikoproteinę fuzyjną F1. W późniejszym etapie infekcji białko fuzyjne wyrażane na błonie plazmatycznej zakażonych komórek może pośredniczyć w fuzji z sąsiednimi komórkami, tworząc syncytia, efekt cytopatyczny, który może prowadzić do martwicy tkanek. Białko fuzyjne może również wywoływać apoptozę zależną od p53 w komórkach. To rekombinowane przeciwciało monoklonalne ZooMAb10889, generowane przez naszą zastrzeżoną technologię, oferuje znacznie zwiększoną swoistość, powinowactwo, powtarzalność i stabilność w porównaniu z konwencjonalnymi przeciwciałami monoklonalnymi. (Ref.: McLellan, JS., et al. (2013). Science. 340(6136); 1113-1117; Olivier, A., et al. (2009). Int. J. Exp. Pathol. 90(4); 431-438; Schlender, J., et al. (2003). J. Virol. 77(8); 4609-4616).
Postać fizyczna
Oczyszczone rekombinowane mysie przeciwciało monoklonalne IgG, liofilizowane w PBS z 5% trehalozą, o normalnym wyglądzie gruboziarnistej lub półprzezroczystej żywicy. Składniki PBS/trehaloza w preparacie ZooMAb mogą mieć wygląd półstały (żel przypominający kulki) po liofilizacji. Jest to zjawisko normalne. Należy postępować zgodnie z zalecaną procedurą rekonstytucji zawartą w arkuszu danych, aby rozpuścić półstały, przypominający kulki materiał o wyglądzie żelu. Otrzymany roztwór przeciwciała jest całkowicie stabilny i funkcjonalny, co potwierdzają pełne testy funkcjonalne. Nie zawiera biocydów ani konserwantów, takich jak azydek, ani żadnych produktów ubocznych pochodzenia zwierzęcego. Większe opakowania są dostarczane jako wielokrotności 25 μL.
Przechowywanie i stabilność
Zaleca się przechowywanie liofilizowanego produktu w temperaturze 2-8°C. Przed rekonstytucją fiolki należy krótko mikrowirować, aby odwirować materiał na dno fiolki. Każdą fiolkę należy odtworzyć, dodając 25 μl przefiltrowanej wody laboratoryjnej lub PBS. Odtworzone przeciwciała można przechowywać w temperaturze 2-8°C lub -20°C w celu długotrwałego przechowywania. Unikać wielokrotnego zamrażania.
Informacje prawne
ZooMAb is a registered trademark of Merck KGaA, Darmstadt, Germany
Oświadczenie o zrzeczeniu się odpowiedzialności
O ile nie określono inaczej w naszym katalogu lub innej dokumentacji firmy dołączonej do produktu(-ów), nasze produkty są przeznaczone wyłącznie do użytku badawczego i nie mogą być wykorzystywane do żadnych innych celów, w tym między innymi do nieautoryzowanych zastosowań komercyjnych, zastosowań diagnostycznych in vitro, zastosowań terapeutycznych ex vivo lub in vivo lub jakiegokolwiek rodzaju konsumpcji lub zastosowania u ludzi lub zwierząt.
Ta strona może zawierać tekst przetłumaczony maszynowo.