近接依存性標識の新手法
生体分子同士がどのように相互作用しているかを理解することは、基礎生物学への新しい知見、新しい治療法の発見につながることが期待されます。一方で、従来手法でこれらの重要な相互作用を特定することは非常に困難でした。
最近、これらの相互作用解明に向けた、近接依存性標識法の開発が進んでいます。ここでは、外部刺激によって触媒的に活性種を生成する「アンテナ」を、目的の生体分子に付加しています。発生した活性種は「アンテナ」近くの生体分子に標識化し分析することで、相互作用するタンパク質(または核酸)のリストが得られ、「アンテナ」への近接度または距離を確認することができます(図1)。
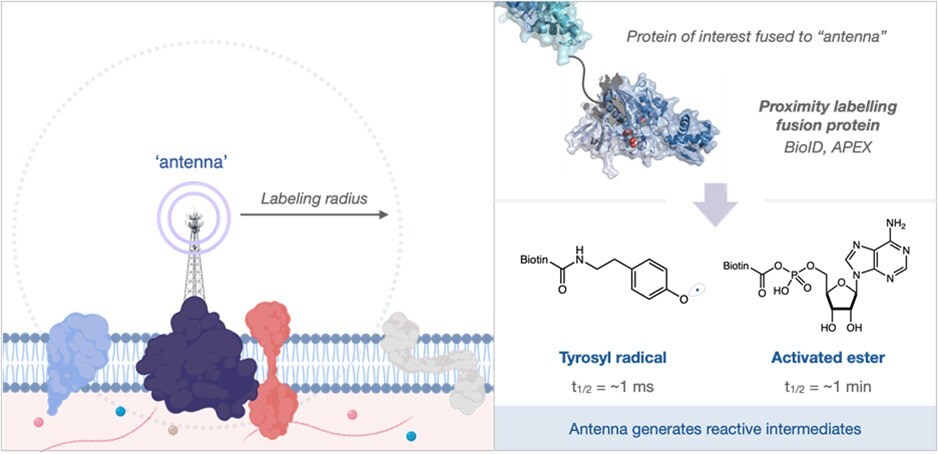
図1.(左図)「アンテナ」により近接した生体分子を標識(右図)標的タンパク質を「アンテナ」と結合させることで、反応性中間体を生成
細胞表面における近接性標識の課題
近年、適した「アンテナ」や反応中間体に関する研究は進んでいる一方で、多くは調整されたビオチンリガーゼやペルオキシダーゼ酵素に基づいています。これらの手法では、ビオチンと過酸化水素の添加によって活性化されたエステルおよびフェノキシラジカル中間体をそれぞれ生成します(図1, 右)。この反応中間体は、溶液中での半減期が1ミリ秒から1分程度であり、細胞内の混雑した環境では自由拡散が制限され生体分子と速やかに反応し標識化が進行します。一方で細胞内に比較して混雑していない細胞外では、半減期が長いことから標識半径が大きくなり標識精度が落ちてしまうことが問題となっていました(図2)。このことは、偽陽性の検証が頻繁に必要となり研究リソースが奪われてしまう問題にもなります。
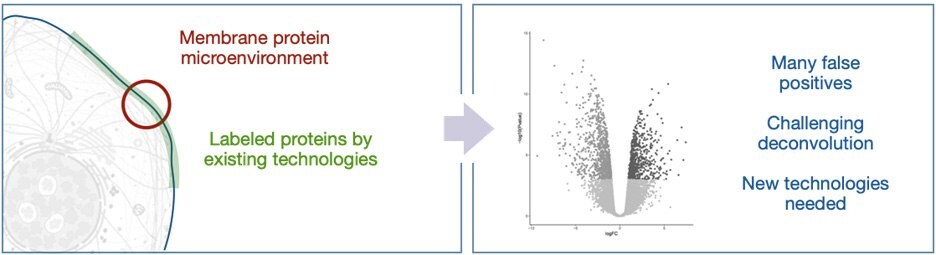
図2.このように現在の近接依存標識手法では、細胞外空間において特に多くの偽陽性を引き起こす可能性があるのです。
高解像度の近接依存標識:ATLASμMapキット
近年、プリンストン大学のMacMillan教授のグループとメルクの研究者が共同で、これらの問題を解決する方法を開発しました。新しい手法では、溶液半減期が著しく短いカルベン反応性中間体を活用することで、より解像度の高い標識プラットフォーム開発を考えました。カルベン活性種は、光活性化するイリジウム触媒により、アリールジアジリンから触媒的に生成します。このイリジウム触媒を抗体に結合させることで、膜タンパク質近傍の微小環境における局所的な標識化が可能になります(図3A)。
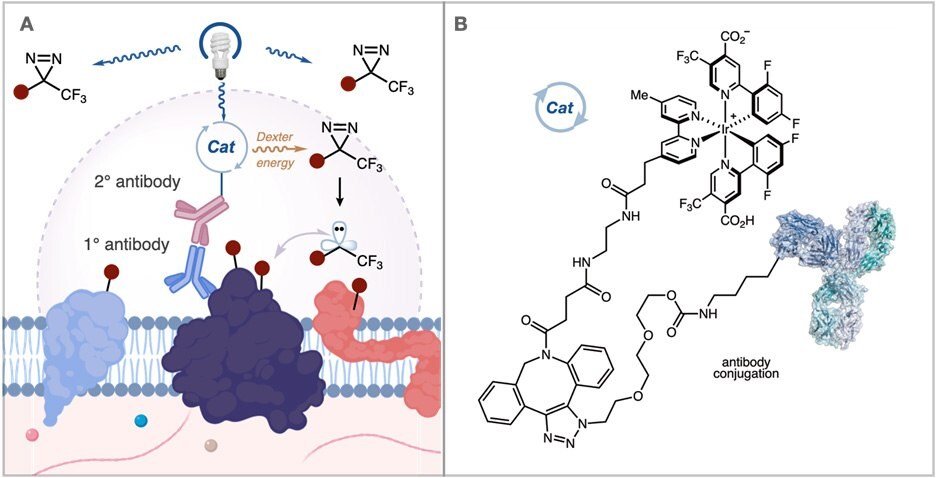
図3(A)抗体に結合したイリジウム触媒を活性化すると、半減期の短いカルベン反応中間体が生成され、細胞外空間で近接標識が可能(B)ATLASキットは、イリジウム触媒を目的の抗体に結合させる方法を提供
特長
- 目的とする抗体への組み込みが容易
- 短い標識半径
- 可視光による簡易な活性化手法
- 短い半減期による高い時間分解能
- あらゆる膜タンパク近傍の微小環境を高精度で研究
参考文献
続きを確認するには、ログインするか、新規登録が必要です。
アカウントをお持ちではありませんか?