高塩濃度細胞溶解と耐塩性エンドヌクレアーゼを用いたAAVベクターのプロセス強化
アデノ随伴ウイルス(AAV)ベクターの製造では、細胞溶解とヌクレアーゼ処理が併用される中間ステップがあります。このステップでは、界面活性剤を用いて細胞の脂質二重層を破壊してベクターを取り出し、エンドヌクレアーゼ により宿主細胞DNAと残りのプラスミドを分解して患者さんの安全性を確保し、ダウンストリームのプロセス効率を高めます。残留DNAは必ず投与量当たり10 ng未満まで減らさなければなりません。またフラグメントサイズについては、2020年のFDAによる遺伝子治療のIND(新薬臨床試験開始)申請に関するガイドラインで推奨されるように、必ず約200塩基対未満になっていなければなりません。
このページでは、細胞溶解に関する主な検討事項、そしてベクターの力価と感染価を高めるために高塩濃度と耐塩性エンドヌクレアーゼをどう使えるかについて説明します。
細胞溶解に関する検討事項
単純なように見えますが、細胞溶解ステップにはいくつかの課題が伴います。細胞溶解で広く使用されているTRITON™ X-100(4-tert-octylphenol polyethoxylate)などの界面活性剤は問題があります。2021年1月現在、TRITON™ X-100は、REACH(化学物質の登録、評価、認可、および制限)リストに追加されたため、その無認可使用が欧州委員会により欧州連合内で禁止されています。EU内での使用に関連する厳格なガイドラインに加えて、このリストへ追加された理由は、TRITON™ X-100の分解産物に内分泌かく乱効果と変異原性があるためで、患者さんと環境に対して危険であると判断されました。
細胞溶解用の界面活性剤を選択する際に考慮すべきその他の事項としては、ウイルスベクターとウイルス粒子の感染性を損なわないこと、ならびにダウンストリームプロセスを妨げないことがあり、後者はポリソルベートの使用により生じます。また、選ばれる界面活性剤は、後続のワークフローステップにおける除去と検出も簡単にできなければなりません。
最後に、細胞溶解とベクター収率に対する塩濃度の影響を理解することが大切です。歴史的に、AAVカプシドの放出に使用される溶解バッファーは、生理的塩濃度(150 mM NaCl)を含有していました。しかしながら最近の論文では、塩濃度を500 mMまで上げることで、ベクター粒子数が増え、感染価が高まり、AAVの凝集が抑えられることが報告されています。ただし、以下に述べるように、高塩濃度は、AAVベクター製造プロセスでDNA分解に使用される従来のエンドヌクレアーゼの活性に悪影響を及ぼします。
AAV収率に対する中間ステップの高塩濃度の影響
細胞溶解において塩濃度を上昇させた際の影響を明らかにするための試験を実施しました。AAV5ベクターをHEK293細胞で産生させ、TRITON™ X-100、ポリソルベート20、Deviron® C16、またはDeviron® 13-S9のいずれかで細胞溶解しました。プロセスにより産生されたカプシドのベースライン数は、ポリソルベート20溶解バッファーで150 mM NaClを用いて測定しました。溶解バッファーで500 mMの塩を使用した結果、AAV5カプシド力価は平均29%増加しました(図1)。

図1AAV5力価の産生に対する高塩濃度溶解の影響
AAV感染価に対する中間ステップの高塩濃度の影響
AAV感染価に対する500 mM NaCl条件の影響を測定するため、AAV2ベクターをHEK293細胞で産生させる同様の試験を実施しました。ベースラインの溶解バッファー条件は、150 mM NaClおよびポリソルベート20でした。塩濃度を500 mMまで高め、さまざまな界面活性剤を使用したとき、少なくとも10倍の感染価上昇が認められました(図2)。上で述べたように、溶解で高塩濃度を使用することのさらなる利点は、AAV凝集の抑制です。
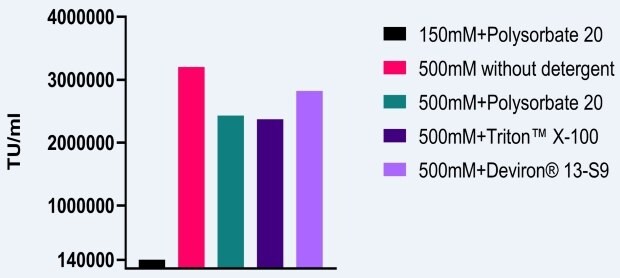
図2AAV5感染価に対する高塩濃度溶解の影響
DNA分解に関する検討事項
細胞溶解ステップと同じく、DNA分解ステップにもいくつかの課題が伴います。そのうち最も重要なのが、規制要件を満たし、サプライチェーンの堅牢性を確保するために適切な品質の材料を調達する必要性です。GMP準拠に加えて、純度、グリコシル化状態、およびバイオバーデンも検討すべき要素です。高塩濃度に対する酵素の耐性も、AAV製造において高塩濃度の使用を妨げている重要な要素となっています。
AAV製造の酵素選択のための主な判断基準
- IPEC PQG GMPまたはそれと同等、FDA DMF/BBMF
- 純度99%超の製品
- 翻訳後修飾なし
- マイコプラズマ試験
- 外来性ウイルス試験
- エンドトキシンン試験
- テールゲートサンプル(少量サンプル)の利用可能性
- 強力な物流体制と供給の安定性
- アプリケーション関連の質問に対するテクニカルサポート
- 精密検出方法
DNA分解で使用される酵素は、ダウンストリームプロセスで必ず効果的に除去されなければならないものでもあり、プロセスで使用される塩濃度におけるその活性を必ず考慮しなければなりません。塩濃度を高めるとベクター収率は高まりますが、従来のエンドヌクレアーゼ酵素とDNAとの間の相互作用はイオン強度が高いと生じないため、核酸の切断が妨げられることになります。つまり、歴史的に、目的のヌクレアーゼ活性と塩濃度とのバランスを適切にする必要があったのです。
AAVベクター製造用耐塩性エンドヌクレアーゼの開発
細胞溶解に適した高塩濃度において効率的な活性を持つエンドヌクレアーゼの必要性に対処するため、タンパク質工学の高度な能力を駆使してBenzonase® 耐塩性エンドヌクレアーゼを開発しました。この非動物由来エンドヌクレアーゼは、1000 mMまでの塩濃度においてDNAとRNAを分解することができ、IPEC-PQG GMP準拠製品およびEmprove® Expert製品として発売されています。
細菌発現系を使用してBenzonase® 耐塩性エンドヌクレアーゼを産生していますが、これは分子サイズが正確に規定され、翻訳後修飾がなく、高いバッチ間再現性が得られるからです。以下のデータは、Benzonase® 耐塩性エンドヌクレアーゼの活性と利点を実証しています。
タンパク質プロファイル
細菌発現系を使用してBenzonase® 耐塩性エンドヌクレアーゼを産生していますが、これは分子サイズが正確に規定され、翻訳後修飾がなく、高いバッチ間再現性が得られるからです。タンパク質プロファイルが均一であるため、イムノアッセイ(ELISAなど)による正確な検出が可能です。これは、高度にグリコシル化されて翻訳後バッチ間のばらつきが大きな酵母発現系の酵素とは異なります。

図3還元SDS-PAGEによるBenzonase® 耐塩性エンドヌクレアーゼの同定および競合製品Aとの比較。

図4非還元SDS-PAGEによるBenzonase® 耐塩性エンドヌクレアーゼの同定および競合製品Aとの比較。
Benzonase® Salt Tolerant endonuclease Emprove® Expertの大腸菌で産生された酵素の特長
- クリーンで高純度なタンパク質
- 翻訳後修飾なし
- 高いバッチ間再現性
図3と図4の結果から、Benzonase® Salt Tolerant endonuclease Emprove® Expertは正確に規定された分子サイズを持つことが分かります。評価基準として使用した高塩濃度で活性を持つエンドヌクレアーゼ(競合製品A)はそうではありません。
エンドヌクレアーゼ活性
エンドヌクレアーゼが活性を発揮するにはマグネシウムが必要です。図5は、Benzonase® 耐塩性エンドヌクレアーゼと非耐塩性エンドヌクレアーゼの活性をさまざまなマグネシウム濃度で比較したものです。Benzonase® 耐塩性エンドヌクレアーゼの活性は、高塩濃度で高まり、1~10 mMの範囲のMg2+ と塩濃度500 mMで安定していました。塩濃度150 mMと500 mMでは、Benzonase® 耐塩性エンドヌクレアーゼの活性は、10 mM Mg2+ を用いた場合の非耐塩性エンドヌクレアーゼの活性と同等でした(図6)。
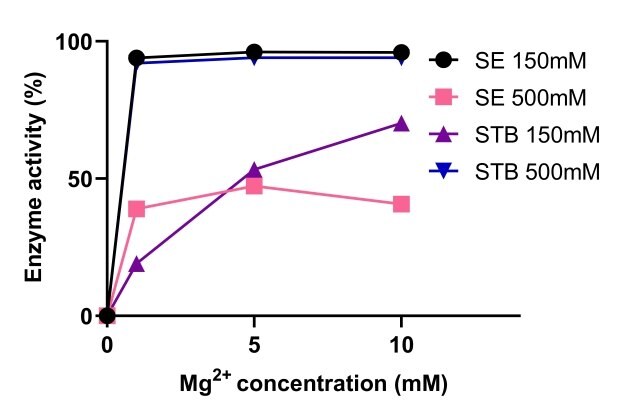
図5Benzonase® 耐塩性エンドヌクレアーゼと非耐塩性エンドヌクレアーゼの活性比較。
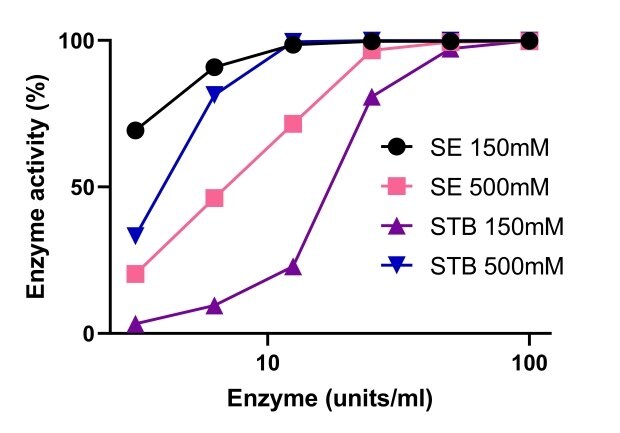
図6Benzonase® 耐塩性エンドヌクレアーゼと非耐塩性エンドヌクレアーゼの活性比較。
図7は、DNAをBenzonase® 耐塩性エンドヌクレアーゼと市販の耐塩性/非耐塩性エンドヌクレアーゼを用いて500 mMと1 MのNaClにおいて37°Cで1時間分解した試験の結果を示しています。Benzonase® 耐塩性エンドヌクレアーゼは、500 mMと1 Mの塩濃度でDNAを完全に分解し、市販エンドヌクレアーゼと同等またはより高い性能を発揮しました。

図7Benzonase® 耐塩性エンドヌクレアーゼと市販の耐塩性/非耐塩性エンドヌクレアーゼによる37°C、1時間のDNA分解の比較。
凡例
M – GeneRuler Ultra Low Range DNAラダー(カタログ番号SM1213)
競合製品A ** – 耐塩性エンドヌクレアーゼ競合製品
SE – Standard(非耐塩性)エンドヌクレアーゼ(カタログ番号103773など)
STB – Benzonase® 耐塩性エンドヌクレアーゼEmprove® Expert
核酸フラグメントサイズ
Benzonase® 耐塩性エンドヌクレアーゼは、DNAを10塩基対より小さなサイズの検出不可能なレベルまで分解します。図8は、低分子量DNAマーカーを用いて4%アガロースゲルで分析したDNAフラグメントを示しています。150 mMの塩濃度ではDNAは完全には分解されておらず、500 mMの塩濃度では分解後にDNAフラグメントは残っていませんでした。

図837°Cで30分間の25 U/mLのBenzonase® 耐塩性エンドヌクレアーゼによる分解後にサイズ分離されたDNAフラグメント
AAVベクター製造におけるBenzonase® 耐塩性エンドヌクレアーゼの界面活性剤との適合性
Benzonase® 耐塩性エンドヌクレアーゼの活性は、細胞溶解のために使用される4種類の界面活性剤との併用において評価しました。TRITON™ X-100、ポリソルベート20、およびTRITON™ X-100の使用禁止を受けて開発された2種類の界面活性剤代替品(Deviron® C16および13-S9)。図9に示すように、Benzonase® 耐塩性エンドヌクレアーゼは、4種類の界面活性剤のいずれにも影響を受けませんでした。DNAは、TRITON™ X-100、ポリソルベート20、およびDeviron® 13-S9(7B)の存在下で500 mM NaCl含有溶解バッファーにおいて完全に分解されました。
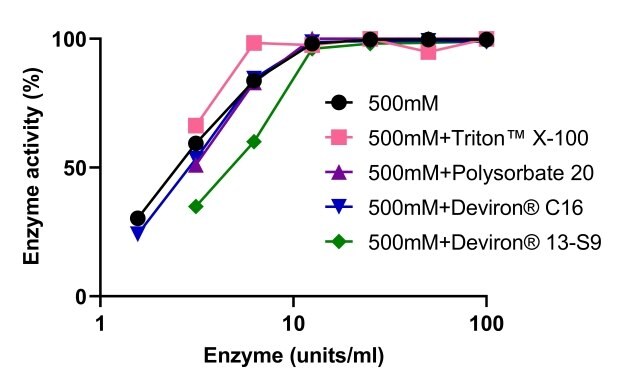
図9さまざまな界面活性剤と併用したBenzonase® 耐塩性エンドヌクレアーゼの活性

図10さまざまな界面活性剤と併用したBenzonase® 耐塩性エンドヌクレアーゼによるDNA分解。
アプリケーションに適したBenzonase® の選択
Benzonase® 耐塩性エンドヌクレアーゼは、塩濃度が200 mM以上になるアプリケーションで使用する必要があります。塩濃度が500 mMの場合、DNAは完全に分解され、上で示すようにAAV力価の29%の増加と2,000%近い感染価を達成することが可能です。AAVの凝集が妨げられ、ウイルスカプシドからDNAが確実に効果的に除去されるため、この中間ステップで高塩濃度条件を用いて、患者さんの安全性を高めます。またBenzonase® 耐塩性エンドヌクレアーゼの翻訳後プロファイルにより、医薬品製造においてグリコシル化されていない検出しやすいタンパク質を確実に使用することができます。
塩濃度が200 mM未満のアプリケーションでは、Benzonase® Safety Plus非耐塩性エンドヌクレアーゼをお使いください。
表3は、メルクの3種類のGMP Benzonase® エンドヌクレアーゼ標準品の仕様の要約です。Benzonase® 耐塩性エンドヌクレアーゼは、製造業者が開発から製造に移る際の混乱を最小限に抑え、徹底的なリスクアセスメントを実施できるようにするEmprove® プログラムの一部です。このプログラムでは、業界をリードする基準に従って厳密に適格性が評価された原材料や出発物質を提供します。このプログラムの材料は、原材料の適格性評価、リスクアセスメントの実施、製造プロセスの最適化の際の医薬品製造業者の情報ニーズを満たす包括的文書パッケージにより裏付けられています。
高塩濃度に伴う課題の解決
AAV製造の細胞溶解ステップで高塩濃度を使用することで、力価と感染価を高めることができます。ただし、高塩濃度条件ではDNA分解で使用する従来のエンドヌクレアーゼの活性が阻害されてしまうため、このアプローチの利用は歴史的に実用的ではありませんでした。
Benzonase® 耐塩性エンドヌクレアーゼの登場により、細胞溶解とDNA分解という中間ステップにおいて500 mM程度の塩濃度を利用することができるようになりました。このエンドヌクレアーゼは、TRITON™ X-100の代替品であるDeviron® 界面活性剤など検査済みのすべての界面活性剤と併用できます。
Benzonase® 耐塩性エンドヌクレアーゼ または Deviron® ポートフォリオ製品のいずれかのサンプルをご希望のお客様は、下のリンクをクリックして簡単なウェブフォームにご記入ください。
Benzonase® のよくある質問
定義
Benzonase® エンドヌクレアーゼとは?
Benzonase® エンドヌクレアーゼは、研究やバイオプロセシングで使用されるエンドヌクレアーゼに付けられたMerckが所有する商品名です。
この商品名が付いている酵素にはどのようなものがありますか?
Benzonase® ヌクレアーゼファミリーには、現在2種類の酵素が含まれています。
- セラチア菌から単離され、大腸菌K12(W3110株)で組み換え生産されたBenzonase® endonuclease Safety Plusなどの従来のBenzonase® エンドヌクレアーゼ製品ライン。このタンパク質の分子量は30 kDaで、等電点(PI)は6.85です。
- 新しいBenzonase® 耐塩性エンドヌクレアーゼ(1.4445)。最先端のタンパク質工学を用いて設計されており、高塩濃度で高い活性を発揮できるようになっています。
このタンパク質の分子量は約27 kDaで、PIはpH 9.68です。このよくある質問専用セクションでは、この酵素に特化した説明をご覧いただけます。
作用機序
Benzonase®ヌクレアーゼはどの種類の核酸に作用しますか? RNAの単離に使用できますか?
Benzonase®ヌクレアーゼはあらゆる形態のDNAとRNA(一本鎖、二本鎖、線状および環状)に作用し分解する非選択性エンドヌクレアーゼです。
Benzonase®ヌクレアーゼによる核酸分解が完全に進むと最終的にどうなりますか?
Benzonase®ヌクレアーゼは、末端が5'-モノリン酸で長さが2~5塩基のオリゴヌクレオチドにまで核酸を徹底的に分解します。
不活化と除去
どうすればBenzonase®ヌクレアーゼを不活化できますか? どうすれば除去できますか?
EDTAを使用して必須金属イオンをキレートすれば可逆的な阻害が可能です。不可逆的失活は、極端な条件(70°Cの100 mM NaOHに30分間)でなければ達成できません。クロマトグラフィーを使用すれば、Benzonase®を目的産物から分離できます。ただし、本エンドヌクレアーゼは丈夫であることから、ヌクレアーゼを含まない最終産物が求められる場合、Benzonase®の使用は推奨しません。
Benzonase® エンドヌクレアーゼが働かないのはなぜですか?活性を低下させるものは何ですか?
Benzonase® ヌクレアーゼは、幅広い使用条件下で活性を発揮します(酵素特性セクションを参照)。ただし、Benzonase® エンドヌクレアーゼの活性には1~2 mMのMg2+が必要です。
Mg2+の代わりにMn2+を使用することもできますが、この酵素はMg2+の存在下でのみ最適な活性を発揮できます。300 mMを超える1価陽イオン濃度、100 mMを超えるリン酸濃度、100 mMを超える硫酸アンモニウム濃度によりその活性は約50%阻害されます。また、1 mMを超える濃度のEDTAでもBenzonase® エンドヌクレアーゼ活性は阻害されます。
活性が低下しています。なぜですか?
Benzonase® エンドヌクレアーゼは通常、非常に安定です。ただし、まれに活性低下が確認されます。考えられる原因はいくつかあります。不可逆的不活化は、サンプルに含まれるプロテアーゼなどの変性剤の存在や不適切な保管によるものです。可逆的不活化は、一般に、必要なマグネシウムイオンを除去してしまうEDTAなどのキレート剤の存在が原因です。
バイオプロセシングテンプレートのBenzonase® エンドヌクレアーゼはどのように除去できますか?
Benzonase® エンドヌクレアーゼの除去は、ダウンストリームにおけるいくつかの単位操作で達成できます。例えば、清澄化用デプスフィルターによるろ過、濃縮・ダイアフィルトレーション用タンジェンシャルフローフィルトレーション(TFF)、クロマトグラフィー(IEX、SEC、HIC)などです。詳細については、付録第2章「Benzonase® エンドヌクレアーゼの除去」(36ページ)を参照してください。
安定性と操作条件
使用しているBenzonase® エンドヌクレアーゼを実験台に出しっぱなしにしてしまいました。問題はありませんか?
Benzonase® エンドクレアーゼについて広範囲の安定性試験を実施しており、きわめて安定的であることを確認しています。37℃で長期培養しても、Benzonase®ヌクレアーゼは90%を超える活性を数か月間維持していました。
別のバッファーを使用しようと考えています。Benzonase®エンドヌクレアーゼの活性を十分に得るためには、どのような条件が絶対に必要ですか? 活性を低下させるものは何ですか?
Benzonase® エンドヌクレアーゼが活性を発揮するには1~2 mMのMg2+が必要です。50%を超える1価陽イオン濃度、20 mMを超えるリン酸濃度、および25 mMを超える硫酸アンモニウム濃度によりBenzonase®の活性は約50%阻害されます。
低温で反応させる場合、どのくらいBenzonase® エンドヌクレアーゼを追加する必要がありますか?
Benzonase® エンドヌクレアーゼが活性を発揮するには1~2 mMのMg2+が必要です。50%を超える1価陽イオン濃度、20 mMを超えるリン酸濃度、および25 mMを超える硫酸アンモニウム濃度によりBenzonase®の活性は約50%阻害されます。
タンパク質抽出アプリケーション
Benzonase® エンドヌクレアーゼは、プロテアーゼ阻害剤カクテルと併用できますか?
はい。ただし、多くのプロテアーゼ阻害剤カクテルにはEDTAが含まれているため注意を要します。1 mMを超える濃度のEDTAは、Benzonase® エンドヌクレアーゼの活性を阻害します。
目的タンパク質が不溶性のため、変性条件下で精製を行う必要があります。Benzonase® エンドヌクレアーゼは尿素中でも作用しますか?
尿素濃度が6 MまでであればBenzonase®ヌクレアーゼ活性は上昇します。6 M尿素では、酵素活性は最初は上昇しますが、時間が経つにつれて低下します。7 M尿素では、15分後にBenzonase®エンドヌクレアーゼは変性し、活性が失われます。しかし、失活する前にかなりの核酸が分解されます。Benzonase®エンドヌクレアーゼの初期濃度を高くすることで、7 M尿素の影響を一部補うことができます。
多種類のBenzonase®エンドヌクレアーゼが提供されているのはなぜですか? HCの意味は何ですか? 純度90%と99%の2種類の製品が用意されている理由は?
できる限り幅広い処理条件やコスト要件に合うように、2つの異なる純度グレードのBenzonase®エンドヌクレアーゼをご用意しています。(純度グレードI(99%超)、純度グレードII(90%超))いずれのグレードも、25 U/μLと高濃度(HC)の250 U/μLがあります。大量購入については、テクニカルサービスにご相談ください。
Benzonase® 製品の全リストと製品間の相違点については、メルクのエンドヌクレアーゼページをご覧ください。
Benzonase®エンドヌクレアーゼによる核酸分解が完全に進むと最終的にどうなりますか?
Benzonase®エンドヌクレアーゼは、末端が5'-モノリン酸で長さが2~5塩基のオリゴヌクレオチドにまで核酸を徹底的に分解します。
バイオ製造アプリケーション
特定のアプリケーションには、どの品質/サイズのBenzonase® エンドヌクレアーゼが適していますか?
Benzonase® エンドヌクレアーゼの活性に影響を及ぼすパラメータはいくつかあります。そのため、最適条件はプロセスにより異なり、実験により明らかにしていく必要があります。粘度低下のためには、Benzonase® エンドヌクレアーゼ、純度グレードII(≥ 90%)で十分なことが多いでしょう。標準的なアッセイ条件下において、1ユニットのBenzonase® エンドヌクレアーゼは、30分以内に37 µgのDNAを完全に分解するのに必要な酵素量にほぼ相当します。
プロセスのどのステップでBenzonase® エンドヌクレアーゼを添加する必要がありますか?
この質問への答えは、Benzonase® エンドヌクレアーゼを使用してる目的により異なります。例示しているアプリケーションがこの質問に答える役に立てばと思います。ただし、原則として、Benzonase® エンドヌクレアーゼは通常、培養後、キャプチャステップ前に添加するのが最適です。
Benzonase® エンドヌクレアーゼは安全ですか?
安全です。Benzonase® エンドヌクレアーゼの毒性試験が実施されています(社内報告書あり)。マウスとラットにおいて1回投与後の全身毒性が調べられました。非常に高用量であっても毒性作用は認められませんでした。また、非常に高用量のBenzonase® エンドヌクレアーゼを静脈内投与されたマウスでも潜在的変異原性は確認されませんでした。
500万ユニットチューブの充填量範囲が明記されていないのはなぜですか?
Benzonase® エンドヌクレアーゼの活性(U/mL)は、製品ロット間でばらつきがある可能性があるため、チューブあたりの量ではなくユニット数を明記することにしています。チューブあたりの量は、分析証明書(CoA)の活性情報から簡単に算出できます。
BENZONASE® 耐塩性エンドヌクレアーゼ
配列は、Benzonase® Safety Plusなどの従来のBenzonase® 製品と似ていますか?
Benzonase® 耐塩性エンドヌクレアーゼは、高塩濃度でも高い活性を維持できるように最先端のタンパク質工学により設計された全く新しい酵素です。他の従来のBenzonase® 製品とは異なるアミノ酸配列です。
従来のBenzonase® 製品との使用条件の違いは何ですか?
エンドヌクレアーゼとしては、Benzonase® 耐塩性エンドヌクレアーゼは、従来のBenzonase® 製品と同じ条件で効果を発揮します。例外は1価陽イオン濃度条件です。300 mM以上のNaClを推奨します。
この酵素はどうすれば阻害できますか?
この酵素は、EDTAの添加または加熱により阻害されます。
この酵素はどのように除去できますか?
上記の「バイオプロセシングテンプレートのBenzonase® エンドヌクレアーゼはどのように除去できますか?」をご覧ください。
微量のこの酵素はどのように検出できますか?
メルクの従来のBenzonase® 酵素については、Benzonase® 耐塩性エンドヌクレアーゼを確実に検出できるように専用ELISAキットをご用意しています。
他の非耐塩性ヌクレアーゼではなくなぜこの酵素を使用すべきなのですか?
市販のバイオプロセシング用非耐塩性ヌクレアーゼはすべて類似のアミノ酸配列に基づいています。つまり、それらの高塩濃度における核酸分解能は同等であり、最適ではないと判断されます。
1価陽イオン濃度の効果的な使用条件は、0~200 mMの範囲です。生物学的プロセスで認められる生理的塩濃度とほぼ同じです。
同時に、HEK細胞溶解で生理的塩濃度を上回る塩濃度を使用すると、全体的なプロセス収率に大きな影響を与えることが分かっています。500 mMのNaCl濃度では、感染価と全AAV回収率が、150 mMの塩濃度の場合より有意に高まります。
つまり、耐塩性エンドヌクレアーゼの使用は、このような高塩濃度条件で核酸を除去するために必要なのです。
200 mMを超える塩濃度でも普通のヌクレアーゼを使用できますか?
生理的塩濃度を超える濃度において普通のヌクレアーゼの活性は大幅に低下するため、酵素の追加が必要になり、医薬品精製プロセスが複雑になります。また、所有コストが高まり、プロセスのコスト効率低下にもつながります。そのため、耐塩性ヌクレアーゼの使用を推奨しています。
Benzonase® 耐塩性エンドヌクレアーゼを検出するために他のサプライヤーの検出キットを使用できますか?他の「高塩濃度耐性」ヌクレアーゼ専用のキットなどは使えますか?
Benzonase® 耐塩性エンドヌクレアーゼは、全く新しい酵素であるため、メルクの検出キット以外に検出できる市販の検出キットはありません。
注記:商品名「Benzonase®」が使用されていて、Merckの公式ルート以外で販売されている製品は、偽造品であると考えてください。
酵素産生では、なぜ発現宿主がそれほど重要なのですか?
タンパク質の発現は、複数の生産プラットフォームを用いて達成されます。酵素や細菌を用いる発現が最も一般的です。それでも得られる産物には類似性がなく、使用されるプラットフォームにより翻訳後修飾プロファイルが異なります。
酵母で発現したタンパク質は、高度にグリコシル化され、修飾されているため、製品を使用する際に、抗体アッセイでの検出精度の低下などさまざまな問題が発生します。
市販されている主な高塩濃度耐性エンドヌクレアーゼは、酵母で発現されています。
ヌクレアーゼの翻訳後修飾はなぜ検出精度や効率に影響を与えるのですか?
グリコシル化されたタンパク質では、(図2のように)不均一なプロファイルが認められ、バッチ間の再現性がありません。標準的な検出法ではイムノアッセイが用いられているため、目的のタンパク質を検出するために作られた抗体では、酵母発現で見られるあらゆる修飾に対処することができません。その結果、ELISAキットなどの抗体ベースの検出法の検出精度は低下します。
この酵素の毒性プロファイルは?
Benzonase® 耐塩性エンドヌクレアーゼは、他のBenzonase® 製品と同じ毒性プロファイルを有しています。
私のプロセスにとって最もコスト効率が高くなるヌクレアーゼを見つけるのを手伝ってもらえますか?全体的なプロセス効率と収率に留意したいです。
お客様の規制関連ニーズやプロセス条件ニーズを満たすヌクレアーゼ製品ポートフォリオをご用意しています。プロセス開発のために、メルクのMSAT(Manufacturing Science And Technology)サポートをお気軽にお申しつけください。メルクのエキスパートが、アップストリームから最終充填まですべての製造テンプレートでサポートいたします。
Deviron® のよくある質問
欧州連合外の場合、TRITON™ X-100を使用し続けることはできますか?
TRITON™ X-100の使用禁止は、REACH2 規制の下でECHA1 により決定されました。使用禁止を推し進めた主な理由は、人間の健康と環境に対する製品の高い毒性でした。したがって、バイオ製造からこの製品を排除することが、業界における最も注目されるトレンドの1つとなっています。EU以外の規制当局もこの製品の使用について評価していくため、さらなる使用禁止の拡大へとつながるでしょう。
バイオ製造ではなぜ研究グレードの界面活性剤を使用できないのですか?
一般に、界面活性剤は、有機化学連鎖反応を用いて大量に製造されます。多くの場合、製造コストを抑えるために、低品質の原材料が使用されます。そのため、ダイオキシンやニトロソアミンなど非常に危険な不純物が最終産物に含まれることがあります。研究グレードの界面活性剤は、洗浄アプリケーションにのみ使用され、製剤の周辺に存在していてはいけません。
Deviron®に切り替える主なステップは?
Deviron® ポートフォリオには、GMP準拠のEXCiPACT認定製造された製品の3つのバッチがあります。適格性評価用に、これらのバッチのサンプルをご用意しています。メルク製品に同梱されるEmprove® ドシエには、規制当局への申請で必要なすべての情報が含まれています。毒性情報もすぐにご利用いただけます。
Deviron® を試してみたいのですが、専門知識がありません。サポートしてもらえますか?
アプリケーション関連のサポートについては、バイオ製造エキスパートチームにお任せください。移行を円滑に進められるようサポートいたします。メルクの担当者にお問い合わせいただければ、無料サポートをお試しいただけます。
MQ400/Emprove® EvolveとMQ500/Emprove® Expert (GMP)は何が違うのですか?
お客様の承認申請をサポートするため、さまざまな文書と品質プログラムを作成して、アプリケーションに最適な製品を選んでいただけるようにしています。以下のリンクをクリックして、Emprove® プログラムと M-Clarity® プログラムの詳細をご覧ください。Deviron® C16 Emprove® EvolveおよびDeviron® 13-S9 Emprove® Expertは、メルクがご提供する最高品質レベルの製品ラインです。
目的のアプリケーションで推奨される濃度は?
ウイルス不活化の場合、現時点では、TRITON™ X-100で使用されるASTM3 E3042-16がいまだにモノクローナル抗体製造で使用されている文書です。業界で使用される濃度は、アプリケーションにより0.5~1%の範囲で異なります。
細胞溶解アプリケーションでは、幅広い濃度が使用されており、すべてプロセスごとに異なります。プロセス開発では、複数の濃度を並行して試してみることをおすすめします。メルクのDeviron® 界面活性剤は、少なくともTRITON™ X-100やポリソルベートと同等の効果を発揮します。
Deviron®についてGMP準拠の検出法を開発できますか?
メルクの研究開発エキスパートは、Deviron® ポートフォリオ用検出法を開発しており、お客様にご利用いただくことができます。ただし、GMP準拠の検出法については、メルクのBioreliance® ラボをパートナーとしてお選びください。ご質問がありましたら、お問い合わせください。
Deviron® ポートフォリオは、細胞溶解アプリケーションでBenzonase® と併用できますか?
Benzonase® は、AAV4プロセスにおけるDNA分解のためのゴールドスタンダードです。Deviron® ポートフォリオは、Benzonase® エンドヌクレアーゼと完全適合するように開発されました。これらの2つのポートフォリオを併用しても、酵素活性や界面活性剤性能の低下はありません。アプリケーションデータは、Deviron® ポートフォリオのカタログでご覧いただけます。
Deviron® ポートフォリオの生産施設は?
Deviron® ポートフォリオは、ドイツにあるメルクのダルムシュタットで生産されています。これまでに年間100トンを超える製品を送り出しています。お客様の計画を共有いただく形で、状況ごとのリードタイムについてお気軽にご相談ください。
1欧州化学機関
2Registration, Evaluation, Authorization and Restriction of Chemicals(化学物質の登録・評価・認可・制限)*
3American Standard for Test Method
4アデノ随伴ウイルス
TRITONは、Dow Chemical Company(「Dow」)またはDow関連会社の商標であり、許可を得て使用しています。
参考文献
お客様に提供される情報や助言につきましては可能な限り最善を尽くしておりますが、何らの義務または責任を負うものではありません。お客様は法律と規制を遵守してください。またこれは、第三者のあらゆる権利に関しても適用されます。当社提供の情報と助言は、当社製品の想定使用目的に対する適切性をお客様自身が確認する責任を解くものではありません。
続きを確認するには、ログインするか、新規登録が必要です。
アカウントをお持ちではありませんか?