不斉合成のための高効率的かつ高選択的な触媒:
[RhOH(S)-BINAP]2 (1)およびRh(I) 触媒前駆体
ロジウム触媒を用いてアリールボロン酸を炭素-炭素二重結合に不斉共役付加する反応が、京都大学の林らにより新たに開発されました。1Rh-BINAP触媒を用いることにより、他のエナンチオ選択的な1,4-付加反応に比べて、(1)高選択性(>95%ee)、(2)水溶液中で反応が可能、(3)反応温度が室温より高く(60~90℃)プロセス設計に有利、(4)複数のアリール基・アルケニル基を導入可能、(5)種々の電子不足オレフィンにボロン酸を立体選択的に共役付加可能、などの成果をあげています。
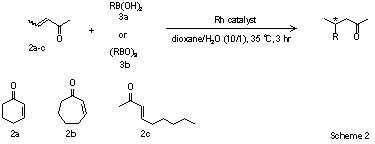
Sigma-Aldrichでは、この最新の触媒テクノロジーを実現する、触媒および活性種へ容易に変換可能な触媒前駆体の両方を試薬としてご提供します(Scheme 1)。Rhダイマー触媒1には、モノマー触媒のRh(acac)(BINAP)に比べ、(1)反応を室温で行うことができ、高温でのボロン試薬の分解が少なくボロン酸使用量が少なくてすむ、(2)芳香族ボロン酸の加水分解が遅いため、1,4-付加生成物の収率が向上する、(3)[RhOH((S)-BINAP)]2のほうがエナンチオ選択性が高い、などの利点があります。総じて、電子特性の異なる環状及び非環状エノンの反応において優れたエナンチオ制御性を示し、高収率、高エナンチオ選択的に生成物を与えます(Scheme 2, 表 1)。
これらのRh(I)触媒は、タキキニンアンタゴニストなどの生物活性分子を合成する際のビルディングブロックとなる、2-aryl-4-piperidone類(Scheme 3)のエナンチオ選択的な合成に利用されました。3,4さまざまな電子特性、立体特性を有する有機ホウ素試薬もしくは有機亜鉛試薬をこの触媒的不斉1,4付加反応に用いられることは留意すべき点であり、すべての場合において、2-aryl-4-piperidone類が高エナンチオ選択的かつ高収率で得られました。

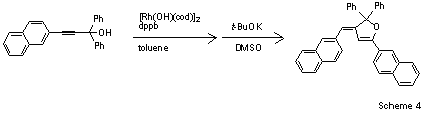
三浦らは、[Rh(OH)(cod)]2を用いてレジオ選択的かつ立体選択的なホモカップリングによりγ-アリール化tert-プロパギルアルコールを得る方法を見出しました(Scheme 4)。5Rh(I)-dppp錯体(dppb=ジフェニルホスフィノブタン)により触媒される新規で有用なアルキンのカップリング反応は、β炭素の脱離により副生成物としてケトンが生成し、2-ヒドロキシメチル-(E)-エニンを与えます。この化合物は、固体で強い蛍光を発するジヒドロフラン誘導体の有用な前駆体です。
続きを確認するには、ログインするか、新規登録が必要です。
アカウントをお持ちではありませんか?


