653152
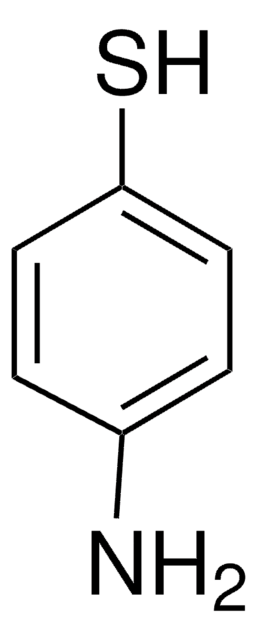
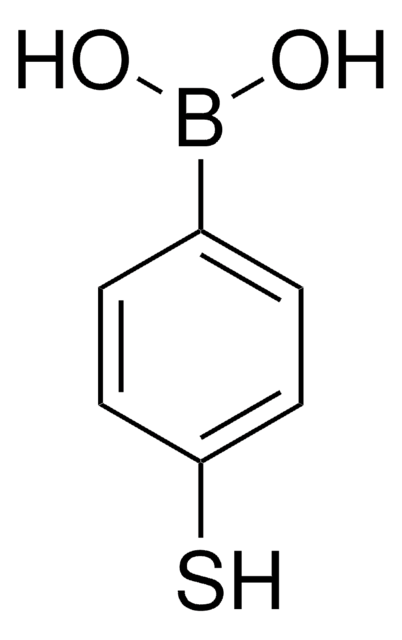
4-メルカプトフェニル酢酸
97%
別名:
(4-Sulfanylphenyl)acetic acid, (4-カルボキシメチル)チオフェノール, 2-(4-Sulfanylphenyl)acetic acid, 2-(4-メルカプトフェニル)酢酸, 4-Mercaptobenzeneacetic acid, p-メルカプトフェニル酢酸
About This Item
アッセイ
97%
形状
solid
mp
105-109 °C (lit.)
保管温度
2-8°C
SMILES記法
OC(=O)Cc1ccc(S)cc1
InChI
1S/C8H8O2S/c9-8(10)5-6-1-3-7(11)4-2-6/h1-4,11H,5H2,(H,9,10)
InChI Key
ORXSLDYRYTVAPC-UHFFFAOYSA-N
詳細
アプリケーション
本化合物は以下の用途に使用することができます。
- ペプチド化学合成のためのケミカルライゲーションプロセスで使用されるペプチドα チオフェニルエステルの樹脂上調製。
- ペプチド調製のためのネイティブケミカルライゲーションおよび/または脱硫法後の(アセトアミド-メチル)システインのワンポット脱保護。
- 合成上困難なタンパク質の調製のためのネイティブケミカルライゲーション法を介した、パラジウムにより促進されたN-末端システインの脱保護。
シグナルワード
Danger
危険有害性情報
危険有害性の分類
Eye Dam. 1 - Skin Irrit. 2 - STOT SE 3
ターゲットの組織
Respiratory system
保管分類コード
11 - Combustible Solids
WGK
WGK 3
引火点(°F)
Not applicable
引火点(℃)
Not applicable
個人用保護具 (PPE)
dust mask type N95 (US), Eyeshields, Gloves
適用法令
試験研究用途を考慮した関連法令を主に挙げております。化学物質以外については、一部の情報のみ提供しています。 製品を安全かつ合法的に使用することは、使用者の義務です。最新情報により修正される場合があります。WEBの反映には時間を要することがあるため、適宜SDSをご参照ください。
Jan Code
653152-VAR:
653152-1G:
653152-5G:
653152-BULK:
試験成績書(COA)
製品のロット番号・バッチ番号を入力して、試験成績書(COA) を検索できます。ロット番号・バッチ番号は、製品ラベルに「Lot」または「Batch」に続いて記載されています。
この製品を見ている人はこちらもチェック
ライフサイエンス、有機合成、材料科学、クロマトグラフィー、分析など、あらゆる分野の研究に経験のあるメンバーがおります。.
製品に関するお問い合わせはこちら(テクニカルサービス)