C–H 官能基化
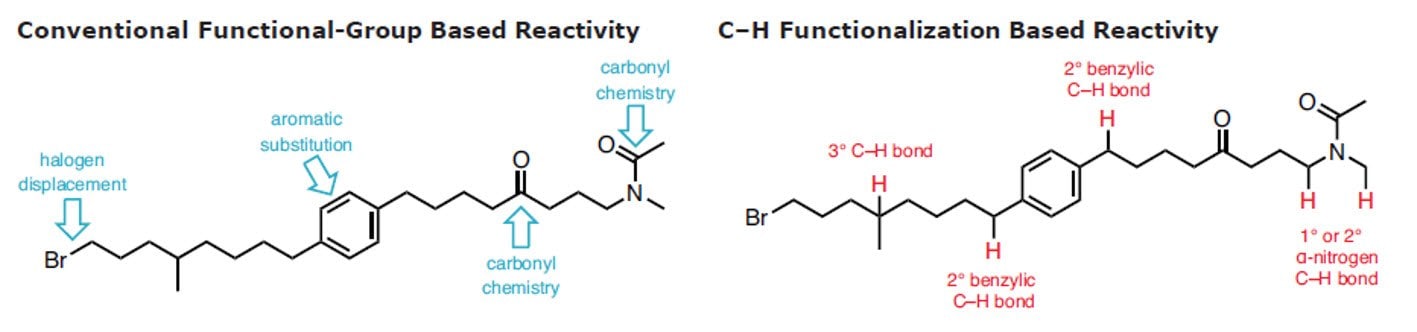
C–H官能基化は、有機合成化学における究極の反応法とされてきました。1近年、有機化学、有機金属、および触媒化学の分野で、C–H結合の反応性の解明とそれを利用した堅牢な反応開発が大きな進歩を遂げており、これらの方法論を逆合成の一般的な手法の一つとして広く活用できる段階に来ているといえるでしょう。2-11 C–H結合をC–C、C–N、C–O、またはC–X結合に選択的かつ精密に制御された方法で確実に変換する手法は、ステップエコノミーと廃棄物削減の観点から有益です。
C–H活性化反応は、特定の分子において反応ターゲットにできるサイトの選択肢を増やし、より複雑な化合物合成のチャンスを増やします。さらに、従来とは完全に異なる化学結合をターゲットにできる高度な化学選択性を備えている点が特徴です。従来の官能基反応と組み合わせることで、C-H官能基化は、複雑な天然物や医薬品合成を大幅に合理化します。C-H官能基化を合成手法の一つに適用することは明らかに利点がありますが、12有機化学の多くのカリキュラムでは、この手法を積極的に活用するようにはまだ更新されていません。詳細は、C-H官能基化反応マニュアルを参照してください。
関連技術資料
- Professor Karl Anker Jørgensen and his group have developed ethers which serve as excellent chiral organocatalysts in the direct asymmetric α-functionalization of aldehydes.
- 芳香族および芳香族ヘテロ環化合物の合成は、化学工業の中核となるテーマです。新しい分子構造への要求がますます増加する中で、どの研究プロジェクトにおいてもコストの削減や開発のスピードアップが求められており、芳香族(ヘテロ環)骨格を多様化する迅速な手法が必要とされています。
- The Du Bois group at Stanford University has made substantial progress within the field of Rh-catalyzed C–H amination via oxidative cyclization of carbamate, sulfamate, sulfamide, urea, and guanidine substrates to give 1,2- and 1,3-heteroatom motifs masked in the form of 5- and 6-membered ring heterocycles.
- 塩化アリールはクロスカップリング反応に利用される化合物であり、医薬品候補化合物や天然物の合成において重要な中間体です。
- 水の存在下でのC-H活性化反応とそれに伴うC-C結合形成のための、リサイクル可能でリガンドを必要としないルテニウム触媒
- すべて表示 (15)
技術資料の検索
参考文献
1.
Arndtsen BA, Bergman RG, Mobley TA, Peterson TH. 1995. Selective Intermolecular Carbon-Hydrogen Bond Activation by Synthetic Metal Complexes in Homogeneous Solution. Acc. Chem. Res.. 28(3):154-162. https://doi.org/10.1021/ar00051a009
2.
He J, Wasa M, Chan KSL, Shao Q, Yu J. 2017. Palladium-Catalyzed Transformations of Alkyl C?H Bonds. Chem. Rev.. 117(13):8754-8786. https://doi.org/10.1021/acs.chemrev.6b00622
3.
Wang D, Weinstein AB, White PB, Stahl SS. 2018. Ligand-Promoted Palladium-Catalyzed Aerobic Oxidation Reactions. Chem. Rev.. 118(5):2636-2679. https://doi.org/10.1021/acs.chemrev.7b00334
4.
Davies HML, Morton D. 2016. Recent Advances in C?H Functionalization. J. Org. Chem.. 81(2):343-350. https://doi.org/10.1021/acs.joc.5b02818
5.
Upp DM, Lewis JC. 2017. Selective C?H bond functionalization using repurposed or artificial metalloenzymes. Current Opinion in Chemical Biology. 3748-55. https://doi.org/10.1016/j.cbpa.2016.12.027
6.
Cernak T, Dykstra KD, Tyagarajan S, Vachal P, Krska SW. The medicinal chemist's toolbox for late stage functionalization of drug-like molecules. Chem. Soc. Rev.. 45(3):546-576. https://doi.org/10.1039/c5cs00628g
7.
Yamaguchi J, Yamaguchi AD, Itami K. 2012. C?H Bond Functionalization: Emerging Synthetic Tools for Natural Products and Pharmaceuticals. Angew. Chem. Int. Ed.. 51(36):8960-9009. https://doi.org/10.1002/anie.201201666
8.
Lyons TW, Sanford MS. 2010. Palladium-Catalyzed Ligand-Directed C?H Functionalization Reactions. Chem. Rev.. 110(2):1147-1169. https://doi.org/10.1021/cr900184e
9.
Wencel-Delord J, Dröge T, Liu F, Glorius F. 2011. Towards mild metal-catalyzed C?H bond activation. Chem. Soc. Rev.. 40(9):4740. https://doi.org/10.1039/c1cs15083a
10.
Arockiam PB, Bruneau C, Dixneuf PH. 2012. Ruthenium(II)-Catalyzed C?H Bond Activation and Functionalization. Chem. Rev.. 112(11):5879-5918. https://doi.org/10.1021/cr300153j
11.
Engle KM, Mei T, Wasa M, Yu J. 2012. Weak Coordination as a Powerful Means for Developing Broadly Useful C?H Functionalization Reactions. Acc. Chem. Res.. 45(6):788-802. https://doi.org/10.1021/ar200185g
12.
Gutekunst WR, Baran PS. 2011. C?H functionalization logic in total synthesis. Chem. Soc. Rev.. 40(4):1976. https://doi.org/10.1039/c0cs00182a
ログインして続行
続きを確認するには、ログインするか、新規登録が必要です。
アカウントをお持ちではありませんか?