Purificazione delle proteine
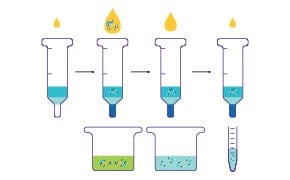
Nella ricerca biologica e biomedica vengono ampiamente utilizzati numerosi metodi di purificazione delle proteine. La scelta delle metodiche per l’espressione di una proteina ricombinante e dei flussi di lavoro per purificarla dipendono da molte variabili tra cui proprietà fisiche e funzione biologica della proteina in esame e il tipo di cellula, batterica o eucariotica, che deve essere utilizzata per esprimerla. Sono stati compiuti significativi progressi nell'area dell’espressione di proteinericombinanti e delle relative metodologie di purificazione e in commercio sono ora disponibili diversi kit e sistemi. Tuttavia, le proteine sono macromolecole complesse e le strategie da utilizzare per un’espressione e una purificazione ottimali devono essere determinate empiricamente.
Articoli tecnici correlati
- Protocol for immunoprecipitation (IP) of FLAG fusion proteins using M2 monoclonal antibody 4% agarose affinity gels
- This page shows how to perform sample desalting, buffer exchange and concentration for affinity chromatography of tagged proteins.
- This page shows how to solubilize membrane proteins with products from Cytiva.
- This page describes efficient column packing and preparation for affinity chromatography of tagged proteins using Cytiva products.
- This page covers the use of Sepharose Fast Flow for purification of proteins.
- Visualizza tutti (71)
Protocolli correlati
- Reduce plastic waste and eliminate hazardous liquid waste for more sustainable laboratories with GenElute™-E Single Spin DNA and RNA prep kits.
- This page shows how to optimize purification of histidine-tagged proteins using GE Healthcare products.
- This page shows how to separate proteins and peptides with affinity for metal ions by immobilized metal chelate affinity chromatography using HiTrap Chelating HP, Chelating Sepharose Fast Flow,His MicroSpin Purification Module or HisTrap Kit from Cytiva.
- His GraviTrap™ TALON® columns are prepacked with 1 ml of TALON® Superflow medium. Each column provides simple manual purification of up to 15 mg of histidine-tagged proteins.
- This page discusses column packing and preparation techniques for reverse phase chromatography.
- Visualizza tutto (107)
Fattori critici per la purificazione delle proteine
La struttura e la funzione delle proteine sono spesso tra i fattori critici da considerare nella scelta della strategia di purificazione. L'attività biochimica o biologica di una proteina ricombinante è parzialmente determinata da domini discreti all'interno della proteina stessa, che dipendono, in buona parte, dal ripiegamento della proteina nelle sue strutture secondaria, terziaria e quaternaria.
Il ripiegamento delle proteine, che viene complessivamente definito struttura di ordine superiore (HOS), è essenziale per la corretta forma tridimensionale e per la funzione della proteina. Un’altra caratteristica molto importante per la purificazione di una proteina è data dalla sua solubilità che è influenzata da numerosi fattori tra cui la dimensione e gli elementi presenti in corrispondenza dell’N e del C-terminale. Comunemente, le proteine ricombinanti incorporano in posizione N- e C-terminale delle etichette (tag), cioè piccole sequenze utilizzate per il rilevamento e la purificazione mediante immunoistochimica o cromatografia di affinità, a seconda del tipo di etichetta e della successiva applicazione.
Metodiche di purificazione delle proteine e relative applicazioni
I ricercatori hanno oggi a disposizione numerose metodiche, reagenti e strumenti per la purificazione delle proteine, sia che intendano studiarne la funzione o che cerchino di incrementarne la purificazione usando strategie su scala industriale per produzioni biologiche e farmaceutiche La metodica di purificazione prescelta determinerà in parte il flusso di lavoro per la preparazione del campione. La cromatografia di affinità rappresenta una fase di purificazione iniziale adatta per le proteinericombinanti solubilizzate che contengano le tag opportune; spesso succede però che si leghino alla colonna anche proteine indesiderate e che eluiscano nel lavaggio finale insieme alla proteina di interesse. Se è necessario si ricorre quindi ad un ulteriore fase di purificazione utilizzando strategie di purificazione supplementari che includono la cromatografia di esclusione dimensionale o la cromatografia a scambio ionico. È importante sottolineare che, nel caso in cui i ricercatori vogliano eliminare qualsiasi sequenza non nativa dalla proteina purificata finale, molte delle etichette di affinità possono essere rimosse.
Per continuare a leggere, autenticati o crea un account.
Non hai un Account?