90182
Nα-Tosyl-L-lysine chloromethyl ketone hydrochloride
≥99.0% (AT)
Sinónimos:
(3S)-1-Chloro-3-tosylamido-7-amino-2-heptanone hydrochloride, (3S)-7-Amino-1-chloro-3-tosylamino-2-heptanone hydrochloride, TLCK, Tosyl-L-lysyl-chloromethane hydrochloride
About This Item
Productos recomendados
origen biológico
synthetic
Nivel de calidad
Análisis
≥99.0% (AT)
formulario
powder or crystals
actividad óptica
[α]20/D −7.8±0.5°, c = 2% in H2O
temp. de almacenamiento
−20°C
cadena SMILES
Cl[H].Cc1ccc(cc1)S(=O)(=O)N[C@@H](CCCCN)C(=O)CCl
InChI
1S/C14H21ClN2O3S.ClH/c1-11-5-7-12(8-6-11)21(19,20)17-13(14(18)10-15)4-2-3-9-16;/h5-8,13,17H,2-4,9-10,16H2,1H3;1H/t13-;/m0./s1
Clave InChI
YFCUZWYIPBUQBD-ZOWNYOTGSA-N
¿Está buscando productos similares? Visita Guía de comparación de productos
Otras notas
Código de clase de almacenamiento
11 - Combustible Solids
Clase de riesgo para el agua (WGK)
WGK 3
Punto de inflamabilidad (°F)
Not applicable
Punto de inflamabilidad (°C)
Not applicable
Equipo de protección personal
dust mask type N95 (US), Eyeshields, Gloves
Certificados de análisis (COA)
Busque Certificados de análisis (COA) introduciendo el número de lote del producto. Los números de lote se encuentran en la etiqueta del producto después de las palabras «Lot» o «Batch»
¿Ya tiene este producto?
Encuentre la documentación para los productos que ha comprado recientemente en la Biblioteca de documentos.
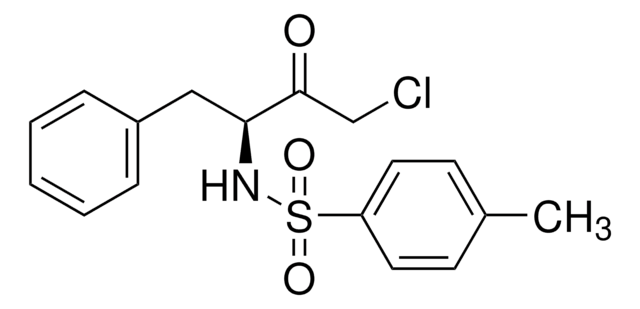
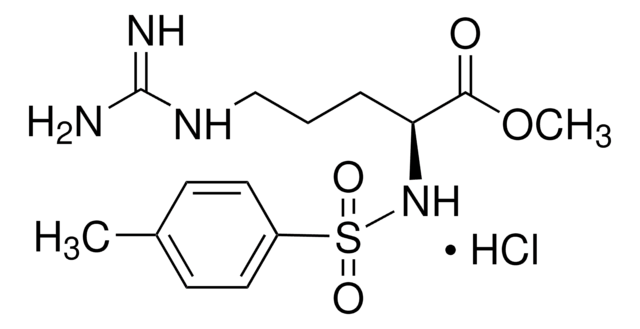
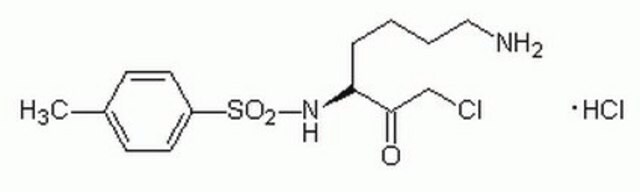
Los clientes también vieron
Nuestro equipo de científicos tiene experiencia en todas las áreas de investigación: Ciencias de la vida, Ciencia de los materiales, Síntesis química, Cromatografía, Analítica y muchas otras.
Póngase en contacto con el Servicio técnico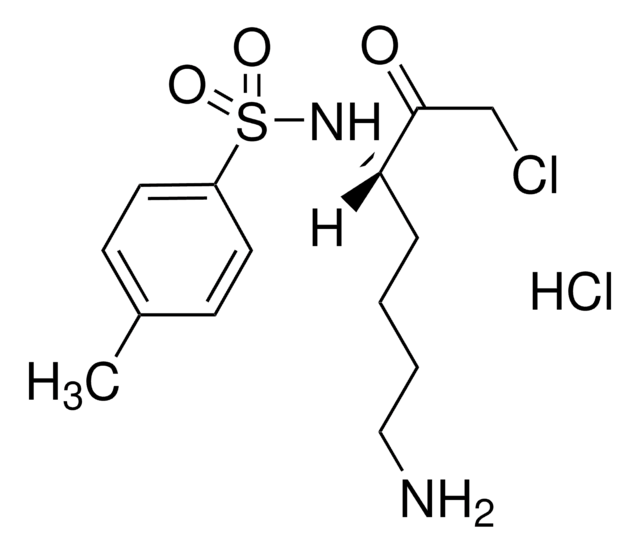












![3-[(3-Colamidopropil)dimetilamonio]-1-propanosulfonato hydrate BioReagent, suitable for electrophoresis, ≥98% (HPLC)](/deepweb/assets/sigmaaldrich/product/structures/322/134/88b00489-fbbd-47b7-ba3e-430dd6a3c852/640/88b00489-fbbd-47b7-ba3e-430dd6a3c852.png)
