P5318
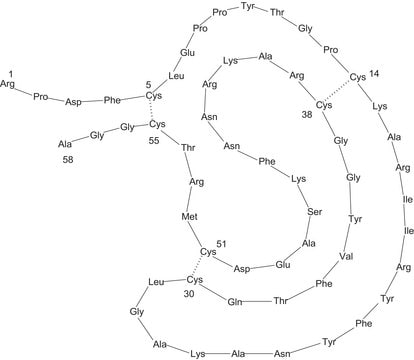
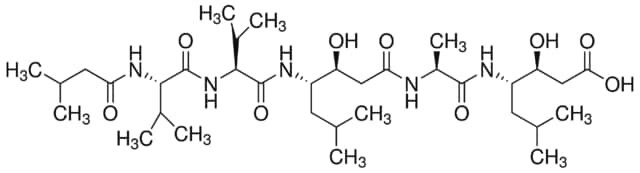
Pepstatina A
powder, ≥90% (HPLC)
About This Item
Productos recomendados
product name
Pepstatina A, microbial, ≥90% (HPLC)
origen biológico
microbial
Nivel de calidad
Análisis
≥90% (HPLC)
formulario
powder
mp
233 °C (dec.) (lit.)
solubilidad
ethanol: 1-2 mg/mL (with heat up to 60 °C)
temp. de almacenamiento
2-8°C
cadena SMILES
CC(C)C[C@H](NC(=O)[C@H](C)NC(=O)C[C@H](O)[C@H](CC(C)C)NC(=O)[C@@H](NC(=O)[C@@H](NC(=O)CC(C)C)C(C)C)C(C)C)[C@@H](O)CC(O)=O
InChI
1S/C34H63N5O9/c1-17(2)12-23(37-33(47)31(21(9)10)39-34(48)30(20(7)8)38-27(42)14-19(5)6)25(40)15-28(43)35-22(11)32(46)36-24(13-18(3)4)26(41)16-29(44)45/h17-26,30-31,40-41H,12-16H2,1-11H3,(H,35,43)(H,36,46)(H,37,47)(H,38,42)(H,39,48)(H,44,45)/t22-,23-,24-,25-,26-,30-,31-/m0/s1
Clave InChI
FAXGPCHRFPCXOO-LXTPJMTPSA-N
¿Está buscando productos similares? Visita Guía de comparación de productos
Descripción general
Aplicación
Acciones bioquímicas o fisiológicas
Nota de preparación
Las disoluciones de reserva a 1 mg/ml son estables por lo menos durante una semana a 4 °C. Una disolución 1 mM en metanol o DMSO es estable durante meses a -20 °C. Si las disoluciones se vuelven de color amarillo oscuros, el reactivo se está hidrolizando.
Una concentración de trabajo de 1 μM es estable durante como mínimo un día a temperatura ambiente.
Código de clase de almacenamiento
11 - Combustible Solids
Clase de riesgo para el agua (WGK)
WGK 2
Punto de inflamabilidad (°F)
Not applicable
Punto de inflamabilidad (°C)
Not applicable
Equipo de protección personal
Eyeshields, Gloves, type N95 (US)
Certificados de análisis (COA)
Busque Certificados de análisis (COA) introduciendo el número de lote del producto. Los números de lote se encuentran en la etiqueta del producto después de las palabras «Lot» o «Batch»
¿Ya tiene este producto?
Encuentre la documentación para los productos que ha comprado recientemente en la Biblioteca de documentos.
Los clientes también vieron
Nuestro equipo de científicos tiene experiencia en todas las áreas de investigación: Ciencias de la vida, Ciencia de los materiales, Síntesis química, Cromatografía, Analítica y muchas otras.
Póngase en contacto con el Servicio técnico