Alle Fotos(5)
Wichtige Dokumente
G2253
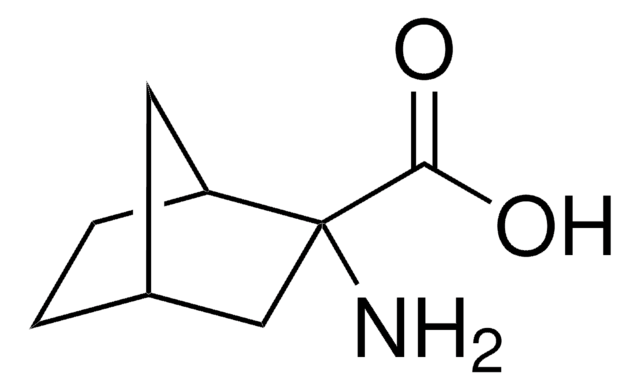
L-Glutaminsäure-γ-Monohydroxamat
≥97% (TLC)
Synonym(e):
L-γ-Glutamylhydroxamsäure, L-5-N-Hydroxyglutamin
Anmeldenzur Ansicht organisationsspezifischer und vertraglich vereinbarter Preise
Alle Fotos(5)
About This Item
Empirische Formel (Hill-System):
C5H10N2O4
CAS-Nummer:
Molekulargewicht:
162.14
MDL-Nummer:
UNSPSC-Code:
12352209
PubChem Substanz-ID:
NACRES:
NA.26
Empfohlene Produkte
Produktbezeichnung
L-Glutaminsäure-γ-Monohydroxamat,
Assay
≥97% (TLC)
Qualitätsniveau
Form
powder
Farbe
white to off-white
Anwendung(en)
detection
Lagertemp.
−20°C
SMILES String
NC(CCC(=O)NO)C(O)=O
InChI
1S/C5H10N2O4/c6-3(5(9)10)1-2-4(8)7-11/h3,11H,1-2,6H2,(H,7,8)(H,9,10)
InChIKey
YVGZXTQJQNXIAU-UHFFFAOYSA-N
Anwendung
L-Glutaminsäure-γ-Monohydroxamat wird als Standard zur Berechnung der Transglutaminase(TG)-Aktivität verwendet.
Biochem./physiol. Wirkung
L-Glutaminsäure-γ-Monohydroxamat [L-Glu (Gamma) HXM] wird als Vanadiumliganden eingesetzt, der die Stoffwechselaktivität von Vanadium potenziert. Außerdem wird L-Glu (Gamma) HXM als Substrat für E. coli Asparaginsynthetase B und als ATP-abhängiger irreversibler Inhibitor von Escherichia coli Gamma-Glutamylcystein-Synthetase verwendet.
Lagerklassenschlüssel
11 - Combustible Solids
WGK
WGK 3
Flammpunkt (°F)
Not applicable
Flammpunkt (°C)
Not applicable
Persönliche Schutzausrüstung
Eyeshields, Gloves, type N95 (US)
Hier finden Sie alle aktuellen Versionen:
Besitzen Sie dieses Produkt bereits?
In der Dokumentenbibliothek finden Sie die Dokumentation zu den Produkten, die Sie kürzlich erworben haben.
Kunden haben sich ebenfalls angesehen
M Katoh et al.
Bioscience, biotechnology, and biochemistry, 62(7), 1455-1457 (1998-08-28)
Incubation of Escherichia coli gamma-glutamylcysteine synthetase with L-glutamic acid gamma-monohydroxamate and ATP caused slow but irreversible inhibition of the enzyme, and more than 90% activity was lost in three days. The enzyme was not inactivated when ATP was absent or
N Seiler et al.
Neurochemical research, 15(3), 301-305 (1990-03-01)
The method for the assay of glutamine synthetase (GlnS) relies on the gamma-glutamyl transferase reaction, i.e. the formation of glutamyl-gamma-hydroxamate from glutamine and hydroxylamine, and the chromatographic separation of the reaction product from the reactants. The method is not only
X Huang et al.
The Journal of biological chemistry, 275(34), 26233-26240 (2000-08-22)
The x-ray crystal structure of the heterodimeric carbamoyl phosphate synthetase from Escherichia coli has identified an intermolecular tunnel that connects the glutamine binding site within the small amidotransferase subunit to the two phosphorylation sites within the large synthetase subunit. The
N Thomasset et al.
Anticancer research, 13(5A), 1393-1398 (1993-09-01)
We have previously shown that L-glutamic acid gamma-monohydroxamate (GAH) exhibits an antitumor activity, both in vitro and in vivo. In this report we explore the selective cytotoxicity of GAH in vitro by comparing the survival of tumor and normal cells.
C J Lusty
FEBS letters, 314(2), 135-138 (1992-12-14)
E. coli carbamyl phosphate synthetase binds 0.2-0.4 mol equivalents of glutamine in an acid resistant form. The bound material is quantitatively released as glutamate by weak base hydrolysis and as a mixture of 12% glutamate, 10% gamma-glutamylhydroxamate, and 70% pyrrollidonecarboxylic
Unser Team von Wissenschaftlern verfügt über Erfahrung in allen Forschungsbereichen einschließlich Life Science, Materialwissenschaften, chemischer Synthese, Chromatographie, Analytik und vielen mehr..
Setzen Sie sich mit dem technischen Dienst in Verbindung.