G4251
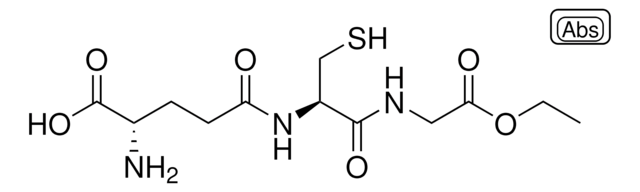
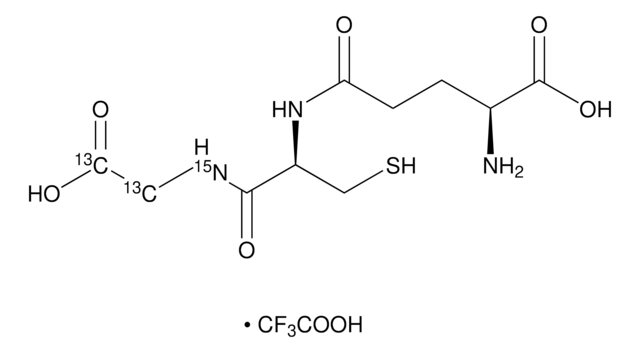
L-Glutathion reduziert
≥98.0%
Synonym(e):
Glutathion-SH, γ-L-Glutamyl-L-cysteinyl-glycin, GSH
About This Item
Empfohlene Produkte
product name
L-Glutathion reduziert, ≥98.0%
Qualitätsniveau
Assay
≥98.0%
Form
powder
Farbe
white
mp (Schmelzpunkt)
192-195 °C (dec.) (lit.)
Löslichkeit
water: 50 mg/mL, clear, colorless
Anwendung(en)
detection
Funktionelle Gruppe
amine
carboxylic acid
thiol
Lagertemp.
2-8°C
SMILES String
N[C@@H](CCC(=O)N[C@@H](CS)C(=O)NCC(O)=O)C(O)=O
InChI
1S/C10H17N3O6S/c11-5(10(18)19)1-2-7(14)13-6(4-20)9(17)12-3-8(15)16/h5-6,20H,1-4,11H2,(H,12,17)(H,13,14)(H,15,16)(H,18,19)/t5-,6-/m0/s1
InChIKey
RWSXRVCMGQZWBV-WDSKDSINSA-N
Suchen Sie nach ähnlichen Produkten? Aufrufen Leitfaden zum Produktvergleich
Amino Acid Sequence
Allgemeine Beschreibung
Anwendung
Biochem./physiol. Wirkung
Sonstige Hinweise
Vergleichbares Produkt
auch häufig zusammen mit diesem Produkt gekauft
Ähnliches Produkt
Lagerklassenschlüssel
11 - Combustible Solids
WGK
WGK 2
Flammpunkt (°F)
Not applicable
Flammpunkt (°C)
Not applicable
Persönliche Schutzausrüstung
Eyeshields, Gloves, type N95 (US)
Hier finden Sie alle aktuellen Versionen:
Besitzen Sie dieses Produkt bereits?
In der Dokumentenbibliothek finden Sie die Dokumentation zu den Produkten, die Sie kürzlich erworben haben.
Kunden haben sich ebenfalls angesehen
Artikel
Oxidative stress is mediated, in part, by reactive oxygen species produced by multiple cellular processes and controlled by cellular antioxidant mechanisms such as enzymatic scavengers or antioxidant modulators. Free radicals, such as reactive oxygen species, cause cellular damage via cellular.
Antioxidants protect biological systems from oxidative damage produced by oxygen-containing free radicals and from redoxactive transition metal ions such as iron, copper, and cadmium.
Unser Team von Wissenschaftlern verfügt über Erfahrung in allen Forschungsbereichen einschließlich Life Science, Materialwissenschaften, chemischer Synthese, Chromatographie, Analytik und vielen mehr..
Setzen Sie sich mit dem technischen Dienst in Verbindung.