8.52008
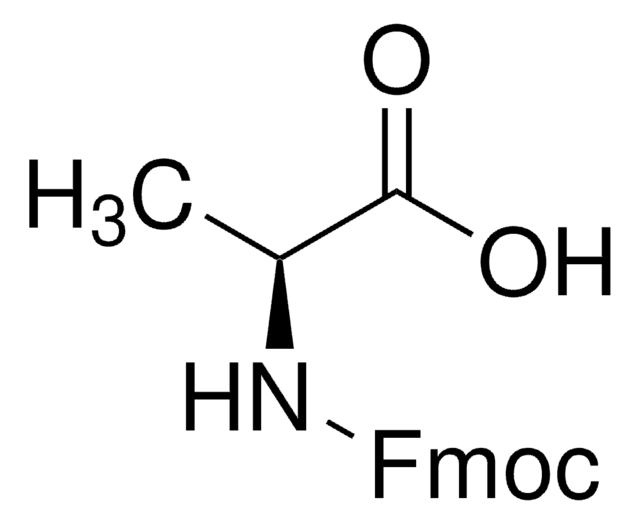
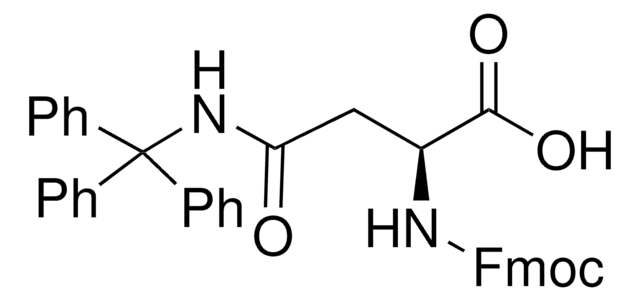
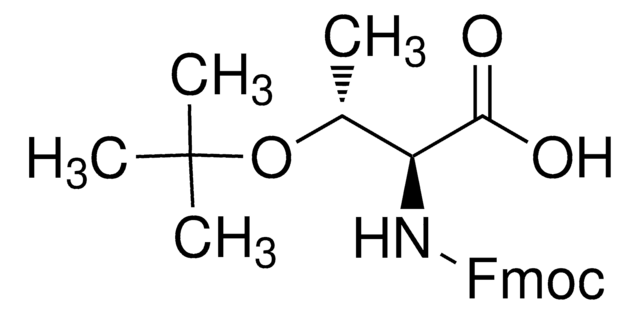
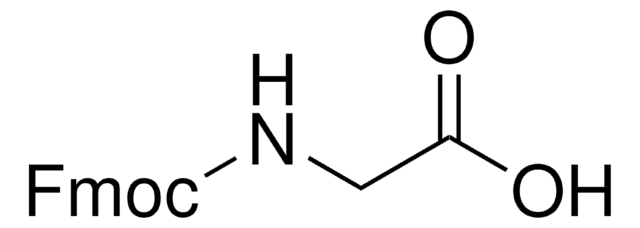
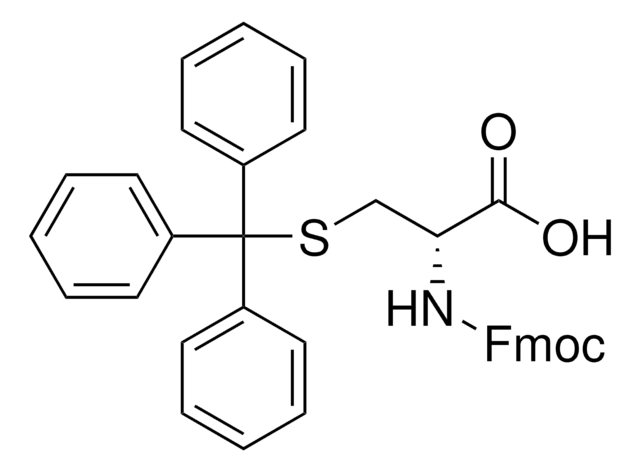
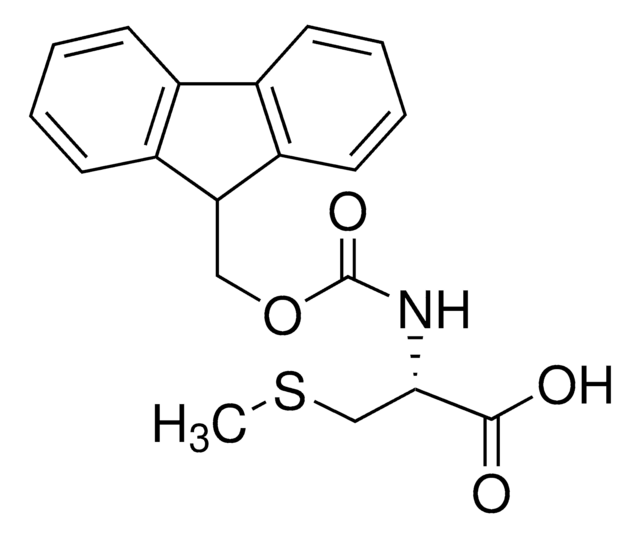
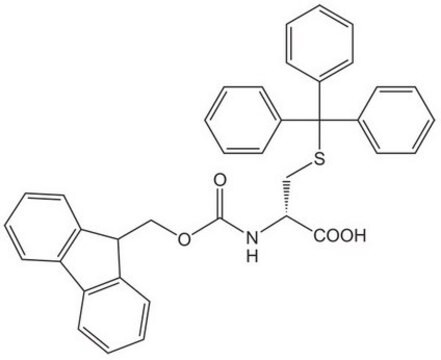
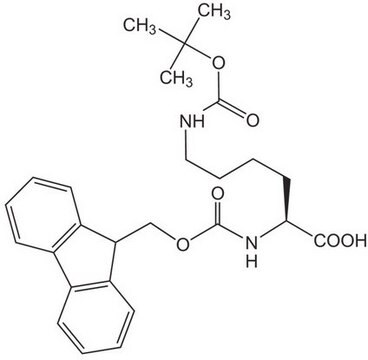
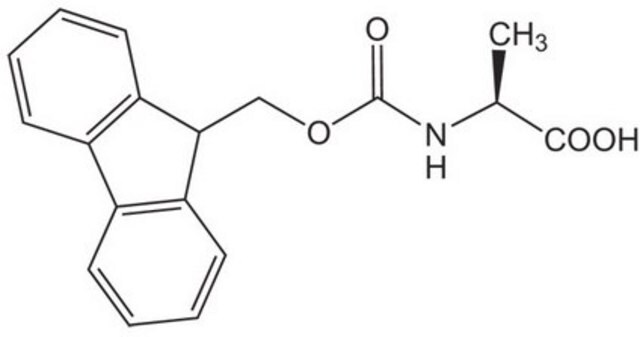
Fmoc-Cys(Trt)-OH
Novabiochem®
Synonyme(s) :
Fmoc-Cys(Trt)-OH, N-α-Fmoc-S-trityl-L-cysteine
About This Item
Produits recommandés
Niveau de qualité
Gamme de produits
Novabiochem®
Pureté
≥98% (TLC)
≥98.0% (acidimetric)
≥99.0% (HPLC)
Forme
powder
Capacité de réaction
reaction type: Fmoc solid-phase peptide synthesis
Fabricant/nom de marque
Novabiochem®
Pf
164-175 °C
Application(s)
peptide synthesis
Groupe fonctionnel
thiol
Température de stockage
−20°C (−15°C to −25°C)
InChI
1S/C37H31NO4S/c39-35(40)34(38-36(41)42-24-33-31-22-12-10-20-29(31)30-21-11-13-23-32(30)33)25-43-37(26-14-4-1-5-15-26,27-16-6-2-7-17-27)28-18-8-3-9-19-28/h1-23,33-34H,24-25H2,(H,38,41)(H,39,40)/p-1/t34-/m0/s1
Clé InChI
KLBPUVPNPAJWHZ-UMSFTDKQSA-M
Description générale
Associated Protocols and Technical Articles
Fmoc-amino acids for Peptide Production
Cleavage and Deprotection Protocols for Fmoc SPPS
Fmoc SPPS of Cysteine-Containing Peptides
Literature references
[1] S. N. McCurdy (1989) Pept. Res., 2, 147.
[2] T. Kaiser, et al. (1996) Tetrahedron Lett., 37, 1187.
[3] Y. X. Han, et al. (1997) J. Org. Chem., 62, 4307.
[4] Y. N. Angell (2002) J. Peptide Res., 5, 292.
Application
- On-resin synthesis of cyclic peptides via tandem N-to-S acyl migration and intramolecular thiol additive-free native chemical ligation: Discusses the use of Fmoc-Cys(Trt)-OH in the synthesis of cyclic peptides, highlighting the efficiency of the resin synthesis method. (Serra et al., 2020).
- Selective Bi‐directional Amide Bond Cleavage of N‐Methylcysteinyl Peptide: The study utilized Fmoc-Cys(Trt)-OH in exploring selective bi-directional amide bond cleavage in peptides, providing insights into controlled peptide modification. (Qiu et al., 2014).
Liaison
Remarque sur l'analyse
Appearance of substance (visual): powder
Colour index (0,5 M in DMF): ≤ 150 Hazen
Identity (IR): passes test
Enantiomeric purity: ≥ 99.5 % (a/a)
Purity (HPLC): ≥ 99.0 % (a/a)
Fmoc-ß-Ala-OH (HPLC): ≤ 0.1 % (a/a)
Fmoc-ß-Ala-Cys (Trt) -OH (HPLC): ≤ 0.1 % (a/a)
Fmoc-Cys(Trt)-Cys(Trt)-OH (HPLC): ≤ 0.1 % (a/a)
Fmoc-Cys-OH (HPLC): ≤ 0.1 % (a/a)
Assay free amino acid (HPLC): ≤ 0.2 %
Purity (TLC(011A)): ≥ 98 %
Purity (TLC(0811)): ≥ 98 %
Solubility (1 mmole in 2 ml DMF): clearly soluble
Assay (acidimetric): ≥ 98.0 %
Water (K. F.): ≤ 2.0 %
Ethyl acetate (HS-GC): ≤ 0.5 %
Acetate (IC): ≤ 0.02 %
To see the solvent systems used for TLC of Novabiochem® products please click here.
Informations légales
Not finding the right product?
Try our Outil de sélection de produits.
Code de la classe de stockage
11 - Combustible Solids
Classe de danger pour l'eau (WGK)
WGK 3
Point d'éclair (°F)
Not applicable
Point d'éclair (°C)
Not applicable
Certificats d'analyse (COA)
Recherchez un Certificats d'analyse (COA) en saisissant le numéro de lot du produit. Les numéros de lot figurent sur l'étiquette du produit après les mots "Lot" ou "Batch".
Déjà en possession de ce produit ?
Retrouvez la documentation relative aux produits que vous avez récemment achetés dans la Bibliothèque de documents.
Les clients ont également consulté
Notre équipe de scientifiques dispose d'une expérience dans tous les secteurs de la recherche, notamment en sciences de la vie, science des matériaux, synthèse chimique, chromatographie, analyse et dans de nombreux autres domaines..
Contacter notre Service technique