K1140
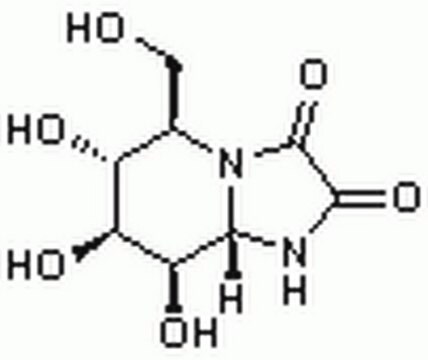
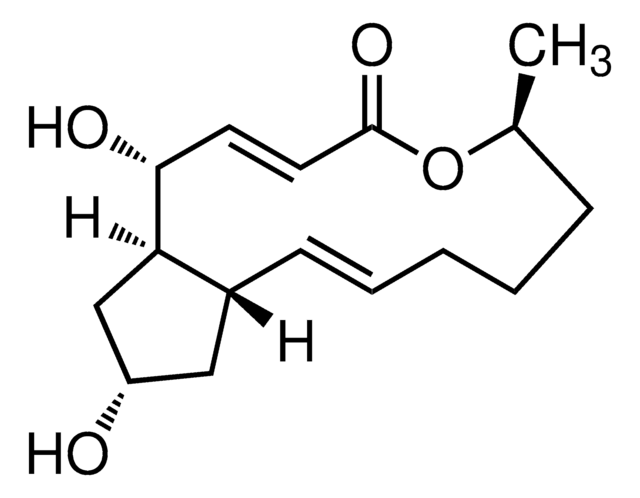
Kifunensin
solid,film or powder, ≥98%
Synonym(e):
FR 900494, Hexahydro-6R,7S,8aS-trihydroxy-5R-(hydroxymethyl)-imidazo[1,2-a] pyridin-2,3-dion
About This Item
Empfohlene Produkte
product name
Kifunensin, mannosidase inhibitor
Biologische Quelle
synthetic (organic)
Qualitätsniveau
Assay
≥98%
Form
film or powder
solid
Löslichkeit
water, double-distilled: 50 mM
Lagertemp.
−20°C
InChI
1S/C8H12N2O6/c11-1-2-3(12)4(13)5(14)6-9-7(15)8(16)10(2)6/h2-6,11-14H,1H2,(H,9,15)/t2-,3-,4+,5+,6+/m1/s1
InChIKey
OIURYJWYVIAOCW-PQMKYFCFSA-N
Angaben zum Gen
human ... MAN1A1(4121) , MAN1A2(10905) , MAN1B1(11253) , MAN1C1(57134)
mouse ... MAN1A1(17155) , MAN1A2(17156) , MAN1B1(227619) , MAN1C1(230815)
rat ... MAN1A1(294410) , MAN1A2(295319) , MAN1B1(499751) , MAN1C1(362625)
Allgemeine Beschreibung
Anwendung
Biochem./physiol. Wirkung
Signalwort
Warning
H-Sätze
Gefahreneinstufungen
Eye Irrit. 2
Lagerklassenschlüssel
11 - Combustible Solids
WGK
WGK 3
Flammpunkt (°F)
Not applicable
Flammpunkt (°C)
Not applicable
Persönliche Schutzausrüstung
Eyeshields, Gloves, type N95 (US)
Analysenzertifikate (COA)
Suchen Sie nach Analysenzertifikate (COA), indem Sie die Lot-/Chargennummer des Produkts eingeben. Lot- und Chargennummern sind auf dem Produktetikett hinter den Wörtern ‘Lot’ oder ‘Batch’ (Lot oder Charge) zu finden.
Besitzen Sie dieses Produkt bereits?
In der Dokumentenbibliothek finden Sie die Dokumentation zu den Produkten, die Sie kürzlich erworben haben.
Kunden haben sich ebenfalls angesehen
Unser Team von Wissenschaftlern verfügt über Erfahrung in allen Forschungsbereichen einschließlich Life Science, Materialwissenschaften, chemischer Synthese, Chromatographie, Analytik und vielen mehr..
Setzen Sie sich mit dem technischen Dienst in Verbindung.