208921
Calmodulin Kinase IINtide, Myristoylated
≥95% (HPLC), solid, CaMK II inhibitor, Calbiochem®
Synonim(y):
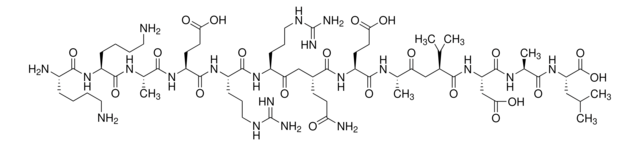
Calmodulin Kinase IINtide, Myristoylated, Myr-N-GGGKRPPKLGQIGRAKRVVIEDDRIDDVLK-OH
About This Item
Polecane produkty
product name
Calmodulin Kinase IINtide, Myristoylated, The myristoylated form of CaMK IINtide.
Poziom jakości
Próba
≥95% (HPLC)
Postać
solid
producent / nazwa handlowa
Calbiochem®
warunki przechowywania
OK to freeze
desiccated (hygroscopic)
kolor
white
rozpuszczalność
DMSO: 5 mg/mL
Warunki transportu
ambient
temp. przechowywania
−20°C
Opis ogólny
Działania biochem./fizjol.
Calmodulin-Dependent Protein Kinase (CaM Kinase)-2
Opakowanie
Ostrzeżenie
Sekwencja
Postać fizyczna
Rekonstytucja
Inne uwagi
Chang, B.H., et al. 1998. Proc. Natl. Acad. Sci. USA95, 10890.
Pereda, A.E., et al. 1998. Proc. Natl. Acad. Sci. USA95, 13272.
Informacje prawne
Kod klasy składowania
11 - Combustible Solids
Klasa zagrożenia wodnego (WGK)
WGK 1
Temperatura zapłonu (°F)
Not applicable
Temperatura zapłonu (°C)
Not applicable
Certyfikaty analizy (CoA)
Poszukaj Certyfikaty analizy (CoA), wpisując numer partii/serii produktów. Numery serii i partii można znaleźć na etykiecie produktu po słowach „seria” lub „partia”.
Masz już ten produkt?
Dokumenty związane z niedawno zakupionymi produktami zostały zamieszczone w Bibliotece dokumentów.
Nasz zespół naukowców ma doświadczenie we wszystkich obszarach badań, w tym w naukach przyrodniczych, materiałoznawstwie, syntezie chemicznej, chromatografii, analityce i wielu innych dziedzinach.
Skontaktuj się z zespołem ds. pomocy technicznej