F6312
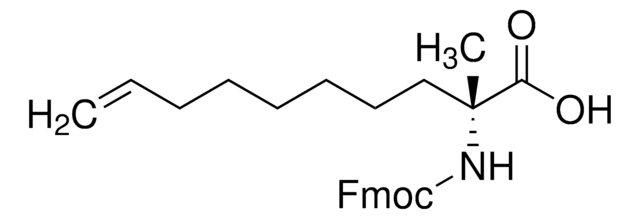
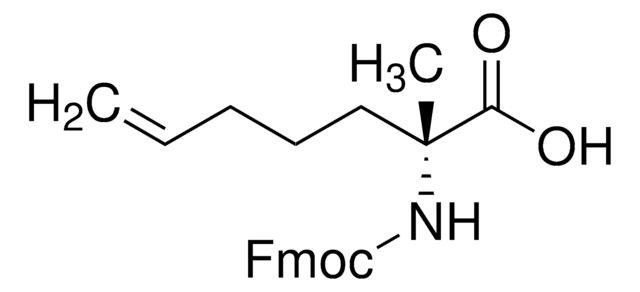
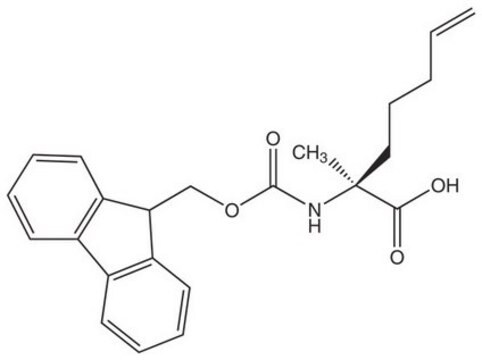
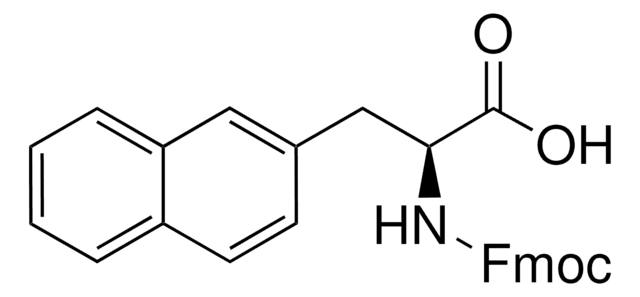
Fmoc-(S)-2-(4-pentenyl)Ala-OH
≥97%, for peptide synthesis
Sinonimo/i:
(S)-N-Fmoc-α-4-n-pentenylalanine, Fmoc-(S)-2-(4-pentenyl)alanine, Fmoc-(S)-2-amino-2-methyl-hept-6-enoic acid
About This Item
Prodotti consigliati
Nome del prodotto
Fmoc-(S)-2-(4-pentenyl)Ala-OH, ≥97%
Saggio
≥97%
Stato
solid
Impiego in reazioni chimiche
reaction type: Fmoc solid-phase peptide synthesis
Punto di fusione
<30 °C
applicazioni
peptide synthesis
Gruppo funzionale
Fmoc
Temperatura di conservazione
−20°C
Stringa SMILE
N([C@](CCCC=C)(C)C(=O)O)C(=O)OCC1c2c(cccc2)c3c1cccc3
InChI
1S/C23H25NO4/c1-3-4-9-14-23(2,21(25)26)24-22(27)28-15-20-18-12-7-5-10-16(18)17-11-6-8-13-19(17)20/h3,5-8,10-13,20H,1,4,9,14-15H2,2H3,(H,24,27)(H,25,26)/t23-/m0/s1
MRJFPZWLOJOINV-QHCPKHFHSA-N
Categorie correlate
Applicazioni
Codice della classe di stoccaggio
11 - Combustible Solids
Classe di pericolosità dell'acqua (WGK)
WGK 3
Punto d’infiammabilità (°F)
Not applicable
Punto d’infiammabilità (°C)
Not applicable
Scegli una delle versioni più recenti:
Possiedi già questo prodotto?
I documenti relativi ai prodotti acquistati recentemente sono disponibili nell’Archivio dei documenti.
I clienti hanno visto anche
Il team dei nostri ricercatori vanta grande esperienza in tutte le aree della ricerca quali Life Science, scienza dei materiali, sintesi chimica, cromatografia, discipline analitiche, ecc..
Contatta l'Assistenza Tecnica.