914339
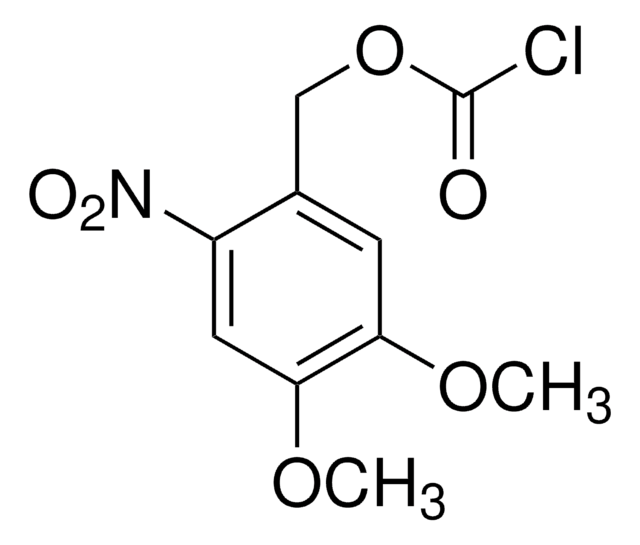
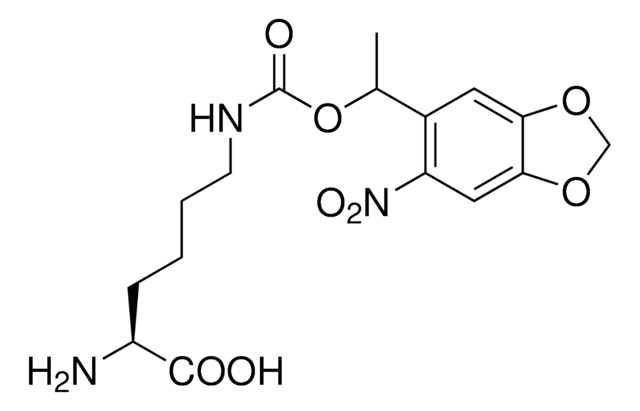
Fmoc-L-Lys(Nvoc)-OH
≥98%
Sinonimo/i:
(S)-2-(((9H-Fluoren-9-yl)methoxy)carbonylamino)-6-((4,5-dimethoxy-2-nitrobenzyloxy)carbonylamino)hexanoic acid, N2-(((9H-Fluoren-9-yl)methoxy)carbonyl)-N6-(((4,5-dimethoxy-2-nitrobenzyl)oxy)carbonyl)-L-lysine, Lysine with photoremovable NVOC, Photocaged amino acid, Photocleavable lysine derivative
About This Item
Prodotti consigliati
Livello qualitativo
Saggio
≥98%
Forma fisica
powder
Punto di fusione
108 °C (decomp.)
Temperatura di conservazione
2-8°C
Applicazioni
Product can be used with our line of photoreactors: Including Penn PhD (Z744035) & SynLED 2.0 (Z744080)
Prodotti correlati
Codice della classe di stoccaggio
11 - Combustible Solids
Classe di pericolosità dell'acqua (WGK)
WGK 3
Punto d’infiammabilità (°F)
Not applicable
Punto d’infiammabilità (°C)
Not applicable
Scegli una delle versioni più recenti:
Certificati d'analisi (COA)
Ci dispiace, ma al momento non ci sono COA disponibili online per questo prodotto.
Se ti serve aiuto, non esitare a contattarci Servizio Clienti
Possiedi già questo prodotto?
I documenti relativi ai prodotti acquistati recentemente sono disponibili nell’Archivio dei documenti.
Il team dei nostri ricercatori vanta grande esperienza in tutte le aree della ricerca quali Life Science, scienza dei materiali, sintesi chimica, cromatografia, discipline analitiche, ecc..
Contatta l'Assistenza Tecnica.