P4265
Pepstatine A
powder, ≥75% (HPLC)
Synonyme(s) :
Pepsin inhibitor
About This Item
Produits recommandés
product name
Pepstatine A, microbial, ≥75% (HPLC)
Source biologique
microbial
Niveau de qualité
Pureté
≥75% (HPLC)
Forme
powder
Pf
233 °C (dec.) (lit.)
Solubilité
ethanol: acetic acid (9:1): 1 mg/mL, clear to hazy, colorless
Température de stockage
2-8°C
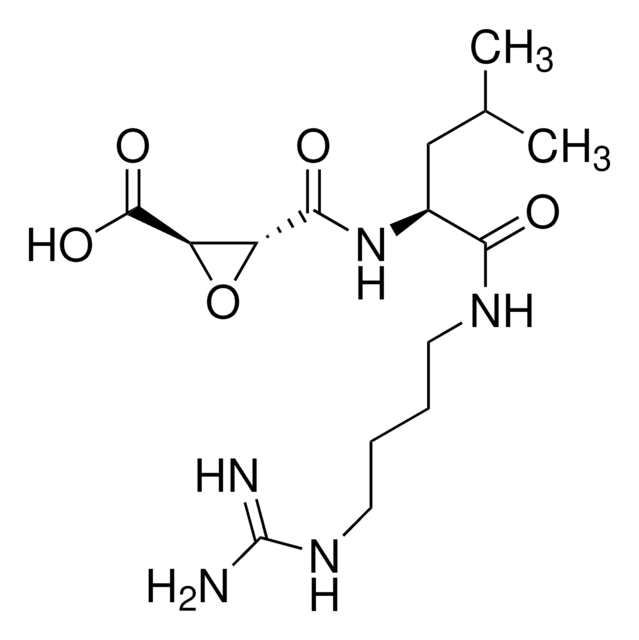
Chaîne SMILES
CC(C)C[C@H](NC(=O)[C@H](C)NC(=O)C[C@H](O)[C@H](CC(C)C)NC(=O)[C@@H](NC(=O)[C@@H](NC(=O)CC(C)C)C(C)C)C(C)C)[C@@H](O)CC(O)=O
InChI
1S/C34H63N5O9/c1-17(2)12-23(37-33(47)31(21(9)10)39-34(48)30(20(7)8)38-27(42)14-19(5)6)25(40)15-28(43)35-22(11)32(46)36-24(13-18(3)4)26(41)16-29(44)45/h17-26,30-31,40-41H,12-16H2,1-11H3,(H,35,43)(H,36,46)(H,37,47)(H,38,42)(H,39,48)(H,44,45)/t22-,23-,24-,25-,26-,30-,31-/m0/s1
Clé InChI
FAXGPCHRFPCXOO-LXTPJMTPSA-N
Vous recherchez des produits similaires ? Visite Guide de comparaison des produits
Application
- comme composant du tampon synaptoneurosome pour homogénéiser le striatum de C57BL/6
- comme composant du tampon de lyse de la kinase 5 dépendante de la cycline (Cdk5)
- comme inhibiteur pour déterminer l'activité chymotrypsine de la langouste de Californie (Panulirus interruptus)
Actions biochimiques/physiologiques
Notes préparatoires
Les solutions mères à 1 mg/ml sont stables pendant au moins une semaine à 4 °C. Une solution à 1 mM dans du méthanol ou du DMSO est stable pendant des mois à -20 °C. Si les solutions deviennent jaune plus foncé, c′est que le réactif s'hydrolyse.
Une concentration de travail de 1 μM est stable pendant au moins un jour à température ambiante.
Code de la classe de stockage
11 - Combustible Solids
Classe de danger pour l'eau (WGK)
WGK 2
Point d'éclair (°F)
Not applicable
Point d'éclair (°C)
Not applicable
Équipement de protection individuelle
Eyeshields, Gloves, type N95 (US)
Certificats d'analyse (COA)
Recherchez un Certificats d'analyse (COA) en saisissant le numéro de lot du produit. Les numéros de lot figurent sur l'étiquette du produit après les mots "Lot" ou "Batch".
Déjà en possession de ce produit ?
Retrouvez la documentation relative aux produits que vous avez récemment achetés dans la Bibliothèque de documents.
Les clients ont également consulté
Notre équipe de scientifiques dispose d'une expérience dans tous les secteurs de la recherche, notamment en sciences de la vie, science des matériaux, synthèse chimique, chromatographie, analyse et dans de nombreux autres domaines..
Contacter notre Service technique