911798
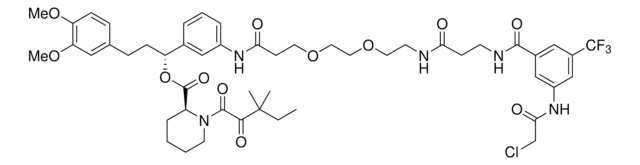
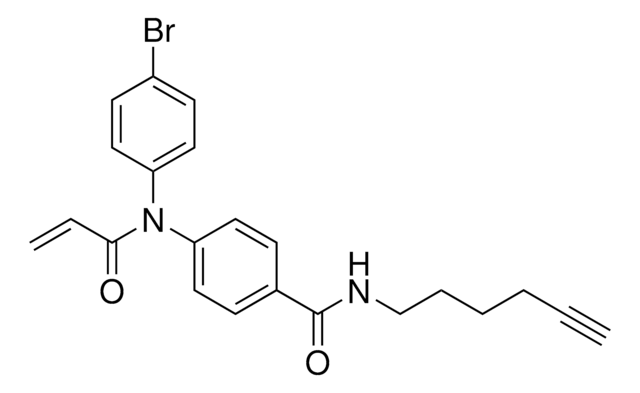
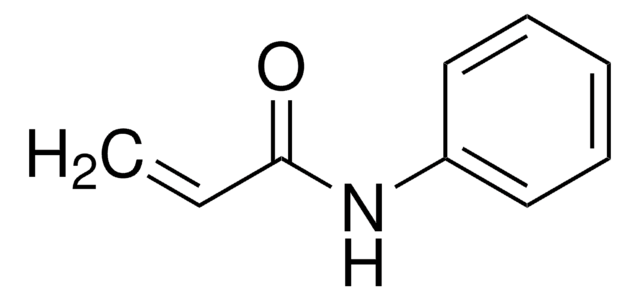
N-(4-Bromophenyl)-N-phenylacrylamide
≥95%
Synonyme(s) :
Electrophilic scout fragment, KB05, Scout fragment for targetable cysteine
About This Item
Produits recommandés
Niveau de qualité
Essai
≥95%
Forme
(Powder or crystals or solid or chunks)
Température de stockage
2-8°C
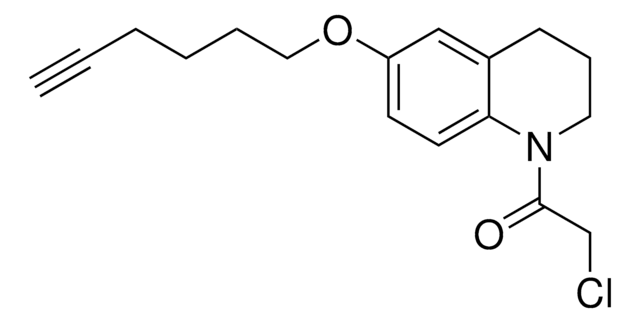
Chaîne SMILES
Brc1ccc(cc1)N(c2ccccc2)C(=O)C=C
InChI
1S/C15H12BrNO/c1-2-15(18)17(13-6-4-3-5-7-13)14-10-8-12(16)9-11-14/h2-11H,1H2
Clé InChI
WFQQVUPOAKOTGT-UHFFFAOYSA-N
Application
Autres remarques
Informations légales
Produit(s) apparenté(s)
Code de la classe de stockage
11 - Combustible Solids
Classe de danger pour l'eau (WGK)
WGK 3
Faites votre choix parmi les versions les plus récentes :
Certificats d'analyse (COA)
It looks like we've run into a problem, but you can still download Certificates of Analysis from our Documents section.
Si vous avez besoin d'assistance, veuillez contacter Service Clients
Déjà en possession de ce produit ?
Retrouvez la documentation relative aux produits que vous avez récemment achetés dans la Bibliothèque de documents.
Articles
Ligandability describes the propensity of a protein target to bind a small molecule with high affinity. It is a precursor to evaluating druggability, which requires more advanced translational pharmacological effects and drug-like properties in vivo.
Notre équipe de scientifiques dispose d'une expérience dans tous les secteurs de la recherche, notamment en sciences de la vie, science des matériaux, synthèse chimique, chromatographie, analyse et dans de nombreux autres domaines..
Contacter notre Service technique