C7698
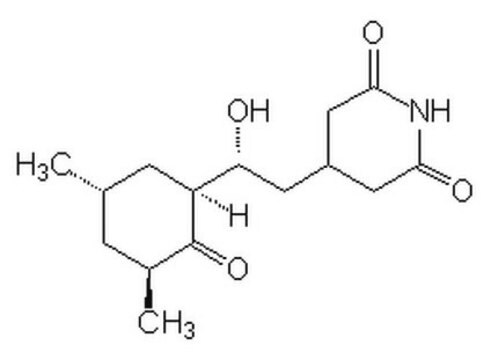
Cycloheximide
from microbial, ≥94% (TLC)
Synonyme(s) :
3-[2-(3,5-Diméthyl-2-oxocyclohexyl)-2-hydroxyéthyl]glutarimide, Actidione, Naramycine A
About This Item
Produits recommandés
Source biologique
microbial
Pureté
≥94% (TLC)
Forme
powder
Couleur
white to off-white
Solubilité
ethanol: soluble, clear to hazy
Spectre d'activité de l'antibiotique
fungi
yeast
Mode d’action
protein synthesis | interferes
Température de stockage
2-8°C
Chaîne SMILES
[H][C@]1(C[C@@H](C)C[C@H](C)C1=O)[C@H](O)CC2CC(=O)NC(=O)C2
InChI
1S/C15H23NO4/c1-8-3-9(2)15(20)11(4-8)12(17)5-10-6-13(18)16-14(19)7-10/h8-12,17H,3-7H2,1-2H3,(H,16,18,19)/t8-,9-,11-,12+/m0/s1
Clé InChI
YPHMISFOHDHNIV-FSZOTQKASA-N
Informations sur le gène
human ... FKBP1A(2280) , PIN1(5300)
Vous recherchez des produits similaires ? Visite Guide de comparaison des produits
Catégories apparentées
Description générale
Dans la recherche en biologie cellulaire et en biochimie, le cycloheximide a un comportement ambivalent vis-à-vis de l'apoptose, qu'il induit ou inhibe en fonction du type de cellules. Ses effets réversibles et rapides en font le choix idéal pour étudier les processus cellulaires et déterminer la demi-vie des protéines. Le cycloheximide a également de nombreuses applications en recherche biomédicale, où il inhibe la synthèse des protéines dans les cellules eucaryotes étudiées in vitro (à l'extérieur des organismes) et il suffit de le retirer pour inverser rapidement ses effets. Cela fait du cycloheximide un choix incontournable pour l'exploration en recherche biomédicale, en biologie cellulaire et en biochimie, où il offre polyvalence et précision du contrôle lors des expériences.
Application
- La cycloheximide a été utilisée comme inhibiteur de la synthèse des protéines dans certaines souches de levure dans le cadre d′expériences de chasse à la cycloheximide.
- Elle a été employée pour inhiber la traduction dans les cellules de mammifères
- Elle a été employée pour inhiber la croissance fongique.
Actions biochimiques/physiologiques
Spectre d'activité : Produit actif contre les levures et les champignons du type Candida, Aspergillus, Saccharomyces et Penicillium.
Caractéristiques et avantages
- Antibiotique de grande qualité convenant à de nombreuses applications de recherche.
- Produit couramment utilisé dans les applications de biologie cellulaire et de biochimie.
Stockage et stabilité
only to qualified or authorized persons.
Autres remarques
Produit comparable
Mention d'avertissement
Danger
Mentions de danger
Conseils de prudence
Classification des risques
Acute Tox. 2 Oral - Aquatic Chronic 2 - Muta. 2 - Repr. 1B
Code de la classe de stockage
6.1A - Combustible acute toxic Cat. 1 and 2 / very toxic hazardous materials
Classe de danger pour l'eau (WGK)
WGK 3
Point d'éclair (°F)
Not applicable
Point d'éclair (°C)
Not applicable
Équipement de protection individuelle
Eyeshields, Faceshields, Gloves, type P3 (EN 143) respirator cartridges
Certificats d'analyse (COA)
Recherchez un Certificats d'analyse (COA) en saisissant le numéro de lot du produit. Les numéros de lot figurent sur l'étiquette du produit après les mots "Lot" ou "Batch".
Déjà en possession de ce produit ?
Retrouvez la documentation relative aux produits que vous avez récemment achetés dans la Bibliothèque de documents.
Les clients ont également consulté
Notre équipe de scientifiques dispose d'une expérience dans tous les secteurs de la recherche, notamment en sciences de la vie, science des matériaux, synthèse chimique, chromatographie, analyse et dans de nombreux autres domaines..
Contacter notre Service technique