208743
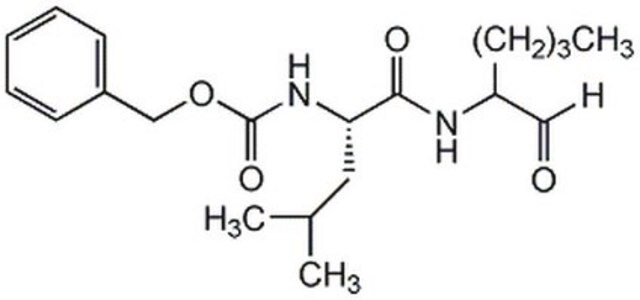
Calpain Inhibitor XI
The Calpain Inhibitor XI, also referenced under CAS 145731-49-3, controls the biological activity of Calpain. This small molecule/inhibitor is primarily used for Protease Inhibitors applications.
Sinônimo(s):
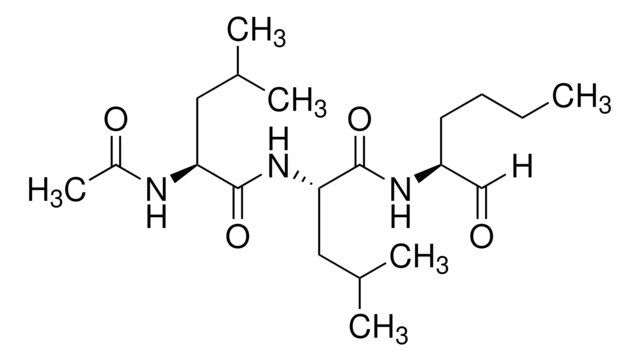
Calpain Inhibitor XI, Z-L-Abu-CONH(CH₂)₃-morpholine
Faça loginpara ver os preços organizacionais e de contrato
About This Item
Fórmula empírica (Notação de Hill):
C26H40N4O6
Número CAS:
Peso molecular:
504.62
Código UNSPSC:
12352200
Produtos recomendados
Nível de qualidade
Ensaio
≥95% (HPLC)
forma
solid
fabricante/nome comercial
Calbiochem®
condição de armazenamento
OK to freeze
desiccated (hygroscopic)
cor
white to off-white
solubilidade
DMSO: 5 mg/mL
Condições de expedição
ambient
temperatura de armazenamento
2-8°C
Descrição geral
A cell-permeable dipeptidyl α-ketoamide that acts as a potent, highly selective, reversible, and active site inhibitor of calpain-1 and -2 (Ki = 140 nM and 41 nM, respectively). Weakly inhibits cathepsin B (Ki = 6.9 µM). Reported to have a neuroprotective role in the central nervous system following focal ischemia. Also protects against virus-induced apoptotic myocardial injury in mice.
A cell-permeable dipeptidyl a-ketoamide that acts as a potent, highly selective, reversible, active site inhibitor of calpain-1 (Ki = 140 nM) and calpain-2 (Ki = 41 nM). Weakly inhibits cathepsin B (Ki = 6.9 µM). Shown to inhibit calpain-m-mediated degradation of neurofilament protein (NFP) (IC50 = 600 nM). Also shown to exhibit neuroprotective effects in the central nervous system following focal ischemia. Reported to protect against reovirus-induced myocarditis in mice.
Ações bioquímicas/fisiológicas
Cell permeable: yes
Primary Target
calpain 1, calpain 2
calpain 1, calpain 2
Product does not compete with ATP.
Reversible: yes
Target Ki: 140 nM and 41 nM, against calpain-1 and -2, respectively
Embalagem
Packaged under inert gas
Advertência
Toxicity: Standard Handling (A)
Sequência
Z-Leu-Abu-CONH(CH₂)₃-morpholine (Abu = α-aminobutyric acid)
forma física
Supplied as a trifluoroacetate salt.
Reconstituição
Following reconstitution aliquot and freeze (-20°C). Stock solutions are stable for up to 3 months at -20°C.
Outras notas
Blomgren, K., et al. 2001. J. Biol. Chem.276, 10191.
DeBiasi, R.L., et al. 2001. J. Virol.75, 351.
Saatman, K.E., et al. 2000. J. Cereb. Blood Flow Metab.20, 66.
Stelmasiak, Z., et al. 2000. Med. Sci. Monit.6, 426.
Blomgren, K., et al. 1999. J. Biol. Chem.274, 14046.
James, T., et al. 1998. J. Neurosci. Res.51, 218.
Li, Z., et al. 1996. J. Med. Chem.39, 4089.
Saatman, K.E, et al. 1996. Proc. Natl. Acad. Sci. USA93, 3428.
Bartus, R.T., et al. 1995. Neurol. Res.17, 249.
Bartus, R.T., et al. 1994. Stroke25, 2265.
DeBiasi, R.L., et al. 2001. J. Virol.75, 351.
Saatman, K.E., et al. 2000. J. Cereb. Blood Flow Metab.20, 66.
Stelmasiak, Z., et al. 2000. Med. Sci. Monit.6, 426.
Blomgren, K., et al. 1999. J. Biol. Chem.274, 14046.
James, T., et al. 1998. J. Neurosci. Res.51, 218.
Li, Z., et al. 1996. J. Med. Chem.39, 4089.
Saatman, K.E, et al. 1996. Proc. Natl. Acad. Sci. USA93, 3428.
Bartus, R.T., et al. 1995. Neurol. Res.17, 249.
Bartus, R.T., et al. 1994. Stroke25, 2265.
Informações legais
CALBIOCHEM is a registered trademark of Merck KGaA, Darmstadt, Germany
Código de classe de armazenamento
11 - Combustible Solids
Classe de risco de água (WGK)
WGK 1
Ponto de fulgor (°F)
Not applicable
Ponto de fulgor (°C)
Not applicable
Certificados de análise (COA)
Busque Certificados de análise (COA) digitando o Número do Lote do produto. Os números de lote e remessa podem ser encontrados no rótulo de um produto após a palavra “Lot” ou “Batch”.
Já possui este produto?
Encontre a documentação dos produtos que você adquiriu recentemente na biblioteca de documentos.
Nossa equipe de cientistas tem experiência em todas as áreas de pesquisa, incluindo Life Sciences, ciência de materiais, síntese química, cromatografia, química analítica e muitas outras.
Entre em contato com a assistência técnica