Wichtige Dokumente
S9697
Superoxid-Dismutase Rind
recombinant, expressed in E. coli, lyophilized powder, ≥2500 units/mg protein, ≥90% (SDS-PAGE)
Synonym(e):
Superoxid-Dismutase 1 Rind, Cytocuprein, Erythrocuprein, Hämocuprein, CU/ZN-SOD, SOD, SOD1, Superoxide: superoxide oxidoreductase
About This Item
Empfohlene Produkte
Biologische Quelle
bovine
Qualitätsniveau
Rekombinant
expressed in E. coli
Assay
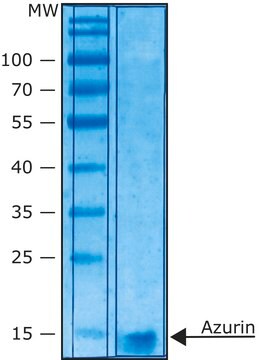
≥90% (SDS-PAGE)
Form
lyophilized powder
Spezifische Aktivität
≥2500 units/mg protein
Lagerbedingungen
(Tightly closed)
Methode(n)
inhibition assay: suitable
Farbe
white
Optimaler pH-Wert
7.8 (25 °C)
pH-Bereich
7.6-10.5
pI
4.95
Hinweis zur Sequenz
MATKAVCVLKGDGPVQGTIHFEAKGDTVVVTGSITGLTEGDHGFHVHQFGDNTQGCTSAGPHFNPLSKKHGGPKDEERHVGDLGNVTADKNGVAIVDIVDPLISLSGEYSIIGRTMVVHEKPDDLGRGGNEESTKTGNAGSRLACGVIGIAK
UniProt-Hinterlegungsnummer
Lagertemp.
−20°C
Allgemeine Beschreibung
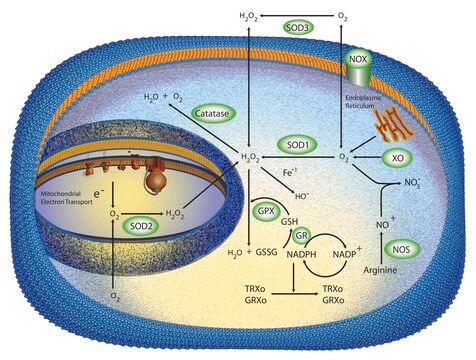
SOD aus Rindererythrozyten war die erste in Säugetiergeweben gefundene SOD. Es gibt drei Formen der SOD, die sich jeweils in den Metallionen im aktiven Zentrum unterscheiden. Diese sind Cu+2/Zn+2, Mn+2 und Fe+2 SOD. In Wirbeltieren befindet sich die Cu/Zn-SOD im Zytoplasma, Chloroplast und kann im extrazellulären Raum von Mitochondrien auftreten, wogegen Mn-SOD im mitochondrialen Matrixraum und Peroxisom vorkommt. Fe-SOD kommt in Prokaryoten und manchen höheren Pflanzen im Chloroplast vor.
Anwendung
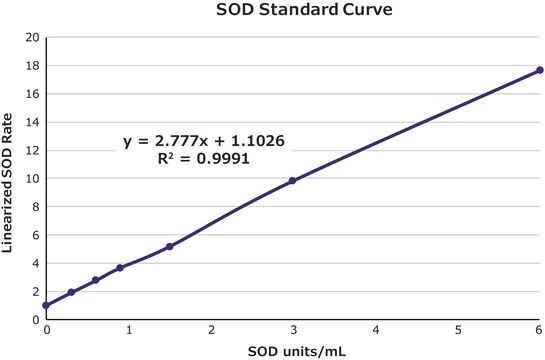
- zum Erzeugen einer Kalibrierungskurve für die Bewertung der Enzymaktivitäten von Superoxiddismutase (SOD)
- in einer Studie zum Untersuchen, wo Lipoproteine den L-Arginin-Stickoxid-Weg beeinflussen können
- in einer Studie zum Untersuchen der Massenspektren für die durch Carbonat-Anion-Radikal eingeleitete posttranslationale Modifikation von Tryptophan zu Kynurenin in humaner Cu-, Zn-Superoxiddismutase
Biochem./physiol. Wirkung
Einheitendefinition
Angaben zur Herstellung
Rekonstituierung
Hinweis zur Analyse
Aufgrund der Abwesenheit von Tryptophan weist SOD keinen signifikanten Absorptionspeak bei 280 nM auf.
Sonstige Hinweise
Antikörper
Ähnliches Produkt
Signalwort
Danger
H-Sätze
P-Sätze
Gefahreneinstufungen
Resp. Sens. 1
Lagerklassenschlüssel
10 - Combustible liquids
WGK
WGK 1
Flammpunkt (°F)
Not applicable
Flammpunkt (°C)
Not applicable
Hier finden Sie alle aktuellen Versionen:
Besitzen Sie dieses Produkt bereits?
In der Dokumentenbibliothek finden Sie die Dokumentation zu den Produkten, die Sie kürzlich erworben haben.
Kunden haben sich ebenfalls angesehen
Artikel
Oxidative stress is mediated, in part, by reactive oxygen species produced by multiple cellular processes and controlled by cellular antioxidant mechanisms such as enzymatic scavengers or antioxidant modulators. Free radicals, such as reactive oxygen species, cause cellular damage via cellular.
Unser Team von Wissenschaftlern verfügt über Erfahrung in allen Forschungsbereichen einschließlich Life Science, Materialwissenschaften, chemischer Synthese, Chromatographie, Analytik und vielen mehr..
Setzen Sie sich mit dem technischen Dienst in Verbindung.