495604
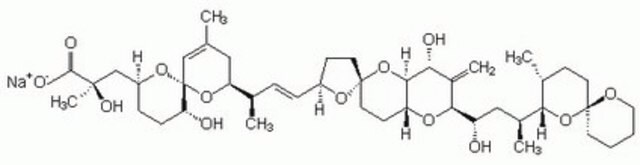
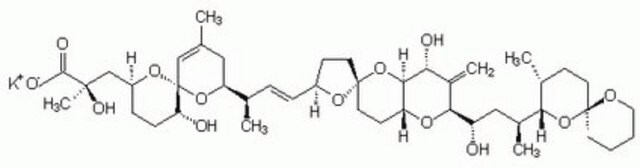
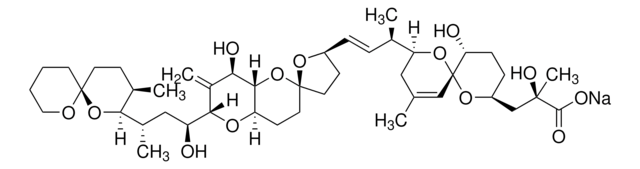
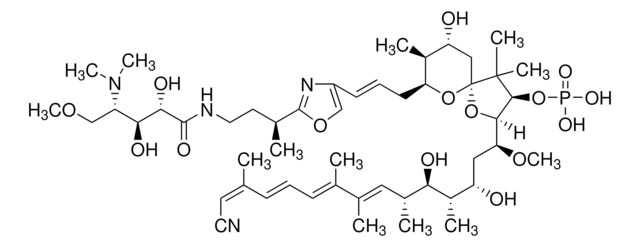
Okadaic acid
from Prorocentrum sp., ≥95% (HPLC), solid (glassy), protein phosphatase 1 inhibitor, Calbiochem
Synonym(e):
Okadainsäure, Prorocentrum sp., OS
About This Item
Empfohlene Produkte
Produktbezeichnung
Okadainsäure, Prorocentrum sp., Okadaic Acid, CAS 78111-17-8, is a highly potent inhibitor of protein phosphatase 1 (IC₅₀ = 10-15 nM) and 2A (IC₅₀ = 0.1 nM).
Qualitätsniveau
Assay
≥95% (HPLC)
Form
solid (glassy)
Hersteller/Markenname
Calbiochem®
Lagerbedingungen
OK to freeze
protect from light
Farbe
colorless
Löslichkeit
DMF: soluble
chloroform: soluble
ethanol: soluble
methanol: soluble
Versandbedingung
ambient
Lagertemp.
−20°C
InChI
1S/C44H68O13/c1-25-21-34(55-44(23-25)35(46)12-11-31(54-44)24-41(6,50)40(48)49)26(2)9-10-30-14-18-43(53-30)19-15-33-39(57-43)36(47)29(5)38(52-33)32(45)22-28(4)37-27(3)13-17-42(56-37)16-7-8-20-51-42/h9-10,23,26-28,30-39,45-47,50H,5,7-8,11-22,24H2,1-4,6H3,(H,48,49)/b10-9+/t26-,27-,28+,30+,31+,32+,33-,34+,35-,36-,37?,38+,39?,41-,42+,43-,44-/m1/s1
InChIKey
QNDVLZJODHBUFM-AAWJMCDUSA-N
Allgemeine Beschreibung
Biochem./physiol. Wirkung
Proteinphosphatase
Verpackung
Warnhinweis
Rekonstituierung
Sonstige Hinweise
Kiguchi, K., et al. 1994. Cell Growth Differentiation5, 995.
Ohaka, Y., et al. 1993. Biochem. Biophys. Res. Commun. 197, 916.
Gopalakrishna, R., et al. 1992. Biochem. Biophys. Res. Commun. 189, 950.
Kreienbuhl, P., et al. 1992. Blood80, 2911.
Nomura, M., et al. 1992. Biochemistry31, 11915.
Song, Q., et al. 1992. J. Cell Physiol.153, 550.
Tada, Y., et al. 1992. Immunopharmacol.24, 17.
Cohen, P., et al. 1990. Trends Biochem. Sci.15, 98.
Cohen, P. 1989. Annu. Rev. Biochem.58, 453.
Cohen, P., and Cohen, P.T. 1989. J. Biol. Chem.264, 21435.
Haystead, T.A., et al. 1989. Nature337, 78.
Rechtliche Hinweise
Signalwort
Danger
H-Sätze
Gefahreneinstufungen
Acute Tox. 3 Dermal - Acute Tox. 3 Inhalation - Acute Tox. 3 Oral - Skin Irrit. 2
Lagerklassenschlüssel
6.1C - Combustible acute toxic Cat.3 / toxic compounds or compounds which causing chronic effects
WGK
WGK 3
Flammpunkt (°F)
Not applicable
Flammpunkt (°C)
Not applicable
Analysenzertifikate (COA)
Suchen Sie nach Analysenzertifikate (COA), indem Sie die Lot-/Chargennummer des Produkts eingeben. Lot- und Chargennummern sind auf dem Produktetikett hinter den Wörtern ‘Lot’ oder ‘Batch’ (Lot oder Charge) zu finden.
Besitzen Sie dieses Produkt bereits?
In der Dokumentenbibliothek finden Sie die Dokumentation zu den Produkten, die Sie kürzlich erworben haben.
Kunden haben sich ebenfalls angesehen
Unser Team von Wissenschaftlern verfügt über Erfahrung in allen Forschungsbereichen einschließlich Life Science, Materialwissenschaften, chemischer Synthese, Chromatographie, Analytik und vielen mehr..
Setzen Sie sich mit dem technischen Dienst in Verbindung.