X-tremeGENETM HP、X-tremeGENETM 9、X-tremeGENETM 360トランスフェクション試薬
細胞のトランスフェクションを成功させる可能性は、細胞型、プロトコル、トランスフェクション試薬の組成によって大きく異なります。X-tremeGENE™トランスフェクション試薬は、DNA、small DNA、CRISPR/Cas9成分などの多様な分子を有する一般的かつトランスフェクションが困難な細胞を効率的にトランスフェクションするよう設計されています。
新しい製品:X-tremeGENE™ 360トランスフェクション試薬は、トランスフェクションが困難な細胞型や一般的な細胞型にsiRNA/miRNA、プラスミドDNA、CRISPR/Cas9成分を送達するための、高性能で多目的かつ信頼性の高いソリューションです。詳細はsigmaaldrich.com/xtg360roを参照してください。

図1.X-tremeGENE™ HP試薬によるヒト初代線維芽細胞の効率的なトランスフェクション。
初代線維芽細胞をヒト包皮から単離し、4 μLのX-tremeGENE™HP試薬と1 μgのGFPコードプラスミドDNAを6ウェル細胞培養プレートでトランスフェクションしました。トランスフェクションから48時間後にGFPの発現状態を可視化しました。左側の図はGFPの蛍光を示し、右側の図は対応する明視野イメージを示しています。

図2.ヒト間葉系幹細胞において、X-tremeGENE™ HP試薬およびX-tremeGENE™ 9試薬は競合試薬を上回る性能。
ヒト間葉系幹細胞を、4名のドナーの骨髄吸引生検から分離しました。X-tremeGENE™ HP試薬(XHP)、X-tremeGENE™ 9試薬(X9)、および競合薬(LTX)を用いて、指定の比率で細胞をトランスフェクションしました(試薬[μL]:GFPをコードするプラスミドDNA[μg]。比率2:1は、X-tremeGENE™ 9試薬を使用して試験していません)。トランスフェクションしていない細胞を対照(陰性)として用いました。トランスフェクションの48時間後にFACS解析を実施しました。

図3.X-tremeGENE™ HP DNAトランスフェクション試薬は、トランスフェクション困難な細胞型において競合試薬を上回る性能。
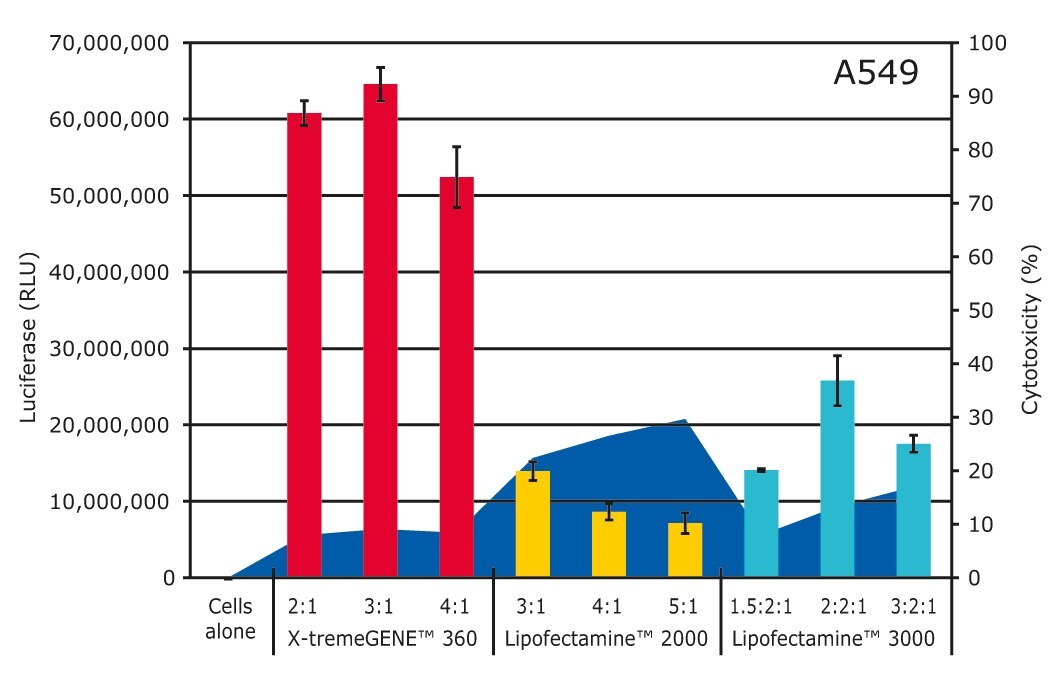
図4.X-tremeGENETM 360は、A549細胞で試験されたLipofectamine試薬を上回る性能。X-tremeGENETM 360、Lipofectamine® 2000(Thermo Fisher Scientific)、Lipofectamine® 3000(Thermo Fisher Scientific)を用いて、A549細胞にルシフェラーゼをコードするプラスミドDNAを、指定の試薬/DNA比で24時間トランスフェクションした。トランスフェクションは、従来のアッセイ法を用いてルシフェラーゼ活性により測定した。細胞毒性は、細胞のみと比較して、損傷細胞のサイトゾルからのLDH放出を定量することによって評価した。X-tremeGENETM 360を最適な比率でトランスフェクションした細胞では、Lipofectamine® 2000またはLipofectamine® 3000をトランスフェクションした細胞と比較して、導入遺伝子発現量が高く、細胞毒性が低かった。
X-tremeGENE™ HP試薬(XHP)および競合試薬(LTXおよびL2K)を用いて、指定された比率(試薬[μL]:GFPをコードするプラスミドDNA[μg])で細胞をトランスフェクションしました。トランスフェクション効率は、GFP蛍光顕微鏡を用いて可視化しました。
細胞型特有の製品の推奨 |
|---|
注記:上記のデータは、GFPをコードするpcDNA3.1プラスミドまたはルシフェラーゼをコードするpCIプラスミドのいずれかを、サイトメガロウイルス(CMV)プロモーターとともに用いて得られたものです。これらの推奨は実験結果に基づくガイドラインです。最適な試薬:DNA比率は、経験的に決定しなければなりません。
アプリケーションの表 |
|---|
続きを確認するには、ログインするか、新規登録が必要です。
アカウントをお持ちではありませんか?