M3529
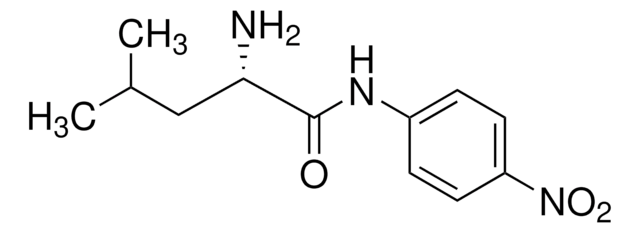
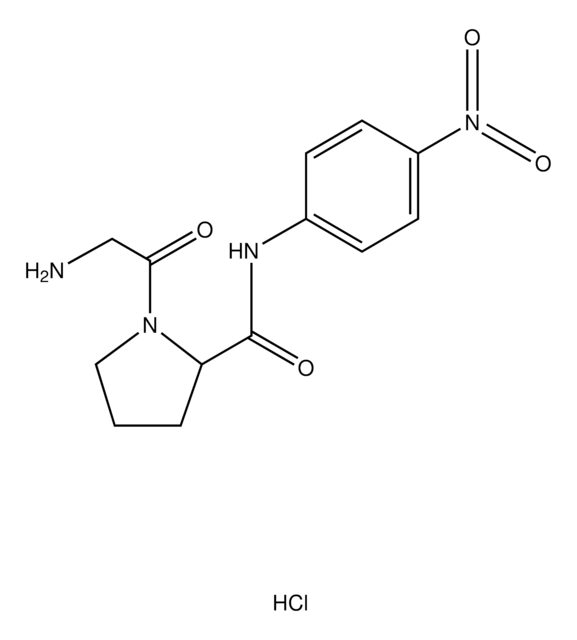
L-Methionine p-nitroanilide
≥98% (TLC), suitable for ligand binding assays
About This Item
Produits recommandés
Nom du produit
L-Methionine p-nitroanilide,
Essai
≥98% (TLC)
Forme
powder
Technique(s)
ligand binding assay: suitable
Couleur
white to faint yellow
Température de stockage
−20°C
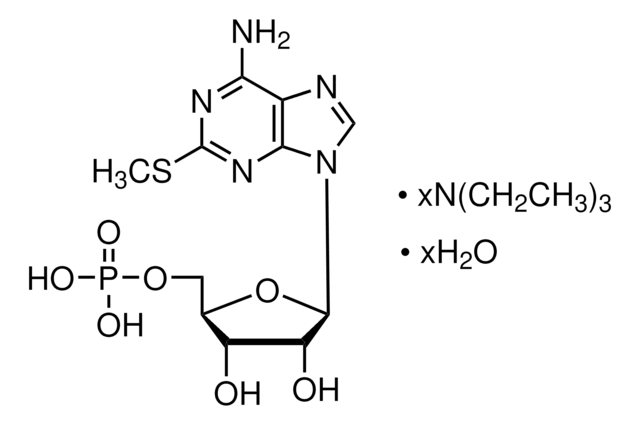
Chaîne SMILES
CSCC[C@H](N)C(=O)Nc1ccc(cc1)[N+]([O-])=O
InChI
1S/C11H15N3O3S/c1-18-7-6-10(12)11(15)13-8-2-4-9(5-3-8)14(16)17/h2-5,10H,6-7,12H2,1H3,(H,13,15)/t10-/m0/s1
Clé InChI
PLBWRAWSHVJPTL-JTQLQIEISA-N
Vous recherchez des produits similaires ? Visite Guide de comparaison des produits
Catégories apparentées
Actions biochimiques/physiologiques
Code de la classe de stockage
11 - Combustible Solids
Classe de danger pour l'eau (WGK)
WGK 3
Point d'éclair (°F)
Not applicable
Point d'éclair (°C)
Not applicable
Faites votre choix parmi les versions les plus récentes :
Certificats d'analyse (COA)
Vous ne trouvez pas la bonne version ?
Si vous avez besoin d'une version particulière, vous pouvez rechercher un certificat spécifique par le numéro de lot.
Déjà en possession de ce produit ?
Retrouvez la documentation relative aux produits que vous avez récemment achetés dans la Bibliothèque de documents.
Notre équipe de scientifiques dispose d'une expérience dans tous les secteurs de la recherche, notamment en sciences de la vie, science des matériaux, synthèse chimique, chromatographie, analyse et dans de nombreux autres domaines..
Contacter notre Service technique