N8129
β-Nicotinamide-adénine-dinucléotide, réduit disodium salt hydrate
≥97% (HPLC)
Synonyme(s) :
β-DPNH, β-NADH, DPNH, Diphosphopyridine-nucléotide, forme réduite, NADH
About This Item
Produits recommandés
Niveau de qualité
Pureté
≥97% (HPLC)
≥97% (spectrophotometric assay)
Forme
powder
Température de stockage
−20°C
Chaîne SMILES
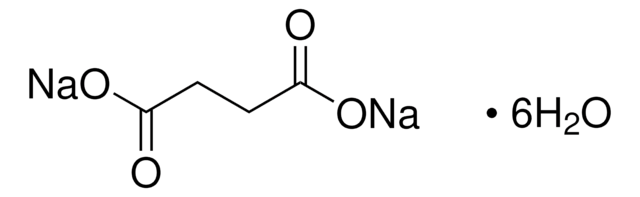
O.[Na+].[Na+].NC(=O)C1=CN(C=CC1)[C@@H]2O[C@H](COP([O-])(=O)OP([O-])(=O)OC[C@H]3O[C@H]([C@H](O)[C@@H]3O)n4cnc5c(N)ncnc45)[C@@H](O)[C@H]2O
InChI
1S/C21H29N7O14P2.2Na.H2O/c22-17-12-19(25-7-24-17)28(8-26-12)21-16(32)14(30)11(41-21)6-39-44(36,37)42-43(34,35)38-5-10-13(29)15(31)20(40-10)27-3-1-2-9(4-27)18(23)33;;;/h1,3-4,7-8,10-11,13-16,20-21,29-32H,2,5-6H2,(H2,23,33)(H,34,35)(H,36,37)(H2,22,24,25);;;1H2/q;2*+1;/p-2/t10-,11-,13-,14-,15-,16-,20-,21-;;;/m1.../s1
Clé InChI
FWBNCIFELNNJCX-UHOVGGJYSA-L
Vous recherchez des produits similaires ? Visite Guide de comparaison des produits
Application
Actions biochimiques/physiologiques
En tant que réactif, NADH peut être utilisé dans les essais de cycles enzymatiques pour amplifier la détection de l′activité des enzymes ou métabolites significatifs du point de vue biologique présents en faibles concentrations.
Conditionnement
Code de la classe de stockage
13 - Non Combustible Solids
Classe de danger pour l'eau (WGK)
WGK 3
Point d'éclair (°F)
Not applicable
Point d'éclair (°C)
Not applicable
Équipement de protection individuelle
Eyeshields, Gloves, type N95 (US)
Certificats d'analyse (COA)
Recherchez un Certificats d'analyse (COA) en saisissant le numéro de lot du produit. Les numéros de lot figurent sur l'étiquette du produit après les mots "Lot" ou "Batch".
Déjà en possession de ce produit ?
Retrouvez la documentation relative aux produits que vous avez récemment achetés dans la Bibliothèque de documents.
Les clients ont également consulté
Articles
Learn about the four membrane-bound protein complexes that make up the electron transport chain metabolic pathway supplying energy as ATP for cellular respiration.
Oxidative stress is mediated, in part, by reactive oxygen species produced by multiple cellular processes and controlled by cellular antioxidant mechanisms such as enzymatic scavengers or antioxidant modulators. Free radicals, such as reactive oxygen species, cause cellular damage via cellular.
Protocoles
Enzymatic Assay of Malic Dehydrogenase (EC 1.1.1.37)
Enzymatic Assay of Fructose-6-Phosphate Kinase Pyrophosphate Dependent
Notre équipe de scientifiques dispose d'une expérience dans tous les secteurs de la recherche, notamment en sciences de la vie, science des matériaux, synthèse chimique, chromatographie, analyse et dans de nombreux autres domaines..
Contacter notre Service technique