C7352
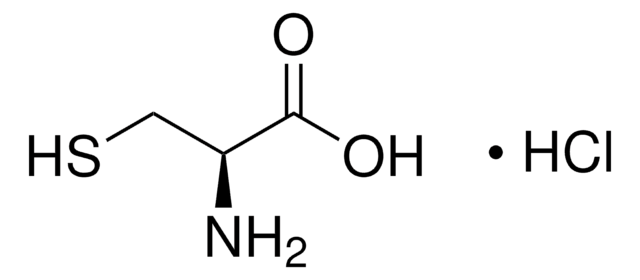
L-cystéine
from non-animal source, BioReagent, suitable for cell culture, ≥98%
Synonyme(s) :
Acide (R)-2-amino-3-mercaptopropionique
About This Item
Produits recommandés
Source biologique
non-animal source
Gamme de produits
BioReagent
Essai
≥98%
Forme
crystalline powder
Technique(s)
cell culture | mammalian: suitable
Impuretés
endotoxin, tested
Couleur
white
Pf
240 °C (dec.) (lit.)
Solubilité
H2O: 25 mg/mL
Chaîne SMILES
N[C@@H](CS)C(O)=O
InChI
1S/C3H7NO2S/c4-2(1-7)3(5)6/h2,7H,1,4H2,(H,5,6)/t2-/m0/s1
Clé InChI
XUJNEKJLAYXESH-REOHCLBHSA-N
Vous recherchez des produits similaires ? Visite Guide de comparaison des produits
Description générale
Application
- comme supplément dans un milieu TYI-S-33 (trypticase/extrait de levures/fer-sérum) pour la culture de Giardia lamblia, pour fabriquer une solution enzymatique dans du milieu d'Eagle modifié par Dulbecco (DMEM) afin d'établir une culture d'hippocampe
- pour évaluer son effet protecteur vis-à-vis de la toxicité de l'acrylamide sur les testicules
- dans la préparation d'une solution de dilution Tris/acide acétique pour la cryoconservation du sperme
- comme additif pour fabriquer une solution de digestion à la papaïne
Actions biochimiques/physiologiques
Autres remarques
Code de la classe de stockage
11 - Combustible Solids
Classe de danger pour l'eau (WGK)
WGK 1
Point d'éclair (°F)
Not applicable
Point d'éclair (°C)
Not applicable
Équipement de protection individuelle
dust mask type N95 (US), Eyeshields, Gloves
Faites votre choix parmi les versions les plus récentes :
Déjà en possession de ce produit ?
Retrouvez la documentation relative aux produits que vous avez récemment achetés dans la Bibliothèque de documents.
Les clients ont également consulté
Articles
Antioxidants protect biological systems from oxidative damage produced by oxygen-containing free radicals and from redoxactive transition metal ions such as iron, copper, and cadmium.
Protocoles
Separation of L-Alanine; Glycine; L-Valine; L-Leucine; L-Isoleucine; L-Proline; L-Methionine; L-Serine; L-Threonine; L-Phenylalanine; L-Aspartic acid; L-4-Hydroxyproline; L-Cysteine; L-Glutamic acid; L-Asparagine; L-Lysine; L-Glutamine; L-Histidine; L-Tyrosine; L-Tryptophan; L-Cystine
Chromatograms
application for HPLCNotre équipe de scientifiques dispose d'une expérience dans tous les secteurs de la recherche, notamment en sciences de la vie, science des matériaux, synthèse chimique, chromatographie, analyse et dans de nombreux autres domaines..
Contacter notre Service technique