Wichtige Dokumente
C7352
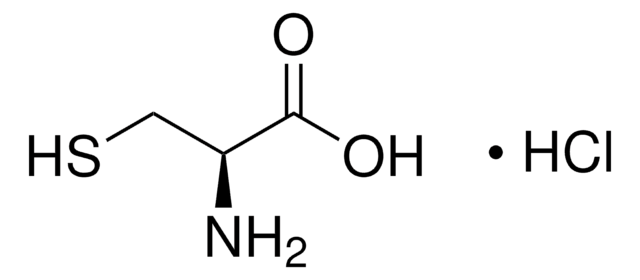
L-Cystein
from non-animal source, BioReagent, suitable for cell culture, ≥98%
Synonym(e):
(R)-2-Amino-3-mercaptopropionsäure
About This Item
Empfohlene Produkte
Biologische Quelle
non-animal source
Produktlinie
BioReagent
Assay
≥98%
Form
crystalline powder
Methode(n)
cell culture | mammalian: suitable
Verunreinigungen
endotoxin, tested
Farbe
white
mp (Schmelzpunkt)
240 °C (dec.) (lit.)
Löslichkeit
H2O: 25 mg/mL
SMILES String
N[C@@H](CS)C(O)=O
InChI
1S/C3H7NO2S/c4-2(1-7)3(5)6/h2,7H,1,4H2,(H,5,6)/t2-/m0/s1
InChIKey
XUJNEKJLAYXESH-REOHCLBHSA-N
Suchen Sie nach ähnlichen Produkten? Aufrufen Leitfaden zum Produktvergleich
Allgemeine Beschreibung
Anwendung
- als Mediumzusatz für Trypticase-Hefeextrakt-Eisen-Serum (TYI-S-33)-Medium zur Kultivierung von Giardia lamblia, zur Herstellung einer Enzymlösung in Dulbeccos modifiziertem Eagle-Medium (DMEM) für die Etablierung einer Hippocampus-Kultur
- zum Testen seiner schützenden Wirkung bei der durch Acrylamid induzierten Toxizität in den Hoden
- für die Herstellung einer Tris-Acetat-Extenderlösung für die Kryokonservierung von Sperma
- als Additiv für die Herstellung einer Papain-Verdaulösung
Biochem./physiol. Wirkung
Sonstige Hinweise
Anwendung
Lagerklassenschlüssel
11 - Combustible Solids
WGK
WGK 1
Flammpunkt (°F)
Not applicable
Flammpunkt (°C)
Not applicable
Persönliche Schutzausrüstung
dust mask type N95 (US), Eyeshields, Gloves
Hier finden Sie alle aktuellen Versionen:
Besitzen Sie dieses Produkt bereits?
In der Dokumentenbibliothek finden Sie die Dokumentation zu den Produkten, die Sie kürzlich erworben haben.
Kunden haben sich ebenfalls angesehen
Artikel
Antioxidants protect biological systems from oxidative damage produced by oxygen-containing free radicals and from redoxactive transition metal ions such as iron, copper, and cadmium.
Protokolle
Separation of L-Alanine; Glycine; L-Valine; L-Leucine; L-Isoleucine; L-Proline; L-Methionine; L-Serine; L-Threonine; L-Phenylalanine; L-Aspartic acid; L-4-Hydroxyproline; L-Cysteine; L-Glutamic acid; L-Asparagine; L-Lysine; L-Glutamine; L-Histidine; L-Tyrosine; L-Tryptophan; L-Cystine
Chromatograms
application for HPLCUnser Team von Wissenschaftlern verfügt über Erfahrung in allen Forschungsbereichen einschließlich Life Science, Materialwissenschaften, chemischer Synthese, Chromatographie, Analytik und vielen mehr..
Setzen Sie sich mit dem technischen Dienst in Verbindung.